Kaliumheptafluoroniobat
Kaliumheptafluoroniobat ist eine anorganische chemische Verbindung des Kaliums aus der Gruppe der Kaliumfluorkomplexe.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
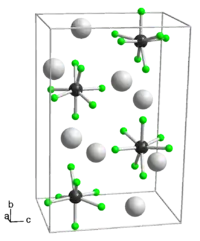 | ||||||||||||||||
| _ K+ _ Nb5+ _ F− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Kaliumheptafluoroniobat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | K2[NbF7] | |||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 304,09 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
3,19 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
löslich in Wasser (80 g·l−1 bei 18 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Kaliumheptafluoroniobat kann durch Reaktion von Niob(V)-oxid mit Flusssäure und Kaliumhydrogendifluorid gewonnen werden.[3]
Eigenschaften
Kaliumheptafluoroniobat ist ein hygroskopischer weißer Feststoff, der löslich in Wasser ist und in Form kleiner, stark glänzender Nadeln vorliegt.[1] [NbF7]2− hydrolysiert leicht zu [NbOF5]2−.[3] Kaliumheptafluoroniobat besitzt eine monokline Kristallstruktur mit der Raumgruppe P21/c (Raumgruppen-Nr. 14) und den Gitterparametern a = 5,846 Å, b = 12,69 Å, c = 8,515 Å und β = 90,0°.[5]
Verwendung
Kaliumheptafluoroniobat wird zur elektrochemischen Synthese von Niobdiborid NbB2 verwendet.[4] Es dient auch als Zwischenprodukt zur Herstellung von Niob aus Nioberzen wie Niobit durch Schmelzflusselektrolyse bei ca. 800 °C.[6] K2[NbF7] dotiert mit Mn4+ wurde als Leuchtstoff für warmweiße LED vorgeschlagen, da es unter UV bzw. blauer Anregung intensive schmalbandige rote Lumineszenz aufweist.[7]
Einzelnachweise
- Datenblatt Kaliumheptafluoroniobat bei AlfaAesar, abgerufen am 14. Oktober 2013 (PDF) (JavaScript erforderlich).
- Anatoly Agulyansky: Chemistry of Tantalum and Niobium Fluoride Compounds. Elsevier, 2004, ISBN 0-08-052902-X, S. 64 (eingeschränkte Vorschau in der Google-Buchsuche).
- Georg Brauer, unter Mitarbeit von Marianne Baudler u. a. (Hrsg.): Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I. Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 262.
- Datenblatt Potassium heptafluoroniobate(V), 98% bei Sigma-Aldrich, abgerufen am 14. Oktober 2013 (PDF).
- G.M. Brown, L.A. Walker; Refinement of the Structure of Potassium Heptafluoroniobate, K2NbF7, from Neutron-Diffraction Data. In: Acta Crystallographica, 20, 1966, S. 220–229, doi:10.1107/S0365110X66000458.
- Hans Günther Hirschberg: Handbuch der Verfahrenstechnik und Anlagenbau: Chemie, Technik, Wirtschaftlichkeit. Springer DE, 1999, ISBN 3-642-58357-1, S. 284 (eingeschränkte Vorschau in der Google-Buchsuche).
- Thomas Jansen, Florian Baur, Thomas Jüstel: Red emitting K2NbF7:Mn4+ and K2TaF7:Mn4+ for warm-white LED applications. In: Journal of Luminescence. Band 192, S. 644–652, doi:10.1016/j.jlumin.2017.07.061.
