Ibogain
Ibogain ist ein Indolalkaloid mit im weiteren Sinne halluzinogener Wirkung. Es kommt in verschiedenen Hundsgiftgewächsen vor, vor allem in Tabernanthe iboga.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
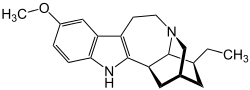 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Ibogain | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C20H26N2O | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 310,44 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Geschichte
Ibogain wurde erstmals 1901 sowohl von Dybowski und Landrin[4] als auch von Haller und Heckel aus der Wurzelrinde der Tabernanthe iboga extrahiert.

Im selben Jahr beobachteten französische Pharmakologen eine ungewöhnliche Art der Erregung bei Tieren. Phisalix vermutete eine halluzinogene Wirkung aufgrund des veränderten Verhaltens von Hunden. Nach weiteren klinischen Tests wurde das Alkaloid zur Unterstützung der Rekonvaleszenz und bei Neurasthenie empfohlen, wurde dann aber kaum eingesetzt. In den 1940er Jahren veröffentlichten Raymond-Hamet und Kollegen Untersuchungen zur pharmakologischen Wirkung auf isoliertes Zellgewebe und das kardiovaskuläre System.
In Frankreich wurde von 1939 bis 1967 ein Stimulans namens Lambarene verkauft. Eine Tablette enthielt 8 mg Ibogain, welches aus Tabernanthe manii, einer Verwandten der Tabernanthe iboga, extrahiert wurde. Ein weiterer Ibogainextrakt, Iperton, wurde als Tonikum verkauft.
Die anspruchsvolle Totalsynthese gelang 1966 George Büchi.[5] Seitdem wurden weitere totalsynthetische Zugänge entwickelt,[6] die sämtlich nur von akademischem Interesse sind.
Iboga und Ibogain sind bereits seit 1967 in den USA verboten (Schedule I). 1989 wurde Ibogain in die Dopingliste des Internationalen Olympischen Komitees aufgenommen.
Wirkung
Ibogain wirkt in geringen Dosen stimulierend. Höhere Dosierungen (ab 5–10 mg/kg Körpergewicht) lösen Visionen aus, d. h., bei geschlossenen Augen werden in einer Art traumähnlichem Erleben schnelle Abfolgen von Bildern und Filmen gesehen, oft mit intensivem emotionalem und auch religiös-mystischem Empfinden. Halluzinationen bei geöffneten Augen treten hingegen kaum auf. Daher ist die Wirkung nicht mit der von bekannteren Psychedelika wie LSD vergleichbar. Es wurde vorgeschlagen, statt „halluzinogen“ das Wort „oneirogen“, d. h. traumerzeugend, zu verwenden. Die Wirkung hält zwischen acht und zwölf Stunden an, wobei die akut visionäre Phase nur vier bis acht Stunden dauert. Rund ein Fünftel der Konsumenten berichtet von subjektiven Nachwirkungen noch 24 Stunden nach der Einnahme, 15 Prozent sogar noch nach 36 Stunden. Noch höhere Dosierungen führen zu Krämpfen, Lähmungserscheinungen und können im Tod durch Atemstillstand enden. Des Weiteren besteht die Gefahr von Herzrhythmusstörungen, was im schlimmsten Fall zum plötzlichen Herztod führen kann.[7][8]
Ibogain vermindert den Blutdruck, den Appetit und die Verdauungstätigkeit und ist ein schwacher Acetylcholinesterasehemmer.[9]
Es gibt Personen, die auf Ibogaingaben allergisch reagieren; deshalb sollte zunächst stets eine geringe Testdosis verwendet werden, um eine mögliche Reaktion abzuwarten.[10]
Medizinische Verwendung
Verwendung zum Drogenentzug
In den 1960er-Jahren entdeckte Howard Lotsof die suchtunterbrechende oder suchtvermindernde Wirkung[11] von Ibogain und erhielt in den 1980er und 90er Jahren mehrere US-Patente für die Therapie mit Ibogain. Ein erforschter Effekt ist sowohl die Verbesserung der Entzugssymptomatik bei Opiatentzug als auch der potentielle Nutzen in der Behandlung von Nikotin-, Methamphetamin-,[12] Alkohol- und anderer Substanzabhängigkeit.[13]
Seit Mitte der 1980er Jahre bieten Selbsthilfeorganisationen und Privatleute, aber auch Ärzte, den Entzug mit Ibogain an, sowohl in klinischer wie auch in informeller Umgebung. Während Ibogain in den meisten Ländern zwar nicht als Medikament zugelassen, aber auch nicht illegal ist, hat sich in den USA aufgrund des dortigen Verbots ein Schwarzmarkt gebildet.[14] Dennoch wurde es als Hilfsmittel in der Psychotherapie verwendet.[15]
Der genaue Wirkungsmechanismus, nach dem das Alkaloid Abhängigkeiten durchbrechen soll, ist nicht bekannt. Probanden, denen Ibogain verabreicht wurde, beschrieben wiederholt, dass sie während des Rausches Situationen wiedererlebt hatten, die ihrer Meinung nach für ihre Abhängigkeit ausschlaggebend waren. Andere berichteten von Visionen, die ihnen halfen, die ihrer Sucht zugrundeliegenden Ängste zu erkennen und zu überwinden.
Ab 1985 wurden mehrere Patente auf Ibogaine zum Entzug von chemischen Substanzen zugelassen,[16] sowie in Bezug auf Kokain und Amphetamin,[17] Alkohol,[18] Nikotin[19] sowie Mehrfachabhängigkeiten.[20]
Schmerzmanagement
1957 beschrieb Jurg Schneider, Pharmakologe bei CIBA, dass Ibogain die analgetische Wirkung von Morphin potenziert.[21] Es fanden keine weiteren Forschungen dazu statt, bis fast 50 Jahre später Patrick Kroupa und Hattie Wells das erste Protokoll über eine begleitende Gabe von Ibogain mit Opiaten an Menschen veröffentlichte, welches nahelegt, dass Ibogain die Toleranz senke. Es sollte bemerkt werden, dass die Potenzierung der Wirkung von Ibogain eine sehr riskante Prozedur sein könne.[22]
Psychotherapie
Ibogain wurde als Begleitung für eine Psychotherapie durch Claudio Naranjo eingeführt und in seinem Buch The Healing Journey[15] veröffentlicht. Ihm wurde 1974 das Patent CA939266 zugesprochen.[23]
Pharmakologie
Ibogain soll einen relativ schnellen und schmerzfreien Entzug von Opiaten ermöglichen.[24] Neuere Untersuchungen deuten auf eine Erhöhung des Nervenwachstumfaktors GDNF (Glial Cell Line-Derived Neurotrophic Factor) im Gehirn hin. Im Tierversuch konnte nachgewiesen werden, dass an Alkohol gewöhnte Ratten bei erhöhtem GDNF-Pegel im Gehirn weniger Ethanol konsumierten und auch nach einer zweiwöchigen Abstinenzphase eine geringere Rückfallquote aufwiesen als eine unbehandelte Kontrollgruppe.[25]
Ibogain wird in der Leber zu Noribogain (12-Hydroxyibogamin)[26] metabolisiert, welches einem moderaten Depot-Effekt unterliegt. Man geht heute nicht davon aus, dass Noribogain die zentrale Rolle beim Abstinenz-Phänomen spielt.
Aufgrund von Nebenwirkungen und der toxikologischen Bedenken ist die Verwendung von Ibogain als Arzneimittel auch in Zukunft unwahrscheinlich. Bemühungen, verbesserte Wirkstoffe zu entwickeln und ferner den Wirkmechanismus des Abstinenz-Phänomens zu erklären, führten zu einer Reihe von synthetischen Ibogain-Derivaten, wobei das Derivat 18-Methoxycoronaridin in Tierversuchen deutlich geringere Nebenwirkungen als Ibogain zeigte. Pharmakologisch ist diesen Verbindungen gemein, dass sie den Nikotin-Rezeptor des Typs α3β4 hemmen.[27][28][29][30]
Durch die hemmende Einwirkung auf den hERG-Kanal[7] kommt es am Herzen zur QT-Verlängerung.[31]
Ibogain hemmt den Serotonintransporter, und zwar in nicht-kompetitiver und nicht-kovalenter Weise, und unterscheidet sich damit von allen bisher bekannten Inhibitoren plasmalemmaler Monoamintransporter.[32]
Rechtslage
In den USA ist Ibogain eine unter dem Controlled Substances Act regulierte Klasse-I-Substanz.[33]
Auch in Schweden ist Ibogain als Klasse-I-Substanz reguliert.[34]
In Norwegen fällt Ibogain unter die Anlage 10 der dortigen Vorschriften zum Umgang mit Narkotika und ist daher illegal.[35]
Weblinks
- Ibogain in der Suchttherapie, Vortrag von Sandra Karpetas (Iboga Therapy House, Kanada), gehalten auf dem Entheovision Kongress 2004
Einzelnachweise
- Chemical Structure and Properties auf ibogainedossier.com, abgerufen am 23. März 2015 (englisch).
- Datenblatt Ibogaine hydrochloride bei Sigma-Aldrich, abgerufen am 4. April 2011 (PDF).
- Eintrag zu Ibogaine in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- J. Dybowski, E. Landrin C. R. Acad. Sci. 1901, Vol. 133, S. 748 (Memento vom 25. Juli 2006 im Internet Archive). (pdf, engl.; 61 kB).
- G. Büchi: The Total Synthesis of Iboga Alkaloids. In: J. Am. Chem. Soc. 1966, Vol. 88 (13), S. 3099–3109. (pdf, engl.; 2,1 MB).
- C. Frauenfelder: Neuer Zugang zu den Iboga-Alkaloiden. Zürich 1999, S. 24, doi:10.3929/ethz-a-003839200 (Dissertation, ETH Zürich).
- Koenig X, Kovar M, Boehm S, Sandtner W, Hilber K: Anti-addiction drug ibogaine inhibits hERG channels: a cardiac arrhythmia risk. In: Addict Biol. 2012. doi:10.1111/j.1369-1600.2012.00447.x. PMID 22458604.
- Paling FP, Andrews LM, Valk GD, Blom HJ: Life-threatening complications of ibogaine: three case reports. In: Neth J Med. 70, Nr. 9, 2012, S. 422–4. PMID 23123541.
- Alper K, Reith ME, Sershen H: Ibogaine and the inhibition of acetylcholinesterase. In: J Ethnopharmacol. 139, Nr. 3, 2012, S. 879–82. doi:10.1016/j.jep.2011.12.006. PMID 22200647.
- Dosing. In: ibogainealliance.org. Global Ibogain Therapy Alliance, abgerufen am 21. Februar 2017 (englisch).
- K.R. Alper, H.S. Lotsof, G.M. Frenken, D.J. Luciano, J. Bastiaans 1999 234–42.
- Giannini, A. James: Drugs of Abuse, 2nd. Auflage, Practice Management Information Corporation, 1997, ISBN 1-57066-053-0.
- K.R. Alper, H.S. Lotsof, G.M. Frenken, D.J. Luciano, J. Bastiaans 1999 234–42.
- H.S. Lotsof (1995). Ibogaine in the Treatment of Chemical Dependence Disorders: Clinical Perspectives (Originally published in MAPS Bulletin (1995) V(3):19-26).
- Naranjo, Claudio: V, Ibogaine: Fantasy and Reality. In: The healing journey: new approaches to consciousness. Pantheon Books, New York 1973, ISBN 0-394-48826-1, S. 197–231. Archiviert vom Original am 4. Dezember 2008 (Abgerufen am 10. Oktober 2010).
- Rapid method for interrupting the narcotic addiction syndrome - US 4,499,096 (1985).
- Rapid method for interrupting the cocaine and amphetamine abuse syndrome" - US 4,587,243 (1986).
- Rapid method for attenuating the alcohol dependency syndrome" US 4,957,523 (1989).
- Rapid method for interrupting or attenuating the nicotine/tobacco dependency syndrome - US 5,026,697 (1991).
- Rapid method for interrupting or attenuating poly-drug dependency syndromes, US 5,124,994 (1992).
- Tabernanthine, Ibogaine Containing Analgesic Compositions - US 2817623 (Memento vom 19. März 2012 im Internet Archive).
- Kroupa, Patrick K. and Wells, Hattie: Ibogaine in the 21st Century. (PDF) In: Multidisciplinary Association for Psychedelic Studies (Hrsg.): maps. XV, Nr. 1, 2005, S. 21–25. Abgerufen am 23. Januar 2015.
- MEDICAMENT AGISSANT AU NIVEAU DU SYSTEME NERVEUX CENTRAL UTILISABLE DANS LES TRAITEMENTS PSYCHOTERAPIQUES ET COMME ANTI-DROGUE, CA939266.
- ibeginagain.org: Ibogain Therapie Fragen und Antworten (Memento vom 16. Januar 2012 im Internet Archive)
- Dao-Yao He, Nancy N. H. McGough, Ajay Ravindranathan, Jerome Jeanblanc, Marian L. Logrip, Khanhky Phamluong, Patricia H. Janak, Dorit Ron: Glial Cell Line-Derived Neurotrophic Factor Mediates the Desirable Actions of the Anti-Addiction Drug Ibogaine against Alcohol Consumption. In: Journal of Neuroscience. Band 25, Nr. 3, 2005, S. 619–628, doi:10.1523/JNEUROSCI.3959-04.2005, PMID 15659598.
- S.D. Glick: Ibogaine-like effects of noribogaine in rats. In: Brain Res.. 713(1–2), 1996, S. 294–7. PMID 8725004.
- Arias HR, Rosenberg A, Targowska-Duda KM, et al.: Interaction of ibogaine with human alpha3beta4-nicotinic acetylcholine receptors in different conformational states. In: Int. J. Biochem. Cell Biol.. 42, Nr. 9, 2010, S. 1525–35. PMID 20684041.
- O.D. Taraschenko: Is antagonism of alpha3beta4 nicotinic receptors a strategy to reduce morphine dependence?. In: Eur. J. Pharmacol.. 513(3), 2005, S. 207–18. PMID 15862802.
- C.J. Pace: Novel iboga alkaloid congeners block nicotinic receptors and reduce drug self-administration. In: Eur. J. Pharmacol.. 492(2–3), 2004, S. 159–67. PMID 15178360.
- I.M. Maisonneuve (2003). Anti-addictive actions of an iboga alkaloid congener: a novel mechanism for a novel treatment. Pharmacol. Biochem. Behav. 75(3), 607–18 (engl.).
- Hoelen DW, Spiering W, Valk GD: Long-QT syndrome induced by the antiaddiction drug ibogaine. In: N. Engl. J. Med.. 360, Nr. 3, 2009, S. 308–9. doi:10.1056/NEJMc0804248. PMID 19144953.
- Bulling S, Schicker K, Zhang YW, et al.: The mechanistic basis for noncompetitive ibogaine inhibition of serotonin and dopamine transporters. In: J. Biol. Chem.. 287, Nr. 22, 2012, S. 18524–34. doi:10.1074/jbc.M112.343681. PMID 22451652. PMC 3365767 (freier Volltext).
- Scheduling Actions Controlled Substances Regulated Chemicals.
- Läkemedelsverkets föreskrifter om förteckningar över narkotika; 1997:12 (Memento vom 16. September 2018 im Internet Archive).
- Forskrift om narkotika (narkotikaforskriften). In: lovdata.no. Abgerufen am 24. März 2015.
