Glucose-Oxidase
Glucose-Oxidase (GOD, auch Glukose-Oxidase) ist ein Enzym, das die sauerstoff-abhängige Oxidation am C1-Kohlenstoffatom des Zuckers Glucose katalysiert.
| Glucose-Oxidase (Penicillium amagasakiense) | ||
|---|---|---|
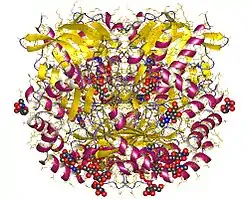 | ||
| Kalottenmodell des Glucose-Oxidase-Dimer aus Penicillium amagasakiense nach PDB 1GPE | ||
| Masse/Länge Primärstruktur | 587 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Homodimer | |
| Kofaktor | FAD | |
| Bezeichner | ||
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 1.1.3.4, Oxidoreduktase | |
| Reaktionsart | Redoxreaktion | |
| Substrat | β-D-Glucose + O2 | |
| Produkte | D-Glucono-1,5-lacton + H2O2 | |
Das dimere Flavoenzym setzt Glucose und Sauerstoff zu Gluconolacton und Wasserstoffperoxid um. Es kommt in Pilzen, wie dem Weißfäulepilz Phanerochaete chrysosporium und den Schimmelpilzen Aspergillus niger und Penicillium amagasakiense, vor, wurde aber auch bereits für Bombyx mori nachgewiesen.[1] Die Kristallstruktur des Enzyms aus diesen beiden Pilzen wurde mit Röntgenkristallographie bestimmt. Die Molekülmasse beträgt 120 kDa.
Nach Bindung der Glucose an das Enzym erfolgt der Elektronentransfer auf das am Enzym gebundene FAD, was zu FADH2 reduziert wird. Das Gluconolacton wird freigesetzt, es kann spontan oder enzymatisch zu Gluconsäure hydrolysiert werden. In einem zweiten Schritt wird molekularer Sauerstoff an das Isoalloxazin-Ringsystem des FAD addiert und das Hydroperoxid dann als Wasserstoffperoxid freigesetzt. Molekularer Sauerstoff ist der natürliche Elektronenakzeptor, das Enzym kann aber mit einer Reihe künstlicher Akzeptoren arbeiten.
Das Enzym hat große Bedeutung in der Bestimmung von Glucose mit dem GOD-Test. Es wird auch häufiger als Modellenzym für elektronische Mini-Enzymbiosensoren verwendet, dabei wird das Enzym auf eine Metallfläche aufgebracht und kann die Elektronen der von ihm katalysierten Redoxreaktion weiterleiten.
Vorkommen
Glucose-Oxidase kommt u. a. natürlich im Honig vor. Dabei ist es Bestandteil körpereigener Sekrete, die die Bienen schon beim Transport von der Blüte zum Stock dem Nektar zufügen. Der durch die Glucose-Oxidase katalysierte Übertragung von Elektronen auf molekularen Sauerstoff, wodurch keimtötendes oder keimhemmendes Wasserstoffperoxid gebildet wird, wird eine große Bedeutung bei der Konservierung des Honigs im Bienenstock beigemessen.[2]
Quellen
- BRENDA – the comprehensive enzyme information system
- Helmut Horn und Cord Lüllmann: „Das große Honigbuch – Entstehung, Gewinnung, Gesundheit und Vermarktung“, Franckh-Kosmos Stuttgart, 3. Auflage 2002, ISBN 978-3-440-10838-3.
Weblinks
- Jennifer McDowall/Interpro: Protein Of The Month: Glucose Oxidase and Biosensors. (engl.)