Gallium(III)-sulfid
Gallium(III)-sulfid ist eine anorganische chemische Verbindung des Galliums aus der Gruppe der Sulfide.
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
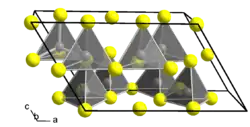 | |||||||||||||||||||
| _ Ga3+ _ S2− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Gallium(III)-sulfid | ||||||||||||||||||
| Andere Namen |
Digalliumtrisulfid | ||||||||||||||||||
| Verhältnisformel | Ga2S3 | ||||||||||||||||||
| Kurzbeschreibung |
geruchloser weißer bis gelber Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 235,63 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Gallium(III)-sulfid kann durch Reaktion von Gallium mit Schwefel bei 1250 °C gewonnen werden.[2]
Ebenfalls möglich ist die Darstellung durch Reaktion von Gallium(III)-oxid oder Gallium(III)-hydroxid mit Schwefelwasserstoff.[2]
Eigenschaften
Gallium(III)-sulfid ist ein weißer bis gelber[2] geruchloser Feststoff, der mit Wasser reagiert.[1] Er löst sich in wässrigen Säuren und hydrolysiert an Luft langsam mit Schwefelwasserstoff-Entwicklung.[3]
Die Verbindung tritt in zwei Formen auf. Die Niedertemperaturform α-Ga2S3 hat eine Zinkblendestruktur während die Hochtemperaturmodifikation β-Ga2S3 eine Wurtzitstruktur bildet. Die Umwandlungstemperatur zwischen den beiden Formen liegt zwischen 550 und 600 °C. Durch mehrere Tage Tempern bei 1000 °C entsteht schließlich als stabile Modifikation eine monokline Überstruktur des Wurtzit-Typs (Raumgruppe Cc (Raumgruppen-Nr. 9), Gitterparameter a = 11,11 Å, b = 6,395 Å, c = 7,021 Å, β = 121,2°) mit geordneter Verteilung der Metallatome.[2][4][5]
Verwendung
Galliumsulfid wird in CIGS-Photovoltaikmodulen als Halbleiter verwendet.[6]
Einzelnachweise
- Datenblatt Gallium(III) sulfide, 99.999% (metals basis) bei AlfaAesar, abgerufen am 27. Februar 2014 (PDF) (JavaScript erforderlich).
- Georg Brauer, unter Mitarbeit von Marianne Baudler u. a. (Hrsg.): Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I. Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 857.
- A.J. Downs: Chemistry of Aluminium, Gallium, Indium, and Thallium. Springer, 1993, ISBN 0-7514-0103-X, S. 162 (eingeschränkte Vorschau in der Google-Buchsuche).
- J. Goodyear, W. J. Duffin, G. A. Steigmann: The unit cell of α-Ga2S3. In: Acta Crystallographica. 14, S. 1168–1170, doi:10.1107/S0365110X61003399.
- C.Y. Jones, J.C. Bryan, K. Kirschbaum, J.G.Edwards: Refinement of the crystal structure of digallium trisulfide, Ga2S3. In: Zeitschrift für Kristallographie – New Crystal Structures, 216, 2001, S. 327–328, doi:10.1524/ncrs.2001.216.14.349.
- Copper Indium Gallium Diselenide Website des Office of Energy Efficiency & Renewable Energy, US Department of Energy. Abgerufen am 23. März 2016
