Freie Leichtketten
Als Freie Leichtketten (FLC, von engl. Free Light Chain) werden die ungebundenen leichten Ketten bezeichnet. Leichte Ketten bilden zusammen mit den schweren Ketten intakte Immunglobuline (Antikörper).
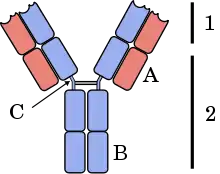
Immunglobuline werden von Plasmazellen (Teil des Immunsystems) gebildet, die sich aus Hämatopoetischen Stammzellen im Knochenmark (B-Lymphozyten) entwickeln. Sie bestehen aus zwei identischen schweren Ketten und zwei identischen leichten Ketten, wobei es fünf verschiedene Isotypen (Klassen) an schweren Ketten (G, A, M, D und E) gibt. Von den leichten Ketten gibt es zwei Isotypen, welche als Kappa (κ) bzw. Lambda (λ) bezeichnet werden (siehe auch: Struktur von Antikörpern). Leichtketten werden bei jedem Menschen im Überschuss gebildet und von den Zellen als freie Leichtketten ins Blut abgegeben. Die natürliche Funktion der freien Leichtketten ist bisher weitestgehend ungeklärt und Bestandteil aktueller Forschung.[1][2][3]
Vorkommen
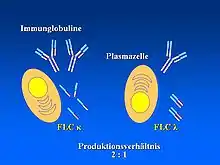
Bei jedem Menschen liegen geringe Mengen an freien leichten Ketten, zusätzlich zu den in den Immunglobulinen gebundenen leichten Ketten, im Blut vor (Normalwerte: κ = 3,30-19,40 mg/l, λ = 5,71-26,30 mg/l).[4] Die freie Leichtkette κ liegt dabei als Monomer (ein einzelnes Molekül, ca. 25 Kilodalton, kDa) vor, während die freie Leichtkette λ vorwiegend ein Dimer (besteht aus zwei miteinander verbundenen Molekülen, ca. 50 kDa) bildet.[5] Das Produktionsverhältnis von der freien Leichtkette κ zu λ beträgt 2:1. Der Stoffwechsel des Körpers bewirkt eine Umkehr dieses Verhältnisses (siehe nächster Abschnitt).
Stoffwechsel
Die freien Leichtketten werden aufgrund ihrer geringen Größe von der Niere gefiltert. Die zwei Nieren des Menschen bestehen jeweils aus etwa einer Million Nephrons, wobei das Nephron die Filtrationseinheit der Niere ist. Da die freie Leichtkette κ im Gegensatz zur dimeren freien Leichtkette λ als Monomer vorliegt, wird sie etwa dreimal schneller von der Niere filtriert und damit zügiger aus dem Blut entfernt.[5] Daher liegen im Blut mehr freie Leichtketten λ als κ vor und somit entspricht das Verhältnis der Konzentrationen im Blut nicht dem κ:λ Produktionsverhältnis von 2:1, sondern kehrt sich um zu etwa 1:2 (die κ/λ-Ratio liegt im Mittel bei 0,63; der normale Bereich liegt im Serum zwischen 0,26 und 1,65).[4]

Aufgrund dieser Filtration haben die freien Leichtketten eine sehr kurze Verweildauer im Blut. Ihre Halbwertszeit beträgt 2-6 Stunden, wobei die freie Leichtkette κ eine Halbwertszeit von 2 bis 3 und die freie Leichtkette λ von 4 bis 6 Stunden hat. Zum Vergleich: Das intakte Immunglobulin IgG, das von der Niere nicht filtriert wird, da es mit einer Masse von 150.000 Dalton zu groß für die Poren ist, hat eine Halbwertszeit von bis zu 20 Tagen.
Nachdem die freien Leichtketten durch die Glomeruli filtriert wurden, gelangen sie in den proximalen Tubulus der Niere, wo sie über die proximalen Tubuluszellen reabsorbiert und metabolisiert werden. Der Organismus sorgt so dafür, dass keine größeren Mengen an Eiweißen (Proteinen) in den Urin verloren gehen.
Beim gesunden Menschen werden etwa 500 mg freie Leichtketten am Tag produziert, die vollständig von der Niere filtriert und reabsorbiert werden.[6][7] Eine intakte Niere kann pro Tag eine Menge von 10 bis 30 g Eiweiß reabsorbieren. Daher gelangen beim gesunden Menschen nur verschwindend geringe oder überhaupt keine Mengen an freien Leichtketten in den Urin.[8][9][10] Demzufolge muss die Konzentration freier Leichtketten im Blut erst sehr stark ansteigen (wie es bei Monoklonalen Gammopathien der Fall sein kann), bevor die Reabsorptionskapazität der Niere überschritten wird und die freien Leichtketten auch in den Urin ausgeschieden werden (Überlaufproteinurie, Proteinurie).[11][12][13]
Klinische Bedeutung
Bei Monoklonalen Gammopathien liegen krankhaft veränderte Plasmazellen vor, die sich unkontrolliert vermehren. Diese Plasmazellen sind monoklonal und somit identisch, da sie alle von derselben Zelle abstammen. Zu den Monoklonalen Gammopathien zählen das Multiple Myelom, das Plasmozytom, Morbus Waldenström, die AL-Amyloidose, die Leichtketten-Speicherkrankheit (Light Chain Deposition Disease), die Monoklonale Gammopathie unklarer Signifikanz (MGUS), die Monoklonale Gammopathie renaler Signifikanz (MGRS) und andere ähnliche Erkrankungen. Bei den meisten Monoklonalen Gammopathien werden in großen Mengen monoklonale Proteine produziert. Diese können monoklonale Immunglobuline und/oder monoklonale freie Leichtketten sein, die in das Blut freigesetzt werden. Die monoklonalen freien Leichtketten werden zum Beispiel beim Leichtketten Myelom als alleiniges Tumorprodukt gebildet, kommen insgesamt aber auch bei der Mehrheit aller Myelom-Formen (85-95 %) zumindest als zusätzliches Tumorprodukt vor. Nur in 5-10 % der Fälle sind ausschließlich intakte Immunglobuline ohne freie Leichtketten als Tumorprodukt nachweisbar.[14][15][16][17]
Die freien Leichtketten können bei den genannten Erkrankungen als Tumormarker verwendet werden. Ihre Bestimmung im Serum ist von Bedeutung bei der Diagnose, der Einschätzung des Risikos einer Progression der Erkrankung, der Kontrolle des Therapieerfolgs und eines Rezidivs bzw. Relapse der Erkrankung. Hierbei gibt das κ/λ-Verhältnis (κ/λ-Ratio) Auskunft über die Klonalität der vorliegenden Erkrankung.[18][19][20][21]
Weiterhin sind die freien Leichtketten ein geeigneter Parameter für die Verlaufs- und Therapiekontrolle aller Monoklonaler Gammopathien mit Beteiligung freier Leichtketten, da aufgrund ihrer kurzen Halbwertszeit von wenigen Stunden eine zeitnahe Beurteilung des Krankheitsverlaufs möglich ist. Änderungen der Tumormasse und -aktivität spiegeln sich daher sehr schnell in der Konzentration freier Leichtketten wider.
Die Änderung der Konzentration freier Leichtketten hat auch eine prognostische Bedeutung bezüglich des Krankheitsverlaufs beim Multiplen Myelom und der AL-Amyloidose. Außerdem stellt das κ/λ-Verhältnis ein Kriterium für die Risikobeurteilung von Monoklonalen Gammopathien unklarer Signifikanz dar. Sind hier abnormale Werte zu beobachten, kann dies ein Hinweis für einen bevorstehenden oder (im Vergleich zu Patienten mit normalen Werten) früheren Progress der Erkrankung sein.[19][20][22]
Analytische Bestimmung
Die Bestimmung der freien Leichtketten durch Immunassays anhand von Serumproben gilt seit annähernd 20 Jahren als die Methode der Wahl, wodurch Urin, ein bis dahin häufiger genutztes Probenmaterial, mehrheitlich abgelöst wurde.[5][23] Ein wichtiger analytischer Vorteil der Immunassays gegenüber elektrophoretischer Methoden (z. B. der Serumeiweißelektrophorese und der Immunfixationselektrophorese) und der Bestimmung der Gesamt-Leichtketten, liegt in der deutlich höheren Sensitivität und in der hohen Spezifität des Tests. Daher lässt sich die Diagnose, Therapie- und Verlaufskontrolle vieler Monoklonaler Gammopathien durch die Bestimmung der freien Leichtketten im Serum deutlich verbessern. Diese Methode hat inzwischen auch Eingang in die nationalen und internationalen Leitlinien zur Diagnose und Verlaufskontrolle von Monoklonalen Gammopathien gefunden.[18][21][24][25] Die hämatologischen Leitlinien beziehen sich zur Bestimmung freier Leichtketten auf den sogenannten Freelite-Test.[18][26] Messergebnisse, die anhand Tests verschiedener Hersteller ermittelt werden, sind nicht vergleichbar. Die unterschiedliche Zusammensetzung sowie die z. T. analytischen Unterschiede der Tests äußern sich in Differenzen im direkten Vergleich der Messergebnisse, insbesondere von pathologischen Proben.
Literatur
- M. A. Bärtsch Aktuelle Aspekte bei der Diagnostik und Therapie des Plasmazellmyeloms In: Deutsches Ärzteblatt 2017, 142(11), S. 800–804.
- D. Felsenberg Monoklonale Gammopathie unklarer Signifikanz (MGUS) In: Forum Sanitas 2018, 2. Ausgabe, S. 39–41.
- K. M. Kortüm Das multiple Myelom In: Der Internist 2013, 54(8), S. 963–977.
- Hartmut Goldschmidt: Das Multiple Myelom (Plasmozytom). Diagnose und Therapie. 2. Auflage. Unimed, Bremen 2011, ISBN 978-3-8374-1032-7.
Weblinks
- AMM-Online, Netzwerk für Myelom-Patienten, Informationsportal mit Patientenforum
- Offizielle Seite der International Myeloma Working Group (englischsprachig)
- Plasmozytom / Multiples Myelom. Antworten. Hilfen. Perspektiven. (PDF; 1,17 MB) Blauer Ratgeber #22 der Deutschen Krebshilfe
- Wikilite - Informationsseite (englischsprachig) über die Bestimmung der Freien Leichtketten
Einzelnachweise
- T. Nakano et al.: Free immunoglobulin light chain: its biology and implications in diseases. In: Clin Chim Acta. 421, Nr. 11-12, 5. März 2011, S. 843–9. doi:10.1016/j.cca.2011.03.007. PMID 21396928.
- F. A. Redegeld et al.: Polyclonal immunoglobulin free light chain and chronic inflammation. In: Mayo Clin Proc. 87, Nr. 10, 6. Oktober 2012, S. 1032-3. doi:10.1016/j.mayocp.2012.07.012. PMID 23036675.
- U. Basile et al.: Plasmatic free light chains as inflammatory marker in insulin resistance: comparison of metabolic syndrome with adult growth hormone deficiency. In: Biofactors. 44, Nr. 5, 2018, S. 480-484. doi:10.1002/biof.1444. PMID 30175865.
- J. A. Katzmann et al.: Serum reference intervals and diagnostic ranges for free kappa and free lambda immunoglobulin light chains: relative sensitivity for detection of monoclonal light chains. In: Clinical Chemistry. 48, Nr. 9, 2. Mai 2002, S. 1437-1444. PMID 12194920.
- A. R. Bradwell et al.: Highly sensitive, automated immunoassay for immunoglobulin free light chains in serum and urine. In: Clinical Chemistry. 47, Nr. 4, 29. März 2001, S. 673-680. PMID 11274017.
- A. Solomon et al.: Light chains of human immunoglobulins.. In: Methods Enzymol. 116, 2018, S. 101-121. doi:10.1016/S0076-6879(85)16008-8. PMID 3937021.
- T. A. Waldmann et al.: The renal handling of low molecular weight proteins: II. Disorders of serum protein catabolism in patients with tubular proteinuria, the nephrotic syndrome, or uremia. In: J Clin Invest. 51, Nr. 8, 1. August 1972, S. 2162–74. doi:10.1172/JCI107023. PMID 5054468. PMC 292373 (freier Volltext).
- G. N. Abraham et al.: The role of the kidney in the catabolism of Bence Jones Proteins and immunoglobulin fragments. In: The American Journal of the Medical Sciences. 268, Nr. 4, Oktober 1974, S. 227–33. doi:10.1097/00000441-197410000-00003. PMID 4217565.
- R. D. Wochner et al.: Evidence for defective immunoglobulin metabolism in severe renal insufficiency. In: J Exp Med. 126, Nr. 2, August 1967, S. 207–21. doi:10.1084/jem.126.2.207. PMID 4165739. PMC 2138312 (freier Volltext).
- T. Maack et al.: Renal filtration, transport, and metabolism of low-molecular-weight proteins: a review. In: Kidney Int. 16, Nr. 3, September 1979, S. 2251–70. doi:10.1038/ki.1979.128. PMID 393891.
- A. R. Bradwell et al.: Serum test for assessment of patients with Bence Jones myeloma. In: Lancet. 361, Nr. 9356, Februar 2003, S. 489–91. doi:10.1016/S0140-6736(03)12457-9. PMID 4165739.
- M. A. Alyanakian et al.: Free immunoglobulin light-chain serum levels in the follow-up of patients with monoclonal gammopathies: correlation with 24-hr urinary light-chain excretion. In: Am J Hematol. 75, Nr. 4, April 2004, S. 246–8. doi:10.1002/ajh.20007. PMID 15054820.
- M. R. Nowrousian et al.: Serum free light chain analysis and urine immunofixation electrophoresis in patients with multiple myeloma. In: Clin Cancer Res. 71, Nr. 24, Dezember 2005, S. 8706–14. doi:10.1158/1078-0432.CCR-05-0486. PMID 16361557.
- G. P. Mead et al.: Serum free light chains for monitoring multiple myeloma. In: Br J Hematol. 126, Nr. 3, 2004, S. 348-354. doi:10.1111/j.1365-2141.2004.05045.x. PMID 15257706.
- R. A. Kyle et al.: Review of 1027 patients with newly diagnosed multiple myeloma. In: Mayo Clin Proc. 78, Nr. 1, 2003, S. 21-33. doi:10.4065/78.1.21. PMID 12528874.
- M. Drayson et al.: Effects of paraprotein heavy and light chain types and free light chain load on survival in myeloma: an analysis of patients receiving conventional-dose chemotherapy in Medical Research Council UK multiple myeloma trials. In: Blood. 108, Nr. 6, 2006, S. 2013-9. doi:10.1182/blood-2006-03-008953. PMID 16728700.
- A. Dispenzieri et al.: Effects Prevalence and risk of progression of light-chain monoclonal gammopathy of undetermined significance: a retrospective population-based cohort study. In: Lancet. 375, Nr. 9729, 15. Mai 2010, S. 1721-8. doi:10.1016/S0140-6736(10)60482-5. PMID 20472173. PMC 2904571 (freier Volltext).
- S. V. Rajkumar et al.: International Myeloma Working Group updated criteria for the diagnosis of multiple myeloma. In: Lancet Oncology. 15, November 2014, S. e538–e548. doi:10.1038/leu.2010.60. PMID 20410922.
- S. V. Rajkumar et al.: Serum free light chain ratio is an independent risk factor for progression in monoclonal gammopathy of undetermined significance. In: Blood. 106, Nr. 3, August 2005, S. 812–7. doi:10.1182/blood-2005-03-1038. PMID 15855274. PMC 1895159 (freier Volltext).
- A. Dispenzieri et al.: Immunoglobulin free light chain ratio is an independent risk factor for progression of smoldering (asymptomatic) multiple myeloma. In: Blood. 111, Nr. 2, 17. Oktober 2007, S. 785-789. doi:10.1182/blood-2007-08-108357. PMID 17942755. PMC 2200851 (freier Volltext).
- A. Durie et al.: International uniform response criteria for multiple myeloma. In: Leukemia. 20, Nr. 9, 21. Juli 2006, S. 1467-73. doi:10.1038/sj.leu.2404284. PMID 16855634.
- R. A. Kyle et al.: Monoclonal gammopathy of undetermined significance (MGUS) and smoldering (asymptomatic) multiple myeloma: IMWG consensus perspectives risk factors for progression and guidelines for monitoring and management. In: Leukemia. 24, Nr. 6, 22. April 2010, S. 1121-7. doi:10.1038/leu.2010.60. PMID 20410922.
- A. R. Bradwell et al.: Serum free light chain immunoassays for monitoring patients with light chain producing and nonsecretory multiple myeloma. In: ASH Meeting Philadelphia. 2002.
- A. Dispenzieri et al.: International Myeloma Working Group guidelines for serum-free light chain analysis in multiple myeloma and related disorders. In: Leukemia. 23, Nr. 2, Februar 2009, S. 215-224. doi:10.1038/leu.2008.307. PMID 19020545.
- Onkopedia - Leilinien der DGHO Abgerufen am 4. Dezember 2018.
- M. A. Bätsch et al.: Aktuelle Aspekte bei der Diagnostik und Therapie des Plasmazellmyeloms. In: Deutsches Ärzteblatt. 142, Nr. 11, 1. Juni 2017, S. 800–804. doi:10.1055/s-0043-100295. PMID 28564730.