Forster-Diazoketon-Synthese
Die Forster-Diazoketon-Synthese ist eine Reaktion aus dem Bereich der Organischen Chemie. Sie wurde 1915 von Martin Onslow Forster entdeckt und nach ihm benannt. Die Reaktion dient der Synthese von Diazoketonen. Diese können dargestellt werden, indem α-Ketooxime mit Chloramin umgesetzt werden.[1][2]
Übersichtsreaktion
Ursprünglich wurde diese Methode zur Herstellung von 3-Diazoampher entwickelt. Später stellte man jedoch fest, dass mit dieser Reaktion allgemein auf die Synthese von α-Diazoketonen anwendbar ist, welche durch die bisher bekannten Verfahren wie beispielsweise die Bamford-Stevens-Reaktion nicht zugänglich sind.[3] Sie wird hauptsächlich zur Herstellung cyclischer Diazoketone verwendet.
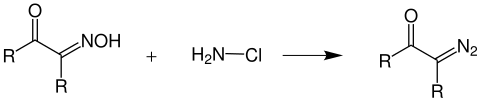
Ein α-Oximoketon (links) reagiert mit Chloramin zu einem α-Diazoketon (rechts).
Reaktionsmechanismus
Es sind zwei verschiedene Reaktionsmechanismen möglich. So wäre ein nukleophiler Angriff des Chloramins an das Stickstoffatom des Oxims denkbar. Diese Variante würde der Carbonylfunktion des Eduktes eine große Rolle zusprechen. Meinwald und Mitarbeiter zeigten 1959 jedoch, dass die Ketogruppe des Eduktes keine Rolle für die Umsetzung eines α-Ketooxims zu einem α-Diazoketons spielt. Daher wurde der folgende Reaktionsmechanismus bevorzugt:[3]
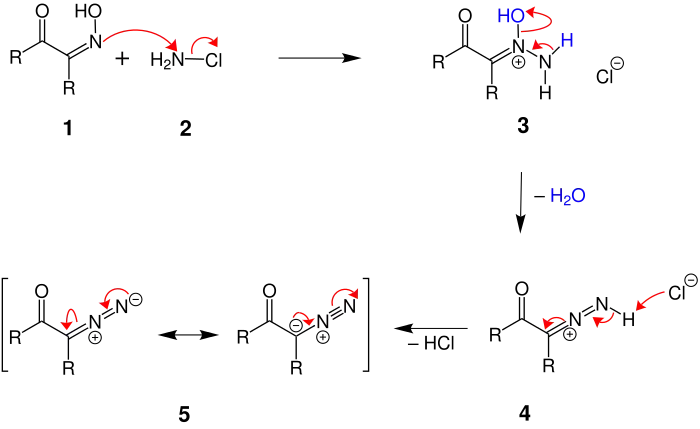
Zunächst findet eine nukleophile Substitution des Stickstoffatoms des Oximoketons 1 am Stickstoffatom des Chloramins 2 statt. Das Chlorid-Ion wird abgespalten und es entsteht 3. Im nächsten Schritt erfolgt eine Wasserabspaltung unter Ausbildung einer Stickstoff-Stickstoff-Doppelbindung, sodass 4 entsteht. Im dritten und damit letzten Reaktionsschritt wird ein Wasserstoffatom abgespalten, wodurch sich eine Dreifachbindung zwischen den Stickstoffatomen ausbilden kann. Es entsteht ein α-Diazoketon 5, welches – wie in der Abbildung dargestellt – mesomere Grenzstrukturen besitzt.[1]
Siehe auch
Einzelnachweise
- Z. Wang (Hrsg.): Comprehensive Organic Name Reactions and Reagents (3 Volume Set). John Wiley & Sons, Hoboken, New Jersey 2009, ISBN 978-0-471-70450-8, S. 1111.
- Martin Onslow Forster: XXIX-Azotisation by chloroamine. In: Journal of the Chemical Society, Transactions. 107, 1915, S. 260, doi:10.1039/CT9150700260.
- Wolfgang Uhl, Apostolos Kyriatsoulis: Namen- und Schlagwortreaktionen in der Organischen Chemie. Vieweg, Braunschweig 1984, ISBN 978-3-528-03581-5, S. 60/61.