Fluoreszenzdiagnostik
Die Fluoreszenzdiagnostik (FD) oder Photodynamische Diagnostik (PDD) ist ein Verfahren zur In-vivo-Diagnostik von epithelialen Tumoren und Präkanzerosen.
Verfahren
Wie bei der Photodynamischen Therapie (PDT) wird ein Photosensibilisator (englisch photosensitizer)[1] oder ein Vorläufer eines Photosensibilisators (Prodrug) appliziert, der sich selektiv in oder an Tumorzellen anreichert. Durch die Bestrahlung mit Licht werden die Sensibilisatormoleküle zum Fluoreszieren gebracht. Dieses Fluoreszenzlicht kann durch das freie Auge oder besser durch ein optisches System detektiert und der Tumor somit lokalisiert werden. Präkanzeröse oder kanzeröse Veränderungen zeigen durch die selektive Anreicherung des Fluorophors im Gegensatz zu den gutartigen Veränderungen eine signifikant höhere Fluoreszenz.[2]
Etabliert ist die Fluoreszenzdiagnostik bisher vor allem in der Dermatologie und Urologie.[3][4] In der Dermatologie eignet sich dieses Verfahren zur Diagnostik von nicht-melanozytären Tumoren wie Basalzellkarzinomen[5] oder Spinaliomen, aber auch von Präkanzerosen wie der Aktinischen Keratose. In der Urologie wird die Fluoreszenzdiagnostik von der European Association of Urology (EAU) in ihren Richtlinien zur Diagnose und Behandlung des urothelialen Carcinoma in situ empfohlen.[6] Vielversprechende Ansätze gibt es auch bei Diagnostik von Tumoren im Mund- und Rachenbereich,[7] im Ösophagus-, Magen- und Darmbereich[8] und in der Gynäkologie bei der Frühdiagnostik des Zervixkarzinoms.
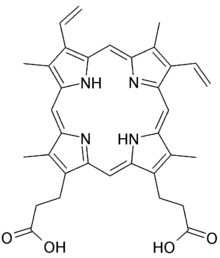
Wegen seiner hohen Selektivität und guten Verträglichkeit wird in der Dermatologie zur FD nahezu ausschließlich Protoporphyrin IX (PpIX) als Sensibilisator verwendet. PpIX entsteht nach topischer Gabe von 5-Aminolävulinsäure (5-ALA) als freie Säure oder in Form ihres Methylesters Methyl-5-amino-4-oxopentanoat (MAOP) im Rahmen der Häm-Biosynthese. Da die erzeugten Porphyrine körpereigene Substanzen sind, sind außer der Sensibilisierung der Haut gegenüber Licht keine Nebenwirkungen bekannt. Die höchste selektive Anreicherung von PpIX in Tumoren wird etwa 2 bis 3 Stunden nach topischer Applikation von MAOP erreicht.[9]
Zur Anregung der Fluoreszenz wird aufgrund des Absorptionspektrums von Porphyrinen Licht der Wellenlänge von 400 bis 500 nm verwendet (Absorptionsmaximum bei ca. 405 nm)[10] und die emittierte Fluoreszenz liegt zwischen 600 und 750 nm (Emissionsmaximum bei ca. 630 nm).
Die Detektion des emittierten Fluoreszenzlichts ist zwar ohne größere technische Hilfsmittel möglich, jedoch mit einigen Nachteilen verbunden. So kann die Eigenfluoreszenz der Haut (Autofluoreszenz) zu einer falschen Beurteilung der Fluoreszenzintensitäten führen. Ein weiterer Nachteil ist die nötige Abdunkelung des Raumes während der Diagnostik. Wesentliche Vorteile bietet demgegenüber die Verwendung eines CCD (charge-coupled device) basierten Kamerasystems. Hierbei können die Fluoreszenzbilder digital nachbearbeitet und archiviert werden, und mit Hilfe geeigneter Emissionsfilter kann die Eigenfluoreszenz herausgefiltert werden.
Die Detektionstiefe, also diejenige Tiefe, bis zu der Tumorzellen noch entdeckt werden können, ist grundsätzlich limitiert durch die Penetrationstiefe des Farbstoffes und die Eindringtiefe des Anregungslichts.[11] Die Fluoreszenz der ALA- oder MAOP-induzierten Porphyrine bleibt weitgehend auf die Epidermis beschränkt.
Vorteile der FD gegenüber anderen Verfahren sind die frühe Diagnostik, die auch an schwer zugänglichen Stellen und in vernarbtem oder entzündetem Gewebe möglich ist, und die Diagnostik ohne Entnahme von Gewebeproben.
Literatur
- Dieter Jocham, Michael Landthaler, Rolf-Markus Szeimies: Klinische Fluoreszenzdiagnostik und Photodynamische Therapie. 2. Auflage. Thieme, Stuttgart 2004, ISBN 978-3-13-137832-3
- Burkhard M. Lippert, S. Schmidt: Fluoreszenzdiagnostik und Photodynamische Therapie. Shaker Verlag, 2000, ISBN 978-3-8265-7393-4
Einzelnachweise
- Ron R Allison, et al.: Photosensitizers in clinical PDT. (PDF) In: Elsevier (Hrsg.): Photodiagnosis and Photodynamic Therapy. 1, 2004, S. 27–42. doi:10.1016/S1572-1000(04)00007-9.
- Clemens Fritsch, Thomas Ruzicka: Fluorescence Diagnosis and Photodynamic Therapy of Skin Diseases: Handbook and Atlas. 1. Auflage. Springer, Wien 2003, S. 23 ff.: E – Fluorescence Detektion of ALA-induced Porphyrins (FDAP)
- C. R. Riedl: Fluoreszenzdiagnostik beim Harnblasenkarzinom (PDF; 260 kB) In: Journal für Urologie und Urogynäkologie, Sonderheft 6(2003), S. 25
- Dieter Jocham, Herbert Stepp, Raphaela Waidelich: Photodynamic Diagnosis in Urology: State-of-the-Art (PDF) In: European Urology 53 (2008) 1138–1150
- Daniela Steinat: Bewertung der Photodynamischen Diagnostik mit 5-Aminolävulinsäure beim Basalzellkarzinom durch 3D-Histologie. Dissertation, 2004, urn:nbn:de:bsz:21-opus-15597.
- M. Babjuk, W. Oosterlinck, R. Sylvester, E. Kaasinen, A. Böhle, J. Palou, M. Rouprêt: Guidelines on TaT1 (Non-muscle invasive) Bladder Cancer. (Memento des Originals vom 22. März 2011 im Internet Archive; PDF; 136 kB) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. European Association of Urology 2010, S. 6: 5.9 Fluorescence cystoscopy
- P.Schleier et al.: Möglichkeiten und Grenzen der Fluoreszenzdiagnostik und photodynamischen Therapie des Mundhöhlenkarzinoms. In: Deutsche Zahnärztliche Zeitschrift. 59, 2004, 5, S. 276–283; zahnheilkunde.de (PDF)
- Arbeitsgruppe 8.31: Gewebeoptik und molekulare Bildgebung - Lasergestützte Fluoreszenzdiagnostik Physikalisch-Technische Bundesanstalt (PTB) (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis.
- H. Weisser, D. Meyer-Rogge, E. Meyer-Rogge: Erste Erfahrungen im niedergelassenen Bereich mit neuem topischen Photosensibilisator MAOP bei aktinischen Keratosen und Basaliomen. In: Akt Dermatol., Band 30, 2004, S. 306–311.
- Clemens Fritsch, Thomas Ruzicka: Fluorescence Diagnosis and Photodynamic Therapy of Skin Diseases: Handbook and Atlas. 1. Auflage. Springer, Wien 2003, ISBN 3-211-83827-9, S. 19 (C – Light Used in FDAP and PDT, Fig. 24: Absorption spectrum of phorphyrin molecules).
- Daniela Steinat: Bewertung der Photodynamischen Diagnostik mit 5-Aminolävulinsäure beim Basalzellkarzinom durch 3D-Histologie. Dissertation 2004, S. 10 (Abb. 3: Schema der Reichweite des Lichtes durch die Haut), urn:nbn:de:bsz:21-opus-15597.