Dritter Hauptsatz der Thermodynamik
Der dritte Hauptsatz der Thermodynamik, auch Nernstsches Theorem bzw. Nernst-Theorem oder Nernstscher Wärmesatz nach dem deutschen Physiker Walther Nernst, sagt aus, dass die Entropie eines geschlossenen Systems für T → 0 gegen eine von thermodynamischen Parametern unabhängige Konstante geht. Daraus folgt, dass der absolute Nullpunkt der Temperatur nicht durch eine endliche Anzahl von Zustandsänderungen erreichbar ist.
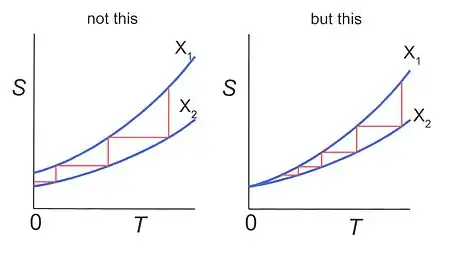
Der Satz kann unter Zuhilfenahme der Quantenmechanik bewiesen werden (s. u.).
Formulierung
Das Theorem wurde 1905 von Nernst aufgestellt und behandelt die Änderung der Entropie einer chemischen Reaktion bei einer Temperatur von null Kelvin: sie geht gegen null.
Die Formulierung wurde 1911 von Max Planck schärfer gefasst. Danach wird die Entropie unabhängig von thermodynamischen Parametern und somit konstant, wenn die Temperatur gegen null geht:
- ,
wobei die Boltzmann-Konstante ist und die Entartung des Grundzustandes.
Ist der Grundzustand des Systems nicht entartet, so gilt und damit . Somit verschwindet die Entropie eines Systems, wenn die Temperatur gegen null geht.
Beweis für kanonische Verteilung
Zuerst wird der statistische Operator durch seine Darstellung in der kanonischen Verteilung ersetzt. ist hierbei die empirische Temperatur.
Wertet man die Spur über die Operatoren aus, erhält man:
Nun wird die Energie des Grundzustandes von jedem Niveau abgezogen.
Es gilt nun für (entspricht ):
Setzt man diese Erkenntnis in die obige Doppelsummendarstellung ein, erhält man die gesuchte Formulierung des Nernst-Theorems nach Planck:
- ,
wobei die Entartung des Grundzustands angibt, also die Zahl der , die gleich sind.