Dinickelorthosilicat
Dinickelorthosilicat ist eine anorganische chemische Verbindung des Nickels aus der Gruppe der Silicate. Es ist das einzige stabile Silikat des Nickels.[4]
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
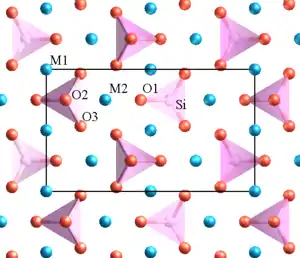 | ||||||||||||||||
| M1, M2: Ni2+ | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Dinickelorthosilicat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | Ni2SiO4 | |||||||||||||||
| Kurzbeschreibung |
grüner Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 209,46 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||
| Dichte |
5,8 g·cm−3[3] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
praktisch löslich in Wasser und wenig löslich in Salzsäure[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Vorkommen
Dinickelorthosilicat kommt natürlich in Form des Minerals Liebenbergit vor.
Gewinnung und Darstellung
Dinickelorthosilicat kann durch Reaktion von Nickel mit Siliciumdioxid und Sauerstoff gewonnen werden.[5]
Es kann auch durch Reaktion von Natriumsilicat mit Nickel(II)-nitrat dargestellt werden.[6]
Eigenschaften
Dinickelorthosilicat ist ein grauer bis grüner[7] Feststoff, der praktisch unlöslich in Wasser ist.[1] Er besitzt eine orthorhombische Kristallstruktur vom Olivintyp mit der Raumgruppe Pbnm (Raumgruppen-Nr. 62, Stellung 3). Bei höheren Temperaturen und Drücken wandelt sich diese in eine kubische Spinellstruktur mit der Raumgruppe Fd3m (Raumgruppen-Nr. 227) um.[8][4][3][9]
Einzelnachweise
- F. Singer: Industrial Ceramics. Springer, 2013, ISBN 978-94-017-5257-2, S. 174 (eingeschränkte Vorschau in der Google-Buchsuche).
- Eintrag zu Dinickelorthosilikat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 23. Juli 2016. (JavaScript erforderlich)
- E. Yu Tonkov: High Pressure Phase Transformations Handbook 1. CRC Press, 1992, ISBN 978-2-88124-758-3, S. 590 (eingeschränkte Vorschau in der Google-Buchsuche).
- OECD: Chemical Thermodynamics of Nickel. Elsevier, 2005, ISBN 0-08-045754-1, S. 242 (eingeschränkte Vorschau in der Google-Buchsuche).
- William Alexander Deer, Robert Andrew Howie, J. Zussman: Rock-Forming Minerals: Orthosilicates, Volume 1A. Geological Society of London, 1982, ISBN 978-1-897799-88-8, S. 161 (eingeschränkte Vorschau in der Google-Buchsuche).
- Jun YATABE, Minoru KUMADA, Tsuneo IKAWA, Toshifumi KAGEYAMA: Synthesis of Nickel Silicate Using Nickel Nitrate and Water Glass as Raw Materials. In: Journal of the Ceramic Society of Japan. 103, 1995, S. 293, doi:10.2109/jcersj.103.293.
- Pierre Villars, Karin Cenzual, Roman Gladyshevskii: Handbook. Walter de Gruyter GmbH & Co KG, 2015, ISBN 978-3-11-031174-7, S. 727 (eingeschränkte Vorschau in der Google-Buchsuche).
- Takamitsu Yamanaka: Crystal structures of Ni2SiO4 and Fe2SiO4 as a function of temperature and heating duration. In: Physics and Chemistry of Minerals. 13, 1986, S. 227, doi:10.1007/BF00308273.
- O. Tamada, K. Fujino, S. Sasaki: Structures and electron distributions of α-Co2SiO4 and α-Ni2SiO4 (olivine structure). In: Acta Crystallographica Section B Structural Science. 39, S. 692, doi:10.1107/S0108768183003250.


