Dimethyltryptamin
N,N-Dimethyltryptamin, kurz DMT, ist ein halluzinogenes Tryptamin-Alkaloid. Es findet u. a. Anwendung als Psychedelikum bzw. Entheogen, indem es geraucht (als Freibase), geschnupft (als Yopo) oder injiziert (als Fumaratsalz) wird.[8] Eine Wirkung bei peroraler Aufnahme (etwa als Ayahuasca) ist nur bei gleichzeitiger bzw. vorheriger Einnahme von Monoaminooxidase-Hemmern (kurz MAOH oder MAOI) möglich, da DMT sehr rasch (First-Pass-Effekt) vom körpereigenen Enzym Monoaminooxidase (Typ A) abgebaut wird.[8][9]
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
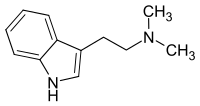 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Dimethyltryptamin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Kurzbeschreibung | ||||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse |
| |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte |
1,096 g·cm−3 (Base)[3] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| pKS-Wert |
8,68[5] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Dimethyltryptamin wurde erstmals im Jahre 1931 von dem kanadischen Chemiker Richard Helmuth Fredrick Manske (1901–1977) synthetisiert.
Wirkungen
Bei exogener Zufuhr wirkt DMT intensiv auf den visuellen Cortex des Gehirns ein und führt zu einer ausgeprägten Veränderung des visuellen Erlebens. Der Konsument bleibt sich in der Regel der Tatsache bewusst, dass er berauscht ist, und unterliegt im strengeren Sinn keinen Sinnestäuschungen, sondern extremen Formen von Pseudohalluzinationen. Höhere Dosierungen führen teils zur Wahrnehmung anderer Realitäten. Der Konsum kann zu Erlebnissen führen, die einer Nahtoderfahrung ähnlich sind.[10] Orale Einnahme, kombiniert mit MAO-Hemmern, führt meist zu Erbrechen, teils begleitet von Durchfall.
Pharmakologie
DMT wirkt als Voll-Agonist am 5-HT2A-Rezeptor[11] und bindet sich nicht selektiv mit Bindungsaffinitäten < 0,6 μM an folgende Serotonin-Rezeptoren: 5-HT1A, 5-HT1B, 5-HT1D, 5-HT2A, 5-HT2B, 5-HT2C, 5-HT6 und 5-HT7.[12][13][14][15][16] Auch bindet sich DMT an den Sigma-1-Rezeptor, was als Hinweis für seine Rolle als endogener Neurotransmitter gedeutet wird.[17][18] Das Gehirn von Ratten ist in der Lage, DMT zu synthetisieren und auszuschütten in Konzentrationen, die vergleichbar mit bekannten Neutrotransmittern sind.[19]
Im Gegensatz zu typverwandten Halluzinogenen wie LSD, Psilocin und Meskalin bildet DMT keine Toleranz aus, der Grund dafür ist unklar.[20] Untersuchungen an Ratten und Fliegen deuten darauf hin, dass DMT neuronale Plastizität fördert.[21]
Verwendung und Vorkommen


In Südamerika wird DMT seit Jahrtausenden verwendet.[22][23][24] Es ist der Hauptwirkstoff von Ayahuasca, einem zu Heilzwecken verwendeten Gebräu indigener Kulturen Südamerikas. Ayahuasca besteht aus einer DMT-Quelle (meist Psychotria viridis oder Diplopterys cabrerana) sowie monoaminooxidasehemmender Zutaten (meist Banisteriopsis caapi, eine Lianenart).[25]
Weitere Pflanzen, in denen DMT mit erhöhtem Anteil enthalten ist, sind Mimosa hostilis, Anadenanthera peregrina, Codariocalyx motorius (Telegrafenpflanze), Schilfrohr (Phragmites australis), Phalaris arundinacea (Rohrglanzgras) und andere Unterarten, viele Arten der Gattung Acacia sowie weiteren Pflanzen. Es kommt in den Hautdrüsensekreten der Aga-Kröte sowie möglicherweise auch in Säugetieren vor.[26][27][28] Ob DMT in einigen Geweben, auch des menschlichen Organismus, als „endogenes Dimethyltryptamin“ produziert wird, ist noch nicht abschließend wissenschaftlich bewiesen, dennoch legen einige Untersuchungen diese Annahme nahe.[29][30]
Rechtsstatus
DMT ist in der Bundesrepublik Deutschland gemäß Betäubungsmittelrecht aufgrund seiner Aufführung in der Anlage I BtMG ein nicht verkehrsfähiges Betäubungsmittel. Der Umgang ohne Erlaubnis ist grundsätzlich strafbar.
Literatur
- Rick Strassman: DMT, Das Molekül des Bewusstseins, AT Verlag, Baden 2004, ISBN 3-85502-967-9
- Jonathan Ott: Ayahuasca-Analoge: pangaeische Entheogene. 1996, ISBN 3-930442-08-6
- T. M. Carbonaro, M. B. Gatch: Neuropharmacology of N,N-dimethyltryptamine. In: Brain research bulletin. April 2016, doi:10.1016/j.brainresbull.2016.04.016, PMID 27126737 (Review).
- Klaus Helm: Synthese und funktionelle In-vitro Pharmakologie neuer Liganden des 5-HT2A-Rezeptors aus der Klasse der Tryptamine. Dissertationsschrift, Universität Regensburg 2014
- S. A. Barker: N,N-Dimethyltryptamine (DMT), an Endogenous Hallucinogen: Past, Present, and Future Research to Determine Its Role and Function. In: Frontiers in neuroscience. Band 12, 2018, S. 536, doi:10.3389/fnins.2018.00536, PMID 30127713, PMC 6088236 (freier Volltext) (Review).
Weblinks
- DMT. In: Erowid. (englisch)
- isomerdesign.com: DMT (englisch)
- DMT: The Spirit Molecule in der Internet Movie Database (englisch)
- Serie: Halluzinogene: DMT – Das stärkste Psychedelikum der Welt. In: spektrum.de. 26. Januar 2019, abgerufen am 5. Februar 2019.
Einzelnachweise
- Qu, Shi-Jin; Tan, Chang-Heng; Zhu, Da-Yuan; Wang, Gui-Feng; Zuo, Jian-Ping; Duan, Wen-Hu; Yao, Shan-Yan: Tryptamine derivatives as novel non-nucleosidic inhibitors against hepatitis B virus. In: Bioorganic & Medicinal Chemistry 19 (2011) 3120–3127, doi:10.1016/j.bmc.2011.04.004.
- Royal Pharmaceutical Society (Hrsg.): Clarke's Analysis of Drugs and Poisons FOURTH EDITION. Pharmaceutical Press, London/Chicago 2011, ISBN 978-0-85369-711-4.
- R. Bergin, D. Carlström, G. Falkenberg, H. Ringertz: Preliminary X-ray crystallographic study of some psychoactive indole bases in Acta Cryst. B 24 (1968) 882, doi:10.1107/S0567740868003353.
- Eintrag zu N,N-Dimethyltryptamin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. Mai 2014.
- Eintrag zu N,N-Dimethyltryptamine in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- Datenblatt N,N-Dimethyltryptamine ≥97% (HPLC) bei Sigma-Aldrich, abgerufen am 17. Dezember 2021 (PDF).
- Datenblatt DMT (PDF; 38 kB) bei Tocris Bioscience, abgerufen am 8. März 2013.
- Rick Strassman: DMT, Das Molekül des Bewusstseins, AT Verlag, Baden 2004, ISBN 3-85502-967-9.
- Dimethyltryptamine (DMT). In: The Drug Classroom. Abgerufen am 6. Dezember 2018 (amerikanisches Englisch).
- DMT Models the Near-Death Experience. Front. Psychol., 15 August 2018, abgerufen am 1. September 2018. DOI:10.3389/fpsyg.2018.01424
- Smith RL, Canton H, Barrett RJ, Sanders-Bush E: Agonist properties of N,N-dimethyltryptamine at serotonin 5-HT2A and 5-HT2C receptors. In: Pharmacol. Biochem. Behav.. 61, Nr. 3, November 1998, S. 323–30. doi:10.1016/S0091-3057(98)00110-5. PMID 9768567.
- Keiser M.J., Setola V., Irwin J.J., Laggner C., Abbas A.I., Hufeisen S.J., Jensen N.H. et al.: Predicting new molecular targets for known drugs. In: Nature. 462, Nr. 7270, November 2009, S. 175–81. doi:10.1038/nature08506. PMID 19881490. PMC 2784146 (freier Volltext).
- Deliganis A.V., Pierce P.A., Peroutka S.J.: Differential interactions of dimethyltryptamine (DMT) with 5-HT1A and 5-HT2 receptors. In: Biochemical Pharmacology. 41, Nr. 11, Juni 1991, S. 1739–44. doi:10.1016/0006-2952(91)90178-8. PMID 1828347.
- Pierce P.A., Peroutka S.J.: Hallucinogenic drug interactions with neurotransmitter receptor binding sites in human cortex. In: Psychopharmacology. 97, Nr. 1, 1989, S. 118–22. doi:10.1007/BF00443425. PMID 2540505.
- Smith R.L., Canton H., Barrett R.J., Sanders-Bush E.: Agonist properties of N,N-dimethyltryptamine at serotonin 5-HT2A and 5-HT2C receptors. In: Pharmacology, Biochemistry and Behavior. 61, Nr. 3, November 1998, S. 323–30. doi:10.1016/S0091-3057(98)00110-5. PMID 9768567.
- T. S. Ray: Psychedelics and the human receptorome. In: PloS one. Band 5, Nummer 2, 2010, S. e9019, doi:10.1371/journal.pone.0009019. PMID 20126400, PMC 2814854 (freier Volltext).
- Fontanilla D., Johannessen M., Hajipour A.R., Cozzi N.V., Jackson M.B., Ruoho A.E.: The Hallucinogen N,N-Dimethyltryptamine (DMT) Is an Endogenous Sigma-1 Receptor Regulator. In: Science. 323, Nr. 5916, Februar 2009, S. 934–7. doi:10.1126/science.1166127. PMID 19213917. PMC 2947205 (freier Volltext).
- Su T.P., Hayashi T., Vaupel D.B.: When the Endogenous Hallucinogenic Trace Amine N,N-Dimethyltryptamine Meets the Sigma-1 Receptor. In: Science Signaling. 2, Nr. 61, 2009, S. pe12. doi:10.1126/scisignal.261pe12. PMID 19278957. PMC 3155724 (freier Volltext).
- Jon G. Dean, Tiecheng Liu, Sean Huff, Ben Sheler, Steven A. Barker: Biosynthesis and Extracellular Concentrations of N,N-dimethyltryptamine (DMT) in Mammalian Brain. In: Scientific Reports. Band 9, Nr. 1, 27. Juni 2019, ISSN 2045-2322, S. 9333, doi:10.1038/s41598-019-45812-w (nature.com [abgerufen am 13. Januar 2022]).
- D. E. Nichols: Hallucinogens. In: Pharmacology & Therapeutics. Band 101, Nummer 2, Februar 2004, S. 131–181, doi:10.1016/j.pharmthera.2003.11.002. PMID 14761703.
- Psychedelic drugs promote neural plasticity in rats and flies. Abgerufen am 28. April 2019 (englisch).
- M. L. Pochettino, A. R. Cortella and M. Ruiz: Hallucinogenic Snuff from Northwestern Argentina: Microscopical Identification of Anadenanthera colubrina var. cebil (Fabaceae) in Powdered Archaeological Material. Economic Botany, 1999, abgerufen am 20. Mai 2019.
- José M. Capriles, Christine Moore, Juan Albarracin-Jordan, Melanie J. Miller: Chemical evidence for the use of multiple psychotropic plants in a 1,000-year-old ritual bundle from South America. In: Proceedings of the National Academy of Sciences. 1. Mai 2019, ISSN 0027-8424, S. 201902174, doi:10.1073/pnas.1902174116, PMID 31061128 (pnas.org [abgerufen am 21. Mai 2019]).
- Yasmin Anwar, Media Relations| May 6, 2019May 16, 2019: Ayahuasca fixings found in 1,000-year-old Andean sacred bundle. 6. Mai 2019, abgerufen am 21. Mai 2019 (amerikanisches Englisch).
- Dennis J. McKenna, G.H.N. Towers, et al.: Monoamine oxidase inhibitors in South American hallucinogenic plants: Tryptamine and β-carboline constituents of Ayahuasca. In: Journal of Ethnopharmacology. 10, 1984, S. 195–223, doi:10.1016/0378-8741(84)90003-5.
- Barker S.A., Monti J.A., Christian S.T.: N, N-dimethyltryptamine: an endogenous hallucinogen. In: International Review of Neurobiology. 22, 1981, S. 83–110. doi:10.1016/S0074-7742(08)60291-3. PMID 6792104.
- Wallach J.V.: Endogenous hallucinogens as ligands of the trace amine receptors: a possible role in sensory perception. In: Medical Hypotheses. 72, Nr. 1, Januar 2009, S. 91–4. doi:10.1016/j.mehy.2008.07.052. PMID 18805646.
- M. A. Thompson: Rabbit Lung Indolethylamine N-Methyltransferase. cDNA AND GENE CLONING AND CHARACTERIZATION. In: Journal of Biological Chemistry. 273, S. 34502–34510, doi:10.1074/jbc.273.51.34502.
- Steven A. Barker, Ethan H. McIlhenny, Rick Strassman: A critical review of reports of endogenous psychedelic N,N-dimethyltryptamines in humans: 1955-2010. In: Drug Testing and Analysis. 4, 2012, S. 617–635, doi:10.1002/dta.422.
- Jimo Borjigin, Michael M. Wang, Rick J. Strassman, Steven A. Barker, Ben Sheler: Biosynthesis and Extracellular Concentrations of N,N-dimethyltryptamine (DMT) in Mammalian Brain. In: Scientific Reports. Band 9, Nr. 1, 27. Juni 2019, S. 9333, doi:10.1038/s41598-019-45812-w.
