Dikaliumnonahydridorhenat(VII)
Dikaliumnonahydridorhenat(VII) ist eine anorganische chemische Verbindung aus der Gruppe der Rhenate.
| Kristallstruktur | |||||||
|---|---|---|---|---|---|---|---|
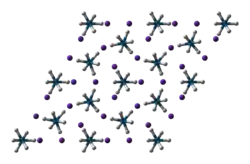 | |||||||
| _ K+ _ Re7+ _ H− | |||||||
| Allgemeines | |||||||
| Name | Dikaliumnonahydridorhenat(VII) | ||||||
| Verhältnisformel | K2ReH9 | ||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 273,4 g·mol−1 | ||||||
| Aggregatzustand |
fest[1] | ||||||
| Dichte |
3,07 g·cm−3[1] | ||||||
| Löslichkeit |
löslich in Wasser[1] | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Gewinnung und Darstellung
Dikaliumnonahydridorhenat(VII) kann durch eine zweistufige Reaktion gewonnen werden. Dabei wird zuerst Dinatriumnonahydridorhenat(VII) mit Bariumhydroxid umgesetzt und das entstehende Zwischenprodukt mit einer Mischung aus Kaliumsulfat und Kaliumhydroxid umgesetzt.[1]
Eigenschaften
Dikaliumnonahydridorhenat(VII) ist ein diamagnetisches weißes Pulver, das löslich in Wasser ist und durch Alkali stabilisiert wird. Es ist wenig löslich in Methanol. An normal feuchter Luft ist es unbeständig unter Bildung von Perrhenat und Carbonat. Es besitzt eine hexagonale Kristallstruktur mit der Raumgruppe P62m (Raumgruppen-Nr. 189) und den Gitterparametern a = 960,7 pm und c = 550,8 pm.[1][3] Die wasserstoffreichen Verbindungen K2ReH9, BaReH9 und K2TcH9 enthalten komplexe Anionen, deren Metallatome sich in dreifach überdachten trigonalen Prismen aus Wasserstoffatomen befinden.[4] Dikaliumnonahydridorhenat(VII) wurde in den 1960er Jahren als erste komplexe Übergangsmetallhydridverbindung entdeckt.[5][6]
Einzelnachweise
- Georg Brauer (Hrsg.) u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band III, Ferdinand Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1624.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- W. Bronger, L. à Brassard, P. Müller, B. Lebech, Th. Schultz, K2ReH9, eine Neubestimmung der Struktur, Zeitschrift für anorganische und allgemeine Chemie, 21. Juni 1999, Volume 625, Issue 7, S. 1143–1146 (doi:10.1002/(SICI)1521-3749(199907)625:7<1143::AID-ZAAC1143>3.0.CO;2-V).
- Christoph Janiak, Hans-Jürgen Meyer, Dietrich Gudat, Ralf Alsfasser: Riedel Moderne Anorganische Chemie. Walter de Gruyter, 2012, ISBN 3-11-024901-4, S. 274 (eingeschränkte Vorschau in der Google-Buchsuche).
- Michael Hirscher: Handbook of Hydrogen Storage. John Wiley & Sons, 2010, ISBN 3-527-62981-5, S. 149 (eingeschränkte Vorschau in der Google-Buchsuche).
- Richard Earl Dickerson, Hans-Werner Sichting: Prinzipien der Chemie. Walter de Gruyter, 1988, ISBN 3-11-009969-1, S. 50 (eingeschränkte Vorschau in der Google-Buchsuche).