Cucurbitacine
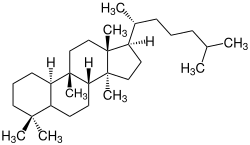
Cucurbitacine sind Bitterstoffe, die hauptsächlich in der Familie der Kürbisgewächse und Braunwurzgewächse (zum Beispiel Bacopa monnieri) vorkommen. Die Gruppe leitet sich vom Cucurbitan ab, einem tetracyclischen Triterpen und Steroid. Es sind rund 40 Cucurbitacine bekannt. Mit Ausnahme der Vertreter Cucurbitacin A, Cucurbitacin C und Cucurbitacin F kommen sie vorwiegend als Glycoside vor.[1]

Vorkommen
Cucurbitacine kommen vorwiegend in Gurken (Cucumis) und Kürbisgewächsen (Cucurbitaceae), einigen Kreuzblütlern (Brassicaceae) sowie in dem japanischen Ständerpilz (Basidiomycetes) Hebeloma vinosophyllum vor.[1]
Unter den Gurken existieren zahlreiche Cultivare, die sich im Vorhandensein bzw. Fehlen des Cucurbitacin C unterscheiden. Dies konnte bereits in frühen Untersuchungen auf einen einzelnen diallelischen Genlocus (= Genort mit zwei verschiedenen Allelen) zurückgeführt werden. Dabei führt das Allel Bi (für „bitter“) zu Gurkenpflanzen, die unter Stressbedingungen bitter werden und an die 300 mg/kg Frischgewicht akkumulieren. Dies gilt sowohl für die Frucht, das heißt die Gurke, als auch für die gesamte Pflanze. Daher ist die Fähigkeit zur Synthese von Cucurbitacin C bereits im Keimblattstadium ermittelbar. Das Allel bi (für „nicht bitter“) verhindert diese Akkumulation.[2] Seit dieser Entdeckung Ende der 1950er Jahre wird bis zum heutigen Tag der gesamte – zumindest mitteleuropäische – Markt von nicht-bitteren Gurken bestimmt.
Struktur
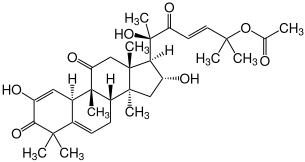
Chemisch gesehen gehören Cucurbitacine zur Gruppe der Tri-Terpenoide mit vier Ringschlüssen (tetrazyklische Triterpene), aufbauend auf dem Grundgerüst des Gonan bzw. Cucurbitan. Alle Cucurbitacine sind ungesättigte Derivate des Cucurbitans, die mehrere Hydroxy- und Ketogruppen tragen (charakteristisch ist eine 11-Oxo-Gruppe) und teilweise acetyliert sind.[1]
Die 40 natürlicherweise vorkommenden Vertreter sowie andere synthetisch veränderte werden in 12 verschiedene Klassen eingeteilt, unter anderem in Abhängigkeit von ihrer Oxygenierung. Bekannt sind die Cucurbitacine A bis S, die Norcucurbitacine und das cardiotoxische Elaterinid (synonym Gratiotoxin, Colocynthin, alpha-Elaterin-2-D-Glucopyranosid, Curcurbitacin-E-beta-Glucosid, Colosid A).[3] Cucurbitacine können glykosyliert sein.[4]
Eigenschaften
Die Cucurbitacine sind hitzebeständig und kaum wasserlöslich; ihr Gehalt bleibt daher beim Kochen von Gemüse erhalten. Umweltstress, also Hitze, Temperaturschwankung, Feucht-Trocken-Schwankung, Pilzinfektion feuchter Pflanzen, sowie Überreife und falsche Lagerung kann neben Rückkreuzung zu erhöhtem Gehalt an Cucurbitacinen in Kürbis, Zucchini, Melone und Gurke führen.
Der bittere Geschmack der Cucurbitacine ist noch in sehr niedrigen Konzentrationen wahrnehmbar (die Geschmacksschwelle liegt bei 10−6 mol/L). Weiterhin haben sie eine stark abführende, diuretische, blutdrucksenkende und antirheumatische Wirkung.[1] Außerdem wurde die Wirkung von Cucurbitacin als Lockstoff aus der Gruppe der Kairomone für einige Käferarten wie Diabrotica nachgewiesen.[5]
Toxizität
Alle Cucurbitacine sind toxisch und wirken auch insektizid und fungizid. Die zytotoxische Wirkung wurde experimentell als Chemotherapeutikum in der Krebstherapie erprobt.[6][7]
Eine besondere Vergiftungsgefahr geht von Zier- und Wildkürbissen aus. Durch Rückmutationen oder unkontrollierte Rückkreuzung kultivierter Kürbisse, vereinzelt auch von Garten-Zucchini,[8] mit Wildkürbissen können die Cucurbitacine auch schwere, in seltenen Fällen tödlich verlaufende Lebensmittelvergiftungen verursachen.[9][8]
Folgende Vergiftungsfälle wurden gemeldet:
- 1981/1982 in Australien,
- 1984 in Alabama und Kalifornien,[10]
- 2001 in Neuseeland,[11]
- 2010 in Indien[12]
- und – vermutlich durch das besonders heiße Wetter Juli/August 2015 – in Deutschland.[8][13]
Die LD50 für Cucurbitacin-B beim Tiermodell Maus beträgt bei oraler Aufnahme 5 mg pro kg Körpergewicht, woraus man auf eine tödliche Dosis von etwa 300 mg beim Menschen schließen kann. Der stark bittere Geschmack verhindert üblicherweise die Aufnahme von gefährlich hohen Dosen. Es gibt keine Rechtsnormen, die den Höchstgehalt von Cucurbitacinen in der Nahrung festlegen. Die Pflanzen der Familie Cucurbita sind jedoch 2009 bei der Europäischen Behörde für Lebensmittelsicherheit (EFSA) im Compendium of botanicals that have been reported to contain toxic, addictive, psychotropic or other substances of concern verzeichnet.[14]
Siehe auch
Literatur
- P. Bhandari et al.: Cucurbitacins from Bacopa monnieri. In: Phytochemistry. Band 68, Nr. 9, 2007, S. 1248–1254, PMID 17442350.
Weblinks
- Strukturformel und Enzyme
- Datenblatt Cucurbitacin I hydrate bei Sigma-Aldrich, abgerufen am 12. Juni 2011 (PDF).
Einzelnachweise
- Eintrag zu Cucurbitacine. In: Römpp Online. Georg Thieme Verlag, abgerufen am 21. August 2015.
- J. M. Andeweg, J. W. De Bruyn: Breeding of non-bitter cucumbers. In: Euphytica. 8, 1959, S. 13, doi:10.1007/BF00022084.
- Wolfgang Blaschek, Rudolf Hänsel, Konstantin Keller, Jürgen Reichling, Horst Rimpler, Georg Schneider (Hrsg.): Hagers Handbuch der Pharmazeutischen Praxis: Folgeband 2: Drogen A-K. 5. Ausgabe, Springer-Verlag, 2013. ISBN 978-3-642-58928-7. S. 809–810. eingeschränkte Vorschau in der Google-Buchsuche
- Eine Übersicht über Vorkommen und Wirkungen in: J. C. Chen, M. H. Chiu u. a.: Cucurbitacins and cucurbitane glycosides: structures and biological activities. In: Natural Product Reports. Band 22, Nummer 3, Juni 2005, S. 386–399, doi:10.1039/b418841c, PMID 16010347 (Review).
- R. L. Metcalf, R. A. Metcalf, A. M. Rhodes: Cucurbitacins as kairomones for diabroticite beetles. In: PNAS. Band 77, Nummer 7, Juli 1980, S. 3769–3772, PMID 16592849, PMC 349707 (freier Volltext).
- M. S. van Kester, J. J. Out-Luiting u. a.: Cucurbitacin I inhibits Stat3 and induces apoptosis in Sézary cells. In: Journal of Investigative Dermatology. Band 128, Nummer 7, Juli 2008, S. 1691–1695, doi:10.1038/sj.jid.5701246, PMID 18200050.
- T. Liu, M. Zhang u. a.: Inhibitory effects of cucurbitacin B on laryngeal squamous cell carcinoma. In: European archives of oto-rhino-laryngology. Band 265, Nummer 10, Oktober 2008, S. 1225–1232, doi:10.1007/s00405-008-0625-9, PMID 18309509.
- Erwin Bachmann: Mann nach Zucchini-Mahlzeit auf Intensivstation. In: Heidenheimer Zeitung, 14. August 2015.
- Matthias Karl Bernhard et al.: Cucurbitacin-Vergiftung durch Kürbisse – ein Fallbericht (Memento des Originals vom 24. September 2015 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.. Kinder- und Jugendmedizin 5 (2003).
- Bitterness in Cucumber & Zucchini. UNL Extension: Hort Update, University of Nebraska-Lincoln. Abgerufen 21. August 2015.
- Richard Lawley, Laurie Curtis, Judy Davi: The Food Safety Hazard Guidebook. Royal Society of Chemistry, 2012, ISBN 978-1-84973-381-6, S. 264 (eingeschränkte Vorschau in der Google-Buchsuche).
- The Times (of India), 10. Juli 2010, abgerufen 21. August 2015.
- orf.at: D: Mann stirbt an Vergiftung durch Eigenbau-Zucchini. 20. August 2015, abgerufen 21. August 2015.
- EFSA Compendium of botanicals that have been reported to contain toxic, addictive, psychotropic or other substances of concern. (Memento des Originals vom 24. September 2015 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. In: EFSA Journal Band 7, Nummer 9, 2009, S. 34. (PDF-Datei)