Cochlea-Implantat
Das Cochlea-Implantat (englisch cochlear implant, CI) ist eine Hörprothese für Gehörlose und Ertaubte, deren Hörnerv als Teilorgan der auditiven Wahrnehmung noch funktionsfähig ist, sowie für hochgradig Schwerhörige, bei denen die Versorgung mit einem Hörgerät nicht mehr ausreichend ist.
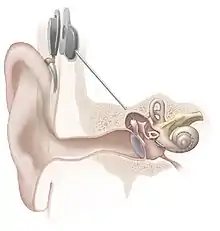
Das CI-System besteht einerseits aus einem Sprachprozessor mit einem Mikrofon, an dem eine Sendespule mit Magnet angebunden ist. Andererseits besteht es aus dem eigentlichen Implantat, das sich aus einem weiteren Magneten, einer Empfangsspule, dem Stimulator und dem Elektrodenträger mit den Stimulationselektroden zusammensetzt. Die Elektroden werden in die Cochlea (Hörschnecke) eingeführt. Die Empfangsspule wird im Schädelknochen nahe der Ohrmuschel unter der Haut platziert. Die Sendespule des Prozessors haftet mit Hilfe der Magneten auf der Kopfhaut über der Empfangsspule des Implantats. Die Spannungsversorgung des Implantats erfolgt durch die Kopfhaut mittels elektromagnetischer Induktion. Die Signalübertragung erfolgt mit Hochfrequenzwellen. Manchmal wird nur das Implantat als CI, die komplette Anlage als CI-System bezeichnet.
Geschichte
André Djourno und Charles Eyriès entwickelten im Jahr 1957 das erste Implantat, welches das zerstörte Innenohr durch ein elektronisches Gerät ersetzte, sie nannten es nach dessen lateinischem Namen. Das ursprüngliche Implantat stimulierte den intakten Gehörnerv über einen einzigen Kanal.[1] Pionierarbeit zur einsatzfähigen Entwicklung des Gerätekonzepts leisteten ab den 1960er Jahren William F. House in den USA,[2] Graeme Clark in Australien und das Ehepaar Ingeborg und Erwin Hochmair in Österreich. House befasste sich dabei mit einer einkanaligen Übertragung, während Clark und das Ehepaar Hochmair mit einem mehrkanaligen Übertragungskonzept letztlich erfolgreicher in der Anwendung und Vermarktung waren. Clark setzte 1964 eine einkanalige Elektrode in die Cochlea eines Patienten an der Stanford University ein.[3]
Genauere Untersuchungen haben jedoch gezeigt, dass die einkanaligen Cochlea-Implantate nur begrenzt nutzbar sind, da sie verschiedene Bereiche der Cochlea nicht zu unterschiedlichen Zeiten stimulieren können, um eine Unterscheidung zwischen niedrigen und mittleren bis hohen Frequenzen zu ermöglichen, wie dies für eine gute Spracherkennung erforderlich ist.[4]
Der NASA-Ingenieur Adam Kissiah begann Mitte der 1970er Jahre mit der Entwicklung eines mehrkanaligen Gerätes. Angeregt wurde er dazu beim Stöbern in Kennedys technischer Bibliothek während seiner Arbeitspausen. Intensiv untersuchte Kissiah bald die Auswirkungen technischer Prinzipien auf das Innenohr und entwickelte um 1978 ein komplettes neuartiges Gerät. Die NASA half ihm, das neue Gerät patentieren zu lassen. Die Patentrechte verkaufte er jedoch später.[5]
Einsatzgebiet und präoperative Abklärung
Eine CI-Versorgung ist dann angezeigt, wenn mittels bester herkömmlicher schallverstärkender Hörgeräte kein ausreichendes Sprachverstehen mehr erzielt werden kann. Das ist ab einer kritischen Anzahl zerstörter Haarzellen der Fall. In Deutschland wird zur Untersuchung des Sprachverstehens mit Hörgeräten bei Jugendlichen und Erwachsenen beispielsweise der Freiburger Einsilbertest verwendet. Hier kann man durch den Vergleich des Sprachverstehens durchschnittlicher CI- und Hörgeräteträger feststellen, dass ein Sprachverstehen der Einsilber mit besten Hörgeräten von nur noch 30 % oder weniger bei mittlerem Sprachpegel (65 dB SPL) mit CIs wesentlich verbessert werden kann. Über 75 Prozent der CI-Träger verstehen mehr als 30 Prozent einsilbige Worte, 50 Prozent sogar mehr als 62 Prozent Einsilber. Generell gilt die Empfehlung, dass sich Patienten mit weniger als 40 Prozent Einsilberverstehen bei normal lauter Sprache möglichst frühzeitig bei einer implantierenden Klinik über die aktuellen Möglichkeiten moderner CIs beraten lassen sollten. Die Erfolgsaussicht hängt wesentlich von der Dauer des kritischen Hörverlusts (ggf. Ertaubungsdauer), der Sprachkompetenz, dem Zustand der Hörnervs, dem Vorliegen zentral auditiver Wahrnehmungs- und Verarbeitungsstörungen und der Motivation des Patienten zum Erkennen und Identifizieren der häufig variablen Höreindrücke und Sprachlaute ab. Folglich ist die präoperative Abklärung der Kandidatur eines Patienten für ein Cochleaimplantat von größter Priorität. Die S2k-Leitlinien empfehlen seit 2020 neben den etablierten Abklärungen auch die standardisierte Erfassung von Fragebögen zur Hörperformance, Lebensqualität und ausführliche Testung des Sprachverstehens mit und ohne Hörgerät. In speziellen Fällen, bei denen eine potentiell retro-cochleäre oder kortikale Hörstörung vorliegen könnte, wird eine präoperative EBERA und/oder ECERA empfohlen.
Bei Erwachsenen, die schon vor dem Spracherwerb ertaubt sind, ist eine CI-Versorgung schwieriger, da sich hier der Hörnerv wegen der langen Dauer der Reizlosigkeit oft bereits zu stark abgebaut hat. Wenn der Hörnerv noch intakt ist, können auch lange ertaubte Erwachsene Hör-Erfolge haben. Diese sind jedoch nicht zu vergleichen mit denjenigen von erst kurz Ertaubten. Bei kleinen Kindern ist eine Bewertung des Sprachverstehens auf der Basis des Einsilbertests nicht möglich. Hier entscheidet man üblicherweise aufgrund der Hörschwelle. Auf der Bewertungsbasis der modernen CIs gilt als Richtmaß eine Hörschwelle von 80 dB HL oder schlechter ab 1000 Hz und höher als Indikation zur CI-Versorgung.
Funktionsweise
Das Cochlea-Implantat besteht aus einem externen Teil (bestehend aus Mikrofon, Sprachprozessor, Batterie oder Akku und Spule) und einem implantierten Teil (bestehend aus Spule, Signalprozessor mit Stimulator und Elektroden für die Stimulation). Der externe Teil wird meist hinter dem Ohr getragen (Versuche, diese Einheit ebenfalls zu implantieren, schlugen bisher fehl) und überträgt digitale Informationen über die äußere Spule an die implantierte Spule. Die Spulen sind jeweils mit einem Magneten ausgestattet, um eine korrekte Lage zu gewährleisten. Die innere Spule leitet die empfangenen Signale an eine Stimulationsschaltung, welche die erforderlichen Ströme für die Elektroden in der Cochlea erzeugt. Die Ströme erregen den Hörnerv des Ohres, der den Haarzellen nachgeschaltet ist. Unterschiedliche Erregungsorte regen Nerven unterschiedlicher Frequenzanpassung an. Die Stärke des elektrischen Stromes ist entscheidend für die Lautheit.
Für die Digitalisierung des Audiosignals vom Mikrofon und die Stimulation innerhalb der Cochlea verwenden die Hersteller verschiedene Kodierungs- und Stimulationsstrategien. Die Elektroden können den Hörnerv parallel oder sequentiell stimulieren. Bei der parallelen Stimulierung können zwei oder mehr Elektroden gleichzeitig die Hörnerven reizen, bei der sequentiellen Stimulierung erfolgt die Stimulierung nacheinander. Trotz unterschiedlicher Stimulationsstrategien und Sprachkodierungen zeigt sich, dass das Sprachverstehen bei den drei großen Herstellern etwa gleich gut ist.
Implantation
Die Implantation geschieht in der Regel unter Narkose, wobei bereits erste Operationen lediglich mit örtlicher Betäubung durchgeführt wurden.[6] Vor der Operation wurden früher oft die Haare hinter dem Ohr wegrasiert, bei den heutigen Methoden ist das allerdings kaum noch nötig. Dann wird die Haut hinter dem Ohr 5 bis 8 cm weit aufgeschnitten und nach hinten geklappt. Aus dem nun freiliegenden Schädelknochen wird eine Vertiefung ausgefräst, die später das Stimulatorgehäuse des Implantats aufnehmen soll. Bei Kindern wird dabei die Hirnhaut (Dura) teilweise freigelegt. Dann wird durch das Felsenbein ein Kanal gefräst, der bis ins Mittelohr reicht. Er muss so platziert werden, dass das runde Fenster, welches zum Innenohr führt, zugänglich wird. Durch diesen Kanal hindurch wird nun ein kleiner Bohrer eingeführt und ein Loch in die Cochlea gebohrt. Das geschieht meist in der Nähe des runden Fensters. Durch das Loch wird das Elektrodenbündel des Implantats maximal tief in die Scala tympani eingeführt. Das dünne Anschlusskabel wird am Felsenbein fixiert, um ein Herausrutschen des Elektrodenarrays zu verhindern. Hierzu kann ein Tunnel in den Knochen gefräst werden, worauf mittlerweile durch die Nutzung eines Fixationsclips verzichtet werden kann, was gerade im Fall eines Gushers als nützlich gilt[7].

Je nach Operationstechnik wird nun der Kanal im Felsenbein mit Knochenmaterial verfüllt oder offen gelassen. Das Implantat kann daraufhin mit medizinischem Garn in der dafür vorgesehenen Vertiefung fixiert werden. Zum Schluss wird noch eine eventuell vorhandene Potenzialausgleichselektrode unter die Kopfhaut geschoben und zuletzt der Hautlappen wieder vorgeklappt und zugenäht. Noch während der Operation wird mit Spezialgeräten die Funktion des Implantats getestet. Hier stehen mehrere Messmethoden zur Verfügung. Durch die elektrische Auslösung des Stapediusreflex (ESR) kann nachgewiesen werden, dass die elektrische Reizung durch das CI den Hirnstamm erreicht. Hierfür sind anatomische Voraussetzungen vonnöten, die nicht bei jedem Patienten vorliegen. Mittels einer Telemetriemessung kann der Kontakt zur Gewebe in der Cochlea bestimmt werden, was beispielsweise bei unsicherer kompletten Insertion des Elektrodenträgers hilfreich sein kann. Die Bestimmung der neuronalen Antwort erfolgt durch die Messung von den sog. eCAPs. Dies stellt das elektrisch evozierte Analogon der Elektrocochleographie dar. Weitergehende Informationen über den Zustand der zum Gehirn führenden Hörbahn im Hirnstamm bietet die intraoperative Bestimmung der elektrisch ausgelösten Nervenaktionspotentiale des Hirnstammes (=EBERA; BERA, ABR). Damit kann auch bei kleinen Kindern der Reifungsstand der Hörbahn bestimmt werden.
Hörempfindung und Hörtraining

Die elektrischen Reize in der Hörschnecke erzeugen beim CI-Träger individuelle Hörempfindungen, die anders sind als die von Normalhörenden. Der neuronale Mechanismus für die Verarbeitung von akustischen Reizen ist aber so flexibel, dass eine Anpassung an diese Empfindungen stattfindet. Ein intensives, langes Hörtraining nach der Operation ist erforderlich, um die neuen Signale den bekannten Hörmustern zuzuordnen. Bei Erwachsenen erfolgt das mittels Audiotherapie, bei gehörlosen oder hörgeschädigten Kindern gibt es die auditiv-verbale Erziehung, die sich hauptsächlich mit dem Erlernen der Lautsprache beschäftigt. Die Therapie mit CI hat Ähnlichkeit mit dem Erlernen einer Fremdsprache. Der Zeitraum, der für das Sprachverstehen benötigt wird, ist individuell unterschiedlich. Für Kinder wird die Dauer auf etwa zwei bis drei Jahre veranschlagt. Erwachsene, die gerade ertaubt sind und frühzeitig mit einem Cochlea-Implantat versorgt werden, benötigen gewöhnlich eine kürzere Rehabilitationsphase.
Medizinische Risiken
Zu den allgemeinen Risiken einer Operation treten spezielle Risiken auf.
- Eine gewisse Gefahr besteht für den Gesichtsnerv und den Geschmacksnerv, da der Kanal für den Elektrodenträger in deren Nähe gefräst wird. Der Chirurg muss daher extrem vorsichtig mit Hilfe von Fazialismonitoring vorgehen, um die Gesichts- und Geschmacksnerven nicht zu verletzen.
- Es besteht ein geringes Risiko einer Meningitis nach der Implantation. Das ist der Fall, wenn Keime über die Eintrittsstelle des Elektrodenbündels eindringen.
Umfang
Am 31. Dezember 2011 gab es weltweit rund 300.000 CI-Träger, davon etwa 30.000 in Deutschland.[8] Im Dezember 2019 wurden weltweit rund 736.900 CI-Träger registriert.[9]
Versorgung von Kleinkindern
Die CI-Versorgung von hochgradig schwerhörenden oder gehörlosen Kleinkindern ist heute aufgrund der im Vergleich zur Hörgeräteversorgung überragenden Hör- und Spracherwerbsleistung medizinischer Standard und wird von einer großen Mehrheit der betroffenen Eltern angenommen. Die Versorgung ist vor dem 2. Lebensjahr empfohlen,[10] da die Resultate mit steigendem Implantationsalter schlechter werden.[11] Eine Implantation nach dem achten Lebensjahr erscheint für die meisten von Geburt an gehörlosen Kinder weniger sinnvoll, da ein Erwerb oder die Verbesserung der Lautsprache durch das Gehör dann nur noch sehr eingeschränkt möglich ist. Das gilt natürlich nicht, wenn ein Kind früher ausreichend mit Hörgeräten versorgt werden konnte und durch eine Verschlechterung der Hörschwelle erst später Sprache mit Hörgeräten nicht mehr ausreichend verstehen kann. Die Kosten sowohl für die einseitige als auch für die beidseitige Implantation werden in Deutschland vollständig von den Krankenkassen, in der Schweiz von der Invalidenversicherung übernommen.
Versorgungsmöglichkeiten
Es gibt zahlreiche Kombinationen, die sich bei einer Versorgung eines Patienten ergeben können. In den folgenden Unterpunkten sollen die wichtigsten beleuchtet werden: Die bilaterale Versorgung mit CIs (BiCI), die einseitige Versorgung bei einseitig Ertaubten (CI-SSD) & die Versorgung von Patienten mit einem Hörgerät auf der kontralateralen Seite (bimodale Versorgung).
Bilaterale CI-Versorgung (BiCI)
Viele Jahre wurde üblicherweise nur in ein Ohr implantiert, auch wenn beide Ohren ertaubt waren. Langjährige psychoakustische Forschungsergebnisse zum binauralen Hören (und natürlich die alltägliche Hörerfahrung, wenn man sich ein Ohr verschließt) konnten aber nachweisen, dass gerade das Sprachverstehen mit nur einem Ohr schlechter ist als mit zwei Ohren und das vor allem in (den üblichen alltäglichen) geräuschvollen Hörsituationen. Bei Kindern sollten Phasen von einseitigem Hören folglich vermieden werden. Bei der Hörgeräteversorgung hat man diesen Umstand schon seit den 1970er Jahren in der beidohrigen Standardversorgung berücksichtigt.
1996 konnte erstmal in der Würzburger Arbeitsgruppe um Prof. Helms eine signifikante Verbesserung im Sprachverstehen durch eine bilaterale CI-Versorgung nachgewiesen werden[12]. Etwa seit 2000, vor allem seit der Einführung von hinter dem Ohr getragenen digitalen Signalprozessoren, wird an fast allen CI-Kliniken auch die beidohrige CI-Versorgung angeboten. Patienten mit beidseitiger CI-Versorgung werden in Fachkreisen mit BiCI abgekürzt.
Versorgung von einseitig Ertauben (CI-SSD)
Die Versorgung von einseitig ertaubten Patienten (kurz: SSD; aus dem Engl. "single sided deafness) ist inzwischen ebenfalls an vielen Kliniken etabliert und in Studien seit 2016 auch nach internationalem Konsens analysiert[13]. Patienten mit einem normalhörenden Ohr und einem, das mit einem CI versorgt ist, werden kurz als CI-SSD bezeichnet.
Bimodale Versorgung
Eine weitere Möglichkeit der Versorgung ist die bimodale CI-Versorgung. Hierbei wird auf einem Ohr ein Hörgerät und auf dem anderen ein Cochlea-Implantat genutzt. Die Geräte können dabei nicht direkt gekoppelt, aber je nach Hersteller mit möglichst ähnlichen Einstellung versehen werden. Der Aspekt der unterschiedlich schnellen Verarbeitung zwischen den beiden Ohren wurde bspw. von Dillion festgestellt[14]. Unter anderen konnten die 2019 erlangten Erkenntnisse zum genauereren Richtungshören durch einen Ausgleich dieser s.g. Laufzeitdifferenzen zwischen den beiden Ohren[15] den Fokus auf die Notwendigkeit der bimodalen Anpassung gelegt.
Vertreter von Gehörlosenkultur
Die Implantation wird von einem Teil der Menschen abgelehnt, die sich der Gehörlosenkultur zugehörig oder verbunden fühlen. Harlan L. Lane bezeichnete die Befürworter des CI sogar als audistisch. Er betrachtete Gehörlose nicht als Behinderte, sondern als Mitglieder einer ethnischen Gruppe.[16]
Ähnliche Techniken
- Hirnstamm-Implantat – Ein Implantat, bei dem statt des Innenohres ein Hör-Areal im Hirnstamm elektrisch erregt wird
- Elektrisch-akustische Stimulation – Eine Kombination aus Hörgeräte- und Cochlea-Implantat-Technologie
Literatur
Leitlinien
- S2k-Leitlinie Langfassung der Leitlinie "Cochlea-Implantat Versorgung" der Deutschen Gesellschaft für Hals-Nasen-Ohren-Heilkunde, Kopf- und Hals-Chirurgie. In: AWMF online (Stand 2020)
Übersichtsarbeiten
- M. L. Carlson, C. L. Driscoll, R. H. Gifford, S. O. McMenomey: Cochlear implantation: current and future device options. In: Otolaryngologic clinics of North America. Band 45, Nummer 1, Februar 2012, S. 221–248, ISSN 1557-8259. doi:10.1016/j.otc.2011.09.002. PMID 22115692. (Review).
- N. R. Peterson, D. B. Pisoni, R. T. Miyamoto: Cochlear implants and spoken language processing abilities: review and assessment of the literature. In: Restorative neurology and neuroscience. Band 28, Nummer 2, 2010, S. 237–250, ISSN 0922-6028. doi:10.3233/RNN-2010-0535. PMID 20404411. PMC 2947146 (freier Volltext). (Review).
- B. Mangus, A. Rivas, B. S. Tsai, D. S. Haynes, J. T. Roland: Surgical techniques in cochlear implants. In: Otolaryngologic clinics of North America. Band 45, Nummer 1, Februar 2012, S. 69–80, ISSN 1557-8259. doi:10.1016/j.otc.2011.08.017. PMID 22115682. (Review).
Sonstiges
- Elisabeth Calcagnini Stillhard: Das Cochlear-Implant. Eine Herausforderung für die Hörgeschädigtenpädagogik. Edition SZH/SPC, Luzern 1994, ISBN 3-908263-03-4.
- Julia Koch: Entdecker in der Welt der Töne. In: Der Spiegel. Nr. 13, 2005, S. 156 (online – mit aktuellen Zahlen).
- Sabine Müller, Ariana Zaracko: Haben gehörlose Kleinkinder ein Recht auf ein Cochlea-Implantat? In: Nervenheilkunde. 4, 2010, S. 244–248. (PDF)
- Marion Hermann-Röttgen (Hrsg.): Cochlea-Implantat. Ein Ratgeber für Betroffene und Therapeuten. Trias, 2009, ISBN 978-3-8304-3530-3.
Weblinks
- Deutsche Cochlea Implantat Gesellschaft: Webseite
- Deutscher Schwerhörigenverbund: Cochlea-Implantat
- CRE206 Das Ohr: Über das Hörsystem des Menschen und Cochlea-Implantate (Podcast von über 4 Stunden Länge vom 2. Juni 2014 mit Stefan Brill zu Gast bei Tim Pritlove): https://cre.fm/cre206-das-ohr
Einzelnachweise
- Mario Svirsky: Cochlea-Implantate und elektronisches Hören. Hrsg.: Physics Today, 70/8. 2017, ISSN 0031-9228, S. 52–58.
- Martin Douglas: Dr. William F. House, Erfinder des wegweisenden Ohrimplantats, stirbt mit 89. In: The New York Times. 15. Dezember 2012, abgerufen am 24. November 2020.
- A. Mudry, M. Mills: Die frühe Geschichte des Cochlea-Implantats: eine Retrospektive. Hrsg.: JAMA Otolaryngology - Head & Neck Surgery; 139/5. Mai 2013, S. 446–53.
- Gaeme/Clark: Das Mehrkanal-Cochlea-Implantat: vergangene, gegenwärtige und zukünftige Perspektiven Hrsg=Cochlea-Implantate International, 10/1. 2009, ISSN 1754-7628, S. 2–13.
- NASA: NASA-Raumstation. print of the US-government, 2003, abgerufen im Jahr 2015.
- Dietz, A., Wüstefeld, M., Niskanen, M., & Löppönen, H. (2016). Cochlear implant surgery in the elderly: the feasibility of a modified suprameatal approach under local anesthesia. Otology & Neurotology, 37(5), 487–491.
- MED-EL Fixation Clip - For Additional Electrode Stability https://s3.medel.com/pdf/FixationClip%20Factsheet.pdf
- Deutsche Cochlear Implant Gesellschaft e.V. (Memento des Originals vom 11. April 2014 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- https://www.nidcd.nih.gov/health/cochlear-implants [abgerufen am 29. November 2021]
- A. Kral, G. M. O'Donoghue: Profound deafness in childhood. In: New England J Med. 363, 2010, S. 1438–1450.
- Niparko u. a.: Spoken language development in children following cochlear implantation. In: JAMA. 303, 2010, S. 1498–1506.
- Müller, J. (1998). Erste Ergebnisse der Bilateralen Cochlear Implant Versorgung. European Archives of Oto Rhino Laryngology, 255, 38.
- Van de Heyning, P., Távora-Vieira, D., Mertens, G., Van Rompaey, V., Rajan, G. P., Müller, J., Hempel, J. M., Leander, D, Polterauer, D., Marx, M., Usami, S., Kitoh, R., Miyagawa, M., Moteki, H., Smilsky, K., Baumgartner, W. D., Keintzel, T. G., Sprinzl, G., Wolf-Magele, A., Arndt, S., Wesarg, T., Zirn, S., Baumann, U., Weissgerber, T., Rader, T., Hagen, R., Kurz, A., Rak, K., Stokroos, R. J., George, E. L. J., López, R. P., Medina-González, M. M., Henkin, Y., Hilly, O., Ulanovski, D., Rajeswaran, R., Kameswaran, M., Di Gregorio, M. F. & Zernotti, M. E. (2016). Towards a unified testing framework for single-sided deafness studies: a consensus paper. Audiology and Neurotology, 21(6), 391–398.
- Dillon H. Hearing aids. 2. ed. New York, Stuttgart: Thieme; 2012.
- Zirn, S., Angermeier, J., Arndt, S., Aschendorff, A., & Wesarg, T. (2019). Reducing the device delay mismatch can improve sound localization in bimodal cochlear implant/hearing-aid users. Trends in hearing, 23, 2331216519843876.
- Harlan L. Lane: The Mask of Benevolence: Disabling the Deaf Community. Neuauflage 2000. Dawn Sign Press. (dt.: Die Maske der Barmherzigkeit. Unterdrückung von Sprache und Kultur der Gehörlosengemeinschaft. Signum, Hamburg 1994)