Benzylisochinolin-Alkaloide
Die Benzyl(tetrahydro)isochinolin-Alkaloide sind Naturstoffe des Isochinolin-Alkaloid-Typs, die sich vom Benzylisochinolin ableiten.
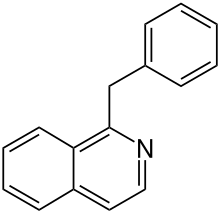


Vorkommen
Benzylisochinolin-Alkaloide werden u. a. in den Pflanzenfamilien der Mohngewächse, Annonengewächse und Lorbeergewächse gebildet.[1] Bekannte Vertreter kommen vor allem in Mohnpflanzen beziehungsweise dem daraus gewonnenen Opium vor, aber auch in Christophskräutern.[2] Das Reticulin wurde beispielsweise aus der Netzannone isoliert.[3]
Bekannte Vertreter
Von den Benzylisochinolin-Alkaloiden sind über 2500 biologisch aktive Derivate bekannt.[4] Aufgrund ihrer Struktur können die Substanzen in zahlreiche Untergruppen eingeteilt werden: die Aporphine, die Phthalidisochinolin-Alkaloide, die Morphinane, die Protoberberin-Alkaloide und die Pavine.[5]
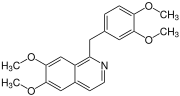
Zu den bekannten Einzelsubstanzen dieser Stoffgruppe gehört Papaverin. Weitere Vertreter sind u. a. die Benzyltetrahydroisochinolin-Alkaloide Reticulin und Laudanosin.[1]
Eigenschaften
Papaverin hat gefäßerweiternde und muskelentspannende Eigenschaften.[3] Laudanosin wirkt als tetanisches Gift.[1]
Biosynthese
Die Biosynthese der Benzylisochinolinalkaloide wurde intensiv untersucht. Sie beginnt mit der Aminosäure Tyrosin, die durch Hydroxylierung und Decarboxylierung in Dopamin beziehungsweise durch oxidative Desaminierung in 4-Hydroxyphenylacetaldehyd umgewandelt wird. Diese beiden Verbindungen werden in einer durch das Enzym Norcoclaurin-Synthase katalysierten Kondensationsreaktion zum Benzylisochinolin-Grundgerüst verbunden.[6]
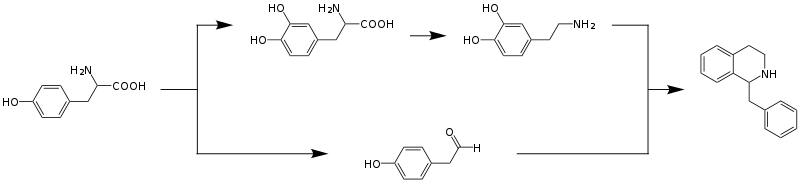
Das Benzylisochinolin aus dieser Reaktion kann über unterschiedliche Substituenten verfügen,[6] Reticulin ist eine wichtige Zwischenstufe.[5]
Einzelnachweise
- Eintrag zu Benzyl(tetrahydro)isochinolin-Alkaloide. In: Römpp Online. Georg Thieme Verlag, abgerufen am 22. Mai 2020.
- Hermann Hager: Hagers Handbuch der pharmazeutischen Praxis: Band 2: Methoden, 1133 Seiten, Verlag Springer (1991), ISBN 978-3-540-52459-5, S. 35 (eingeschränkte Vorschau in der Google-Buchsuche).
- Eberhard Breitmaier: Alkaloide. Springer Fachmedien, Wiesbaden 1997, ISBN 978-3-519-03542-8, S. 62.
- Bettina Ruff: Chemische und biochemische Methoden zur stereoselektiven Synthese von komplexen Naturstoffen, 199 Seiten, Verlag Logos Berlin (2012), ISBN 978-3-8325-3121-8, S. 8 (eingeschränkte Vorschau in der Google-Buchsuche).
- Jennifer M. Finefield, David H. Sherman, Martin Kreitman, Robert M. Williams: Enantiomere Naturstoffe: Vorkommen und Biogenese. In: Angewandte Chemie. 124, 2012, S. 4886–4920, doi:10.1002/ange.201107204.
- Yang-Chang Wu: New Research and Development on the Formosan Annonaceous Plants. In: Studies in Natural Products Chemistry. Band 33, 2007, S. 957–1023, doi:10.1016/s1572-5995(06)80044-x (englisch).
-Reticuline_Structural_Formula_V1.svg.png.webp)
-Laudanosine_Structural_Formula_V1.svg.png.webp)