Bariumbromat
Bariumbromat ist das Bariumsalz der Bromsäure mit der chemischen Zusammensetzung Ba(BrO3)2.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
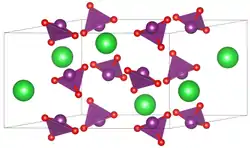 | ||||||||||||||||
| _ Ba2+ _ Br5+ _ O2− | ||||||||||||||||
| Kristallsystem |
monoklin | |||||||||||||||
| Raumgruppe |
C2/c (Nr. 15) | |||||||||||||||
| Gitterparameter | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Bariumbromat | |||||||||||||||
| Verhältnisformel | Ba(BrO3)2 | |||||||||||||||
| Kurzbeschreibung |
farb- und geruchloser Feststoff[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | ||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
3,99 g·cm−3 (Monohydrat)[3] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Herstellung
Bariumbromat kann durch Kochen einer wässrigen Lösung von Bariumchlorid oder Bariumacetat mit Kaliumbromat hergestellt werden.[5][6]
Eigenschaften
Bariumbromat kristallisiert isomorph zu α-Bariumiodat im monoklinen Kristallsystem in der Raumgruppe C2/c (Raumgruppen-Nr. 15) mit den Gitterparametern a = 1332 pm, b = 790 pm, c = 858 pm und β = 134,2° sowie vier Formeleinheiten in der Elementarzelle.[1] Die Löslichkeit in Wasser nimmt mit steigender Temperatur zu: in 1 Liter Wasser lösen sich bei 0 °C 2,86 g, bei 25 °C 7,88 g und bei 99,65 °C 53,9 g Bariumbromat.[3] Bariumbromat tritt üblicherweise als Monohydrat Ba(BrO3)2 · H2O auf, das bei 190 °C[7] sein Kristallwasser abgibt.[6] Dieses kristallisiert ebenfalls monoklin, Raumgruppe I2/c (Nr. 15, Stellung 8), Gitterparameter a = 907,0 pm, b = 789,5 pm, c = 963,0 pm und β = 93,26°.[8] Es ist auch ein Dihydrat bekannt (monoklin, Raumgruppe C2/c (Nr. 15), Gitterparameter a = 1043 pm, b = 719,5 pm, c = 837,5 pm, β = 113,6°).[9]
Beim Erhitzen auf 265 °C[7] zerfällt Bariumbromat in Bariumbromid und Sauerstoff.[5]
Die Lösungsenthalpie beträgt +54 kJ/mol, das Löslichkeitsprodukt 2,43 · 10−4 mol3/l3.[7]
Verwendung
Bariumbromat wird als Oxidationsmittel und als Korrosionsinhibitor verwendet.[3]
Einzelnachweise
- H. D. Lutz, E. Alici, T. Kellersohn, P. Kuske: Zur Polymorphie des Ba(BrO3)2 und Sr(IO3)2, Kristallstruktur, röntgenographische, schwingungsspektroskopische und thermoanalytische Untersuchungen. In: Zeitschrift für Naturforschung B. 45, 1990, S. 587–592 (PDF, freier Volltext).
- Eintrag zu Bariumbromat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2020. (JavaScript erforderlich)
- Dale L. Perry, Sidney L. Phillips: Handbook of inorganic compounds. CRC Press, 1995, ISBN 978-0-8493-8671-8, S. 47 (eingeschränkte Vorschau in der Google-Buchsuche).
- Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag barium salts, with the exception of barium sulphate, salts of 1-azo-2-hydroxynaphthalenyl aryl sulphonic acid, and of salts specified elsewhere in this Annex im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Leopold Gmelin, K. List: Handbuch der anorganischen Chemie, Band 2, 1853, S. 146. (eingeschränkte Vorschau in der Google-Buchsuche)
- R. Abegg, F. Auerbach: "Handbuch der anorganischen Chemie". Verlag S. Hirzel, Bd. 2, 1908. S. 270.Volltext
- Richard C. Ropp: Encyclopedia of the Alkaline Earth Compounds. Newnes, 2012, ISBN 0-444-59553-8, S. 94 (eingeschränkte Vorschau in der Google-Buchsuche).
- L.K. Templeton, D.H. Templeton: Structure of barium bromate monohydrate. In: Acta Crystallographica, C45, 1989, S. 672–673, doi:10.1107/S0108270188013071.
- H.D. Lutz, B. Engelen, C. Freiburg: Bariumbromiddihydrat. In: Acta Crystallographica, B36, 1980, S. 437–438, doi:10.1107/S0567740880003421.

