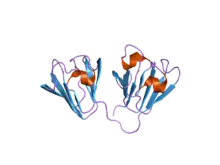
Affilin
Ein Affilin[1] ist ein künstliches Protein, das zur Bindung von Antigenen befähigt ist. Affiline sind strukturell vom menschlichen Ubiquitin oder von menschlichen Gamma-Kristallinen abgeleitet. Sie werden durch Veränderung ihrer oberflächennahen Aminosäuren gewonnen und mit Hilfe sogenannter Displaytechniken isoliert. Affiline besitzen sowohl Eigenschaften von Antikörpern als auch die von niedermolekularen Substanzen und werden daher als Antikörpermimetika bezeichnet. Affiline werden derzeit als mögliche neuartige biopharmazeutische Arzneistoffe untersucht und entwickelt.
Struktur
Als Grundgerüst für die Entwicklung von Affilinen wurden sowohl Gamma-Kristallin B als auch Ubiquitin beschrieben. Charakteristisch für beide Typen von Affilinen ist eine Bindungsregion innerhalb einer β-Faltblatt-Struktur. Sie unterscheiden sich somit von Antikörpern, deren Bindungsregion in flexiblen Schleifenregionen, den Complementarity Determining Regions (CDRs), lokalisiert ist.
Gamma-Kristallin-B-basierte Affiline
Gamma-Kristallin-B-basierte Affiline sind vom Augenlinsen-Strukturprotein Gamma-Kristallin B abgeleitet. Dieses Protein mit einer Molekülmasse von etwa 20 kDa besteht aus zwei strukturell identischen Proteindomänen mit β-Faltblatt-Struktur.[2] Die acht oberflächennahen Aminosäuren 2, 4, 6, 15, 17, 19, 36 und 38 können durch andere ausgetauscht werden.[3]
Ubiquitin-basierte Affiline
Ubiquitin-basierte Affiline sind von dem ubiquitär vorkommenden etwa 76 Aminosäuren langen Protein Ubiquitin abgeleitet. Dieses besteht aus dreieinhalb alpha-helikalen Windungen und einem aus fünf Strängen aufgebauten, antiparallelen β-Faltblatt.[4] Die oberflächennahen Aminosäuren 2, 4, 6, 62, 63, 64, 65 und 66 befinden sich in räumlicher Nähe zueinander am Beginn des ersten N-terminalen β-Faltblattstrangs, in der Schleife oder am Beginn des C-terminalen β-Faltblattstrangs und bilden mit ihren Seitenketten einen zusammenhängenden Bereich auf der Oberfläche des Ubiquitins. Diese Aminosäuren können in den etwa 10 kDa großen Ubiquitin-basierten Affilinen gegen andere ausgetauscht sein.[5]
Eigenschaften
Affiline besitzen eine etwa achtmal bzw. 16-mal kleinere Molekülmasse als Antikörper vom IgG-Typ. Basierend darauf besitzen sie eine gegenüber Antikörpern erhöhte Gewebepermeabilität. Andererseits ermöglicht die geringe Molekülmasse eine Ausscheidung über die Nieren und führt zu einer verkürzten Plasmahalbwertzeit. Ihre pH-Stabilität ermöglicht eine Darmpassage. Affiline sind zudem bis 90 °C temperaturstabil.
Herstellung
Die Herstellung von Affilinen gegen ein spezifisches Zielprotein umfasst mehrere Schritte. Ausgangspunkt ist die Generierung einer Affilin-Molekülbibliothek. Diese Affilinbibliothek wird durch Substitution der acht austauschbaren oberflächennahen Aminosäuren von Gamma-Kristallin B oder Ubiquitin mit Hilfe der zufälligen Mutagenese generiert. Bei Verwendung der proteinogenen Aminosäuren mit Ausnahme von Cystein kann die Bibliothek eine Komplexität von bis zu 17 Milliarden verschiedenen Molekülen erreichen. Bei einer Randomisierung von 14 Positionen in einem Affilindimer sind sogar etwa 1019 verschiedene Moleküle in einer Dimerbibliothek denkbar.
Nach der Generierung einer Affilinbibliothek werden aus dieser einzelne Affiline selektiert, welche das Zielprotein binden. Für die Selektion werden Displaytechniken, wie beispielsweise das Phagendisplay oder das Ribosomendisplay, eingesetzt. Die so selektierten Affiline werden isoliert und weiter biochemisch, pharmakologisch und biophysikalisch charakterisiert.
Nach einer Selektion von Affilinen können diese durch weitere Veränderungen optimiert werden. Eine Di- oder Multimerisierung kann dank des Aviditätseffekts eine Steigerung der Bindungsaffinität zum Zielmolekül und zugleich eine Verlängerung der Plasmahalbwertzeit bewirken. Weitere Optionen sind Konjugationen mit Radionukliden, Zytotoxinen oder Zytokinen.
Die großtechnische Herstellung von Affilinen kann mit Hilfe der in der Biotechnologie gebräuchlichen Produktionsorganismen, wie beispielsweise E. coli, erfolgen.
Literatur
- Hey T, Fiedler E, Rudolph R, Fiedler M: Artificial, non-antibody binding proteins for pharmaceutical and industrial applications. In: Trends Biotechnol.. 23, Nr. 10, Oktober 2005, S. 514–22. doi:10.1016/j.tibtech.2005.07.007. PMID 16054718.
- Ebersbach H, Fiedler E, Scheuermann T, et al.: Affilin-novel binding molecules based on human gamma-B-crystallin, an all beta-sheet protein. In: J. Mol. Biol.. 372, Nr. 1, September 2007, S. 172–85. doi:10.1016/j.jmb.2007.06.045. PMID 17628592.
Einzelnachweise
- Markenregister
- Jaenicke R, Slingsby C: Lens crystallins and their microbial homologs: structure, stability, and function. In: Crit. Rev. Biochem. Mol. Biol.. 36, Nr. 5, 2001, S. 435–99. doi:10.1080/20014091074237. PMID 11724156.
- Patent WO0104144: Design von Beta-Faltblatt-Proteinen mit spezifischen Bindungseigenschaften. Angemeldet am 13. Juli 2000, veröffentlicht am 18. Januar 2001, Anmelder: Scil Proteins GmbH., Erfinder: Fiedler U., Rudolph R..
- Vijay-Kumar S, Bugg CE, Cook WJ: Structure of ubiquitin refined at 1.8 A resolution. In: J. Mol. Biol.. 194, Nr. 3, April 1987, S. 531–44. PMID 3041007.
- Patent WO2006040129: Proteinkonjugale zur Verwendung in Therapie, Diagnose und Chromatographie. Angemeldet am 11. Oktober 2005, veröffentlicht am 20. April 2006, Anmelder: Scil Proteins GmbH., Erfinder: Fiedler E., Ebersbach H., Hey T., Fiedler U..