1-Butyl-3-methylimidazoliumhexafluorophosphat
1-Butyl-3-methylimidazoliumhexafluorophosphat ist eine ionische Flüssigkeit (auch: ionic liquid oder Flüssigsalz), also ein Salz, dessen Schmelzpunkt unter 100 °C liegt.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
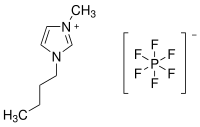 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 1-Butyl-3-methylimidazoliumhexafluorophosphat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C8H15F6N2P | ||||||||||||||||||
| Kurzbeschreibung |
farblos bis hellgelb[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 284,2 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
1,38 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Eigenschaften
Mit einem Schmelzpunkt von 12 °C handelt es sich bei 1-Butyl-3-methylimidazoliumhexafluorophosphat um eine Raumtemperatur-ionische Flüssigkeit (RTIL). Als polare, hydrophobe Flüssigkeit wird es, wie viele ionische Flüssigkeiten, als Lösungsmittel in der Synthese eingesetzt.
Darstellung
1-Butyl-3-methylimidazoliumhexafluorophosphat kann durch eine Anionenmetathese ausgehend von 1-Butyl-3-methylimidazoliumchlorid und einem Hexafluorophosphat-Salz gewonnen werden.[2]
Verwendung
Als Lösungsmittel kann 1-Butyl-3-methylimidazoliumhexafluorophosphat in einer Vielzahl von Reaktionen eingesetzt werden, wie zum Beispiel der Prins-Reaktion[3], der Synthese von Binaphtholen[4] und Heterocyclen.[5] Außerdem wird an der CO2-Speicherung[6] und elektrochemischen CO2-Reduktion[7] geforscht.
Einzelnachweise
- Datenblatt 1-Butyl-3-methyl-imidazolium-hexafluorphosphat (PDF) bei Carl Roth, abgerufen am 12. Februar 2021.
- J. Dupont, C. S. Consorti, P. A. Z. Suarez, R. F. de Souza: Prepartion of 1-Butyl-3-Methyl imidazolium-based room temperature ionic liquids In: Organic Syntheses. 79, 2002, S. 236, doi:10.15227/orgsyn.079.0236 (PDF).
- Poliane K. Batista, João Marcos G. de O. Ferreira, Fabio P. L. Silva, Mario L. A. A Vasconcellos, Juliana A. Vale: The Role Ionic Liquid [BMIM][PF6] in One-Pot Synthesis of Tetrahydropyran Rings through Tandem Barbier–Prins Reaction. In: Molecules. Band 24, Nr. 11, 31. Mai 2019, ISSN 1420-3049, S. 2084, doi:10.3390/molecules24112084, PMID 31159274, PMC 6600659 (freier Volltext).
- Jhillu S. Yadav, Basi V. S. Reddy, Kamakolanu Uma Gayathri, Attaluri R. Prasad: [Bmim]PF 6 /RuCl3 ·xH2O: a novel and recyclable catalytic system for the oxidative coupling of β-naphthols. In: New J. Chem. Band 27, Nr. 12, 2003, ISSN 1144-0546, S. 1684–1686, doi:10.1039/B307253N.
- Gurpreet Kaur, Aditi Sharma, Bubun Banerjee: [Bmim]PF6: An efficient tool for the synthesis of diverse bioactive heterocycles. In: Journal of the Serbian Chemical Society. Band 83, Nr. 10, 2018, ISSN 0352-5139, S. 1071–1097, doi:10.2298/JSC180103052K (nb.rs [abgerufen am 12. Februar 2021]).
- Álvaro Pérez-Salado Kamps, Dirk Tuma, Jianzhong Xia, Gerd Maurer: Solubility of CO 2 in the Ionic Liquid [bmim][PF6]. In: Journal of Chemical & Engineering Data. Band 48, Nr. 3, Mai 2003, ISSN 0021-9568, S. 746–749, doi:10.1021/je034023f.
- Yeonji Oh, Xile Hu: Ionic liquids enhance the electrochemical CO 2 reduction catalyzed by MoO 2. In: Chemical Communications. Band 51, Nr. 71, 2015, ISSN 1359-7345, S. 13698–13701, doi:10.1039/C5CC05263G.
