Thiopurin-Methyltransferase
Thiopurin-Methyltransferase (Syn.Thiopurin-S-Methyltransferase, Mercaptopurin-Methyltransferase, 6-Thiopurin-Transmethylase, TPMT) ist ein Enzym im Zytosol von Tieren, Pilzen und Bakterien, welches Thiopurine methyliert. Diese Reaktion ist Teil der Biotransformation körperfremder Stoffe und ein seltener Mangel des Enzyms führt beim Menschen dazu, dass Medikamente, die Thiopurine enthalten (6TG und Azathioprin), in normaler Dosis als Gift wirken.[2]
| Thiopurin-Methyltransferase | ||
|---|---|---|
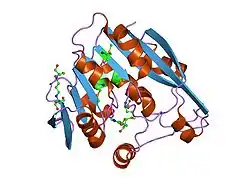 | ||
| Bändermodell der TPMT nach PDB 2bzg | ||
|
Vorhandene Strukturdaten: 1pjz, 2bzg, 2gb4, 2h11, 3bgd, 3bgi | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 245 Aminosäuren, 35 kD | |
| Sekundär- bis Quartärstruktur | Monomer | |
| Bezeichner | ||
| Gen-Name | TPMT | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 2.1.1.67, Methyltransferase | |
| Reaktionsart | Methylierung | |
| Substrat | S-Adenosylmethionin + Thiopurine | |
| Produkte | S-Adenosyl-L-Homocystein + Thiopurin-S-Methylether | |
| Vorkommen | ||
| Übergeordnetes Taxon | Bakterien, Tiere, Pilze[1] | |
Katalysierte Reaktion
S-Adenosylmethionin und Thiopurin werden in S-Adenosyl-L-Homocystein und Thiopurin-S-Methylether umgewandelt. Das Enzym wird durch S-Adenosyl-L-Homocystein gehemmt.[2]
Struktur
TPMT ist ein monomeres, aus einer Domäne bestehendes Protein mit 9-teiligem Kern (β-Faltblatt-Struktur) eingebettet in 2α-Helices. Das Ko-Produkt S-Adenosyl-Homocystein (SAH) bindet an verschiedene Areale (α1, α5, α6), sowie an der β-Faltblattstruktur 1 und 2. S-Adenosyl-Homocystein ist komplett durch die α1-Helix in das Enzym eingebunden, welche das Aktive Zentrum beinhaltet.
Funktion
Die Thiopurinmethyltransferase verstoffwechselt Azathioprin im Organismus. Wenn ein Mangel dieses Enzyms besteht, kann es durch Kumulation von Abbauprodukten des Azathioprins zu vermehrten Nebenwirkungen kommen.[3]
Nachweis
Die Thiopurin-Methyltransferase wird in einem radiochemischen Assay bestimmt.
Einzelnachweise
- Orthologe bei OMA
- UniProt P51580
- Fujita K, Sasaki Y: Pharmacogenomics in drug-metabolizing enzymes catalyzing anticancer drugs for personalized cancer chemotherapy. In: Curr. Drug Metab.. 8, Nr. 6, August 2007, S. 554–62. PMID 17691917.