Tandem-Reaktion
Tandem-Reaktion (auch Domino- oder Kaskaden-Reaktion, engl. Zipper-Reaction) ist ein Oberbegriff für eine intramolekulare Reaktionsfolge von oft hoch reaktiven, acyclischen Vorstufen zu komplexen, vielkernigen Molekülen. Damit sind Gesamtreaktionen gemeint, die eigentlich aus mehreren unabhängigen Reaktionsstufen (nicht mechanistischen Schritten) bestehen, die spontan unmittelbar nacheinander ablaufen. Man könnte sie auch einzeln nacheinander durchführen, um zum selben Produkt zu gelangen.
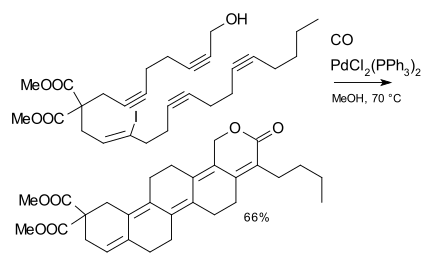
Das Edukt einer Tandem-Reaktion enthält in der Regel mehrere funktionelle Gruppen, die alle fast zeitgleich in einer Abfolge chemischer Reaktionen zu komplexen Zielmolekülen umgesetzt werden.
Der Vorteil der Tandem-Reaktion liegt in der Reaktionsgeschwindigkeit, die wegen des intramolekularen Charakters häufig hoch ist. Die Selektivität ist ebenfalls hoch, da Zwischenstufen selten isoliert werden müssen, kaum Nebenprodukte anfallen und physikalische Trennschritte minimiert werden können.
Die aktiven Reaktionszentren in Tandem-Reaktion sind vielfältig, z. B. aktive Doppel- oder Dreifachbindungszentren oder Epoxide.[1][2][3]
Eingesetzt werden können eine Vielfalt von Reaktionstypen, wie Diels-Alder-Reaktionen, Ringöffnungsreaktionen, Heck-Reaktionen.[4][5] oder Pauson-Khand-Reaktionen.[6]
Über Tandem-Reaktionen kann ein breites Spektrum von Zielmolekülen hergestellt werden, z. B. Polyether-Leiter-Polymere über Oxiran-Tandem-Reaktionen, Terpenoiden, Indoalkaloide und viele andere Naturstoffe.[7]
Einzelnachweise
- Barry M. Trost and Yian Shi: A Pd-Catalyzed Zipper Reaction. In: J. Am. Chem. Soc.. 113, 1991, S. 701–703. doi:10.1021/ja00002a064.
- M. M. Abelman and L. E. Overman: Palladium-catalyzed polyene cyclizations of dienyl aryl iodides. In: J. Am. Chem. Soc.. 110, Nr. 7, 1988, S. 2328–2329. doi:10.1021/ja00215a068.
- T. Sugihara, C. Coperet, Z. Owczarczyk, L. S. Harring and E.-i. Negishi: Deferred Carbonylative Esterification in the Pd-Catalyzed Cyclic Carbometalation-Carbonylation Cascade. In: J. Am. Chem. Soc.. 116, Nr. 17, 1994, S. 7923–7924. doi:10.1021/ja00096a070.
- Ronald Grigg and Visuvanathar Sridharan: Heterocycles via Pd catalysed molecular queuing processes. Relay switches and the maximisation of molecular com plexity. In: Pure Appl. Chem.. 70, Nr. 5, 1998, S. 1047–1057.
- Xiaomin Jin, Cook Group: Palladium Catalyzed Cyclization/Suzuki Coupling of 1,6-Enynes (Memento vom 20. September 2009 im Internet Archive) (11. Februar 2005).
- Nakcheol Jeong, Byung Ki Sung, Jin Sung Kim, Soon Bong Park, Sung Deok Seo, Jin Young Shin, Kyu Yeol In, and Yoon Kyung Choi: Pauson–Khand-type reaction mediated by Rh(I) catalysts. In: Pure Appl. Chem.. 74, Nr. 1, 2002, S. 85–91.
- Graham L. Simpson, Timothy P. Heffron, Estíbaliz Merino, and Timothy F. Jamison: Ladder Polyether Synthesis via Epoxide-Opening Cascades Using a Disappearing Directing Group. (Communication) In: J. Am. Chem. Soc.. 128, Nr. 4, 2006, S. 1056–1057. doi:10.1021/ja057973p.
Literatur
- Yifa Zhou: Enantioselektive Synthese der Indoalkaloide vom Vallesiachotamin- und Corynanthe-Typ durch Domino-Reaktion. Cuvillier, ISBN 3897124033
- Hans-Jürgen Gutke: Untersuchungen zur anionisch induzierten Domino-Reaktion – Bausteine für die Synthese von Terpenoiden. Shaker Verlag GmbH, ISBN 3826574648
- Palladium(II)-katalysierte Domino-Reaktionen zur enantioselektiven Synthese, von Florian Stecker (als Google-Book)