Pomeranz-Fritsch-Reaktion
Die Pomeranz-Fritsch-Reaktion, auch Pomeranz-Fritsch-Cyclisierung genannt, ist eine Namensreaktion der organischen Chemie und wurde 1893 unabhängig voneinander durch den deutschen Chemiker Paul Fritsch (1859–1913) und den österreichischen Chemiker Cäsar Pomeranz (1860–1926) entdeckt.[1][2] Es handelt sich hierbei um eine Reaktion zur Synthese von Isochinolin und dessen Derivaten.[2][3][4]
Übersichtsreaktion
Bei der klassischen Pomeranz-Fritsch-Reaktion wird Benzaldehyd unter Anwesenheit einer Säure mit einem 2,2-Dialkoxyethylamin zu Isochinolin umgesetzt.[5]

Bei der Reaktion können verschiedene Alkylgruppen für die Reste R verwendet werden, z. B. Methyl- und Ethylgruppen.[3]
In der Originalarbeit wurde konzentrierte Schwefelsäure als Protonenquelle verwendet.[1][2] Jedoch sind heute auch Varianten mit Lewissäuren bekannt. Durch die Verwendung verschiedener aromatischer Aldehyde bzw. Ketone können beliebig substituierte Isochinoline synthetisiert werden.[4]
Mechanismus
Ein möglicher Reaktionsmechanismus für die Pomeranz-Fritsch-Reaktion sieht wie folgt aus:[5]
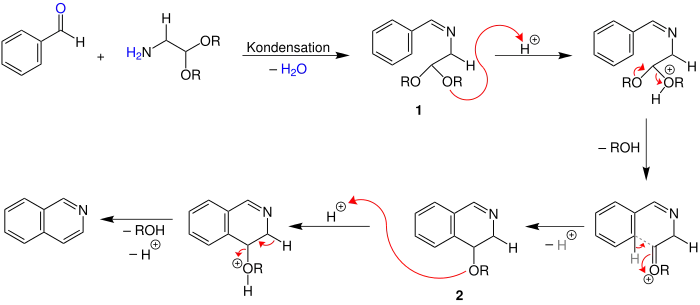
Werden Benzaldehyd und 2,2-Dialkoxyethylamin erhitzt kondensieren diese unter Wasserabspaltung zum Zwischenprodukt 1. Durch Säurezugabe wird eine der beiden Alkoxygruppen protoniert. Anschließend spaltet sich ein Alkohol ab. Unter Abspaltung eines Protons entsteht durch einen Ringschluss der Ether 2. Im nächsten Schritt wird die verbliebene Alkoxygruppe ebenfalls protoniert und abgespalten. Durch Rearomatisierung bildet sich unter Abgabe eines Protons Isochinolin.
Anwendung
Die Pomeranz-Fritsch-Reaktion besitzt zahlreiche Anwendung in der chemischen Industrie. Besonders für die direkte Isochinolin-Synthese stellt sie eine effektive Methode dar. Dabei ist Isochinolin ein wichtiges Zwischenprodukt für die Synthese verschiedener wichtiger Derivate.[3][4]
Diese werden auf verschiedenste Weise genutzt, beispielsweise als:
- Anästhetika wie Dimethisoquin.
- Blutdrucksenker wie Quinapril, Quinapirilat und Debrisoquine. Alles Derivate des 1,2,3,4-Tetrahydroisochinolins.
- Fungizide, wie 2,2'-Hexadecamethylenediisochinoliniumdichloride, das ebenso ein Antiseptikum ist.
- Desinfektionsmittel N-Laurylisochinoliniumbromide
- Vasodilatatoren, wie beispielsweise Papaverin
Zusätzlich werden Isochinolin-Derivate bei der Herstellung von Farbstoffe, Insektiziden, Antimykotika und Korrosionsinhibitoren verwendet.
Einzelnachweise
- C. Pomeranz: Über eine neue Isochinolinsynthese. In: Monatshefte für Chemie und verwandte Teile anderer Wissenschaften. Band 14, Nr. 1, Dezember 1893, S. 116–119, doi:10.1007/BF01517862.
- Paul Fritsch: Synthesen in der Isocumarin- und Isochinolinreihe. In: Berichte der deutschen chemischen Gesellschaft. Band 26, Nr. 1, 1893, S. 419–422, doi:10.1002/cber.18930260191.
- Zerong Wang: Comprehensive Organic Name Reactions and Reagents. John Wiley & Sons, New Jersey 2009, ISBN 978-0-471-70450-8, S. 2256–2259.
- László Kürti und Barbara Czakó.: Strategic Applications of Named Reactions in Organic Synthesis: Background and Detailed Mechanisms. Elsevier Academic Press, 2005, ISBN 978-0-12-429785-2, S. 358–359.
- Jie Jack Li: Name Reactions – A Collection of Detailed Reaction Mechanisms, Springer, 2006, ISBN 978-3-540-30030-4, S. 472–474.