Ostwald-Verfahren
Das Ostwald-Verfahren dient der großtechnischen Herstellung von Salpetersäure durch Oxidation von Ammoniak, welches vorzugsweise durch das Haber-Bosch-Verfahren gewonnen wird.

Geschichte
Es geht auf den deutsch-baltischen Chemiker Wilhelm Ostwald zurück, der 1902 das Patent auf das Verfahren erhielt.[1] Die grundlegende chemische Reaktion von Ammoniak mit Luft am Platinkontakt wurde jedoch bereits 1838 von Frédéric Kuhlmann patentiert.[2][3]
Verfahrensbeschreibung
Das Verfahren läuft in drei Teilschritten ab. Ein Ausgangsstoff ist mittels Haber-Bosch-Verfahren erzeugtes Ammoniakgas. Weitere Ausgangsstoffe sind Sauerstoff und Wasser.
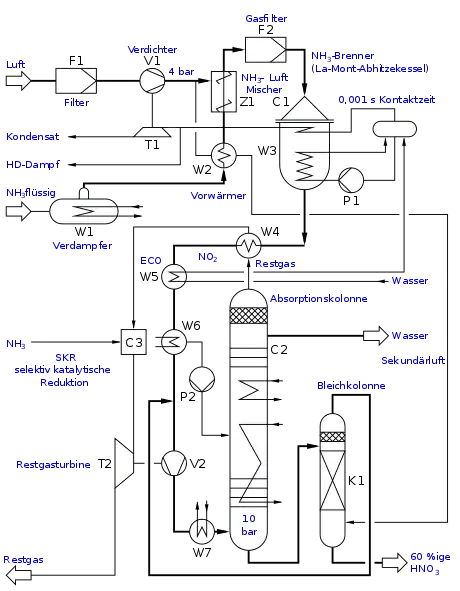
Heterogen katalysierte Verbrennung von Ammoniakgas
Im ersten Schritt wird Ammoniak (NH3) mit Sauerstoff (O2) gemischt und in Gegenwart eines Platin-Rhodium-Katalysators bei 800 °C bis 900 °C zu Wasser (H2O) und Stickstoffmonoxid (NO) umgesetzt (Bei neueren Anlagen wird ein spezielles Rückgewinnungsnetz eingesetzt, um das teure Platin zurückzugewinnen). Das Gasgemisch darf den Katalysator nur ganz kurz – nur etwa eine tausendstel Sekunde – berühren, da ansonsten das bei der Reaktionstemperatur instabile Stickstoffmonoxid in die Elemente N2 und O2 zerfällt.[4]
Eine unerwünschte Nebenreaktion, die auch ohne Katalysator abläuft, ist die Oxidation des Ammoniaks zu elementarem Stickstoff unter Bildung von Wasser:
Eine weitere unerwünschte Nebenreaktion ist die Bildung von Lachgas:
Die Nebenreaktionen werden nach dem Prinzip von Le Chatelier durch eine möglichst hohe Netztemperatur und niedrigen Druck zurückgedrängt.
Erzeugung von Stickstoffdioxid
In Schritt 2 senkt man die Temperatur des Stickstoffmonoxids (NO) auf unter 50 °C und mischt es mit Luft. Es läuft eine weitere Oxidation mit Sauerstoff (O2) zu Stickstoffdioxid (NO2) ab, welches anschließend zu Distickstofftetraoxid dimerisiert:
Reaktion in der Oxidations- und Absorptionskolonne
Die Stickoxide werden im dritten Schritt in Rieseltürmen mit Wasser zu Salpetersäure (HNO3) umgesetzt:
Als Zwischenprodukte entstehen hierbei Stickstoffmonoxid (NO) und die Salpetrige Säure (HNO2), denn die Reaktion verläuft über folgende Zwischenschritte:
- (wie Schritt 2)
Produkte
Die mit dem Ostwald-Verfahren gewonnene ca. 60-prozentige Salpetersäure kann nur auf 68,5 Prozent konzentriert werden, da diese Zusammensetzung dann ein Azeotrop mit einem Siedepunktmaximum von 122 °C ist. Eine höhere Konzentrierung kann in einer Gegenstromdehydratisierung mit Trocknungsmitteln wie Phosphorpentoxid oder Schwefelsäure erreicht werden.[5]
Literatur
- Frédéric Kuhlmann: Abhandlung über die Salpeterbildung. Neue Erzeugung von Salpetersäure und Ammoniak. In: Annalen der Pharmacie. Band 29, Nr. 1, 1839, ISSN 0365-5490, S. 272–279, doi:10.1002/jlac.18390290305.
- Erwin Riedel: Anorganische Chemie. 6. Auflage. de Gruyter, Berlin 2004, ISBN 3-11-018168-1.
Einzelnachweise
- Patent GB190200698: Improvements in the Manufacture of Nitric Acid and Nitrogen Oxides. Angemeldet am 9. Januar 1902, veröffentlicht am 20. März 1902, Erfinder: Wilhelm Ostwald.
- Patent FR11331: Pour la fabrication de l’acide nitrique et des nitrates. Veröffentlicht am 22. Dezember 1838, Erfinder: Frédéric Kuhlmann.
- J. Graham Smith: Frédéric Kuhlmann, pioneer of platinum as an industrial catalyst. In: Platinum Metals Review. Band 32, 1988, S. 84–90 (platinummetalsreview.com [PDF]).
- Prof. Dr. Nils Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 730.
- Charles E. Mortimer: Chemie. 10. überarbeitete Auflage. Thieme, Stuttgart 2010, ISBN 978-3-13-484310-1, S. 444.