Leucine
Als Leucine fasst man zunächst die vier isomeren Aminosäuren Leucin, Isoleucin, tert-Leucin und Norleucin zusammen. Im Vergleich mit den vier Butanolen kann man sie als butylsubstituierte Glycine auffassen; damit sind alle vier Varianten vertreten. Die Zahl der maximal möglichen aliphatischen Aminosäuren mit n Kohlenstoffatomen in der Seitenkette (ohne Berücksichtigung der Stereoisomere) ist gleich der Zahl der ternären Baumgraphen mit n Knoten. Das ergibt die Zahlenfolge 1 (für n = 0), 1, 1, 2, 4, 8, 17, …[1] Für n = 4 ergeben sich also 4 Möglichkeiten. Diese werden gerade durch die oben genannten Aminosäuren realisiert.
Leucin und Isoleucin gehören zu den proteinogenen Aminosäuren, d. h., sie sind Bausteine der Proteine von Lebewesen und über den genetischen Code kodiert.
Berücksichtigt man noch die Stereoisomerie, so sind noch 6 weitere Isomere hinzu zu rechnen: (a) D-Leucin, (b) D-Isoleucin, (c) L-allo-Isoleucin, (d) D-allo-Isoleucin, (e) D-tert-Leucin und (f) D-Norleucin. Sie werden jeweils unter den ihnen zugehörigen Aminosäureartikeln beschrieben.
| Leucine | ||||
| Name | L-Leucin | L-Isoleucin | L-tert-Leucin (Terleucin) | L-Norleucin |
| Andere Namen | 2-Amino-4-methylpentansäure, iso-Butylglycin |
2-Amino-3-methylpentansäure, sec-Butylglycin |
2-Amino-3,3-dimethylbutansäure, tert-Butylglycin |
2-Aminohexansäure, n-Butylglycin |
| Strukturformel | 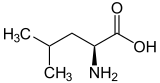 | 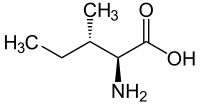 | 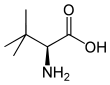 | 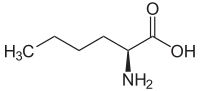 |
| CAS-Nummer | 61-90-5 | 73-32-5 | 20859-02-3 | 327-57-1 |
| PubChem | 6106 | 791 | 164608 | 21236 |
| Summenformel | C6H13NO2 | |||
| Molare Masse | 131,18 g·mol−1 | |||
Das Cycloleucin (1-Aminocyclopentan-1-carbonsäure) kann als cyclisches Derivat des Norleucins aufgefasst werden. Von diesem unterscheidet es sich u. a. durch eine um zwei Wasserstoffatome geringere Molmasse (129,16 g·mol−1). Bestimmendes Strukturelement ist ein Cyclopentanring. Das α-Kohlenstoffatom ist zudem kein Stereozentrum; Cycloleucin ist also nicht chiral.
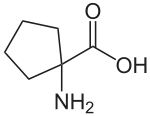 Strukturformel des Cycloleucins
Strukturformel des Cycloleucins
Siehe auch
Literatur
- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Biochemie. 6 Auflage, Spektrum Akademischer Verlag, Heidelberg 2007. ISBN 978-3-8274-1800-5.
- Donald Voet, Judith G. Voet: Biochemistry. 3. Auflage, John Wiley & Sons, New York 2004. ISBN 0-471-19350-X.
- Bruce Alberts, Alexander Johnson, Peter Walter, Julian Lewis, Martin Raff, Keith Roberts: Molecular Biology of the Cell, 5. Auflage, Taylor & Francis 2007, ISBN 978-0815341062.
Einzelnachweise
- K. Grützmann, S. Böcker, S. Schuster: Combinatorics of aliphatic amino acids, Naturwissenschaften 98 (2011) S. 79–86 (doi:10.1007/s00114-010-0743-2; PMID 21120449).