Kriebelmücken
Die Kriebelmücken (Simuliidae) sind eine Familie der Zweiflügler (Diptera) und gehören zu den Mücken (Nematocera). Weltweit leben etwa 2000 Arten dieser Tiergruppe, mehr als 50 Arten sind aus Deutschland bekannt. Es handelt sich dabei um meist kleine Mücken mit Körperlängen zwischen zwei und sechs Millimetern.
| Kriebelmücken | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|

eine Kriebelmücke, Weibchen | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Simuliidae | ||||||||||||
| Newman, 1834 |

Die Weibchen fast aller Kriebelmücken-Arten (97,6 Prozent der Arten)[1] sind obligate Blutsauger bei warmblütigen Wirtsarten, darunter auch dem Menschen.
Merkmale
Kriebelmücken[2][3] sind kleine Zweiflügler mit einer Körperlänge zwischen zwei und sechs Millimeter. Ihr Körperbau ist robust und gedrungen mit kurzen Beinen, sie ähneln daher im Habitus eher kleinen Fliegen. Sie sind in der Regel schwarz gefärbt (deshalb englisch „blackflies“), einige Arten besitzen aber eine gelbe bis orange Tönung oder ein silbrig helles Zeichnungsmuster.
Die Geschlechter lassen sich an der Ausbildung der Komplexaugen leicht erkennen: Bei den Männchen sind diese sehr groß, sie stoßen in der Kopfmitte in breiter Linie zusammen („holoptisch“), bei den Weibchen viel kleiner und breit durch die Stirn (Frons) voneinander getrennt. Zudem besitzen Männchen zwei Typen von Ommatidien; die der oberen (etwas größeren) Augenhälfte sind viel größer und meist heller gefärbt, mit ihrer Hilfe werden in den Paarungsschwärmen die Weibchen erkannt. Punktaugen (Ocellen) fehlen in beiden Geschlechtern. Die Antennen bestehen meist aus elf Segmenten (selten weniger), sie sind perlschnurartig (an den Gliedergrenzen eingeschnürt), kurz und meist zur Spitze hin verengt (konisch). Die Mundwerkzeuge bilden einen kurzen Saugrüssel, der nach unten weist. Auffällig sind die beiden verlängerten, viergliedrigen Unterkiefertaster, deren drittes Glied vergrößert ist, es trägt Sinnespapillen, die als Geschmacksorgane (Chemosensoren) dienen. Der Kopf ist kugelig, er ist meist schmaler, bei den Männchen manchmal genauso breit wie der Rumpfabschnitt.
Der Rumpf der Kriebelmücken ist kurz und hoch gewölbt, was den Tieren ein gebuckeltes Aussehen verleiht. Die glasklaren oder etwas rauchig getrübten, ungezeichneten Flügel sind breit und kurz, von abgerundet ovaler Form. Im Flügelgeäder kommen Queradern nur zur Flügelbasis hin vor. Die ersten drei Längsadern zum Flügelvorderrand hin (Costa, Subcosta und erster Radiusast) sind dunkel gefärbt, beborstet und deutlich stärker als die übrigen Adern. Die drei Beinpaare besitzen zapfenförmig verlängerte Hüften und fünf Fußglieder. Das letzte trägt zwei starke Krallen, die bei Arten, die an Vögeln saugen, an der Basis einen lappenartigen Fortsatz besitzen. Der langgestreckt ovale Hinterleib verengt sich zur Spitze hin etwas, er besitzt neun frei sichtbare Segmente. Die Kopulationsorgane der Männchen an ihrer Spitze sind für die Artbestimmung wichtig, da die Arten in ihrer Körpergestalt sehr ähnlich und sonst nur schwer unterscheidbar sind.
Saugrüssel und Saugakt
Beide Geschlechter der Kriebelmücken tragen einen kurzen Saugrüssel. Dieser wird nur von den Weibchen zum Blutsaugen eingesetzt. Der Rüssel der Männchen ist im Bau etwas vereinfacht. Beide Geschlechter saugen zur eigenen Ernährung Nektar aus Blüten, die Blutmahlzeit dient nur zur Bildung der Eigelege. Kriebelmücken sind Poolsauger; das bedeutet, sie reißen mit den Mundwerkzeugen eine kleine Wunde und saugen das aus verletzten Kapillaren austretende Blut auf, das sich in einer kleinen Blase unter der Haut ansammelt. Sie stechen also nicht, wie etwa die Stechmücken, direkt Blutgefäße an.
Der Stechrüssel[4] besteht aus dem Labrum, dem Hypopharynx, den Mandibeln und den Laciniae der Maxillen. Beim Stechakt werden zunächst das verlängert dreieckige Labrum und der Hypopharynx vorgeschoben und gegen die Haut gedrückt. Dort werden sie durch am Ende sitzende Zähne verankert. Anschließend wird mit den gezähnten Mandibeln in einer scherenartigen Bewegung ein Loch in die Haut geschnitten. Das Labrum wird in die Wunde vorgestreckt, deren Seitenränder durch die Laciniae abgestützt werden. Die gezähnten Laciniae dienen zusätzlich zur Verankerung, so dass beim Zug der Muskeln an ihnen der gesamte Rüssel in die Wunde hineingezogen wird. Der messerartige, gezähnte lange Hypopharynx unterstützt das Eindringen weiter. Zwischen Laciniae und Labrum ist ein Nahrungskanal ausgebildet, durch den das Blut eingesaugt wird. Gleichzeitig wird durch einen Speichelkanal zwischen Hypopharynx und Mandibeln Speichel abgegeben, der die Blutgerinnung unterdrückt.
Eine Blutmahlzeit einer weiblichen Kriebelmücke dauert einige Minuten. Oft kommt es zu einem mehr oder weniger langen Nachbluten. Der Stich kann sehr schmerzhaft sein, vor allem wenn Nerven getroffen werden; manchmal wird er aber erst bemerkt, wenn durch den abgegebenen Speichel Juckreiz einsetzt.
Lebensweise
Beide Geschlechter der Kriebelmücken sind Nektarsauger und fliegen entsprechend Pflanzen an, die große und offene Nektarien besitzen (etwa Weiden, Efeu oder Pastinak). Ausschließlich die Weibchen sind bei fast allen Arten zusätzlich Blutsauger an Vögeln und Säugetieren. Eine solche Blutmahlzeit ist notwendig zur Eientwicklung. Die Wirtsfindung geschieht sowohl durch eine Kohlendioxidspur (olfaktorisch) als auch optisch. Ist ein potentieller Wirt gefunden, wird zunächst ein Probebiss angesetzt; enthält die gefundene Flüssigkeit Adenosindiphosphat (ADP) oder Adenosintriphosphat (ATP), so setzt der Vollsaugvorgang ein. Dabei sind sowohl die Wirte als auch die Positionen des Saugvorgangs artspezifisch. So saugt Simulium equinum bevorzugt an den Ohrmuscheln von Pferden und anderen Großsäugern, Simulium erythrocephalum demgegenüber an der Bauchhaut der Tiere. Etwa 2,4 Prozent der Arten besitzen unterentwickelte Mundwerkzeuge und sind nicht mehr imstande, zu stechen; bei ihnen nehmen die Weibchen keine Nahrung mehr auf. Die Nährstoffe für das Eigelege werden hier bereits im Larvenstadium eingelagert (sog. autogene Arten).
Fortpflanzung
Die Kriebelmücken bilden zur Partnerfindung Schwärme in der Nähe größerer dunkler Gegenstände (z. B. bei Bäumen). Dabei darf der Wind nicht zu stark sein (maximal 10 m/s), und die Lichtstärke muss über 5000 Lux betragen. Es werden keine Mischschwärme aus verschiedenen Arten gebildet. Der Mechanismus zur Erkennung der Artgenossen ist jedoch bislang unbekannt. Die Weibchen werden beim Überfliegen dieser Schwärme von unten von einem Männchen angeflogen, die Begattung beginnt direkt anschließend in der Luft und wird am Boden fortgeführt. In der Geschlechtsöffnung des Weibchens hinterlässt das Männchen eine Spermatophore. Bei einigen Arten kommt Parthenogenese, eingeschlechtliche Fortpflanzung ohne männliche Befruchtung, vor.
Larvalentwicklung
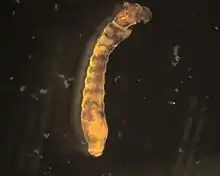

.png.webp)
Die Anzahl der Eier ist artspezifisch. Sie reicht von etwa 50 bei Prosimulium ursinum bis zu 1000 bei Simulium reptans pro Weibchen. Die Eier werden immer an oder in Fließgewässer abgegeben. Häufig geschieht dies durch Auftupfen auf die Wasseroberfläche. Simulium erythrocephalum legt die Eier an Wasserpflanzen in Höhe des Wasserspiegels, Simulium equinum taucht unter und legt die Eier auf der Unterseite von schwimmenden Blättern ab. Simulium morsitans wiederum legt die Eier an Pflanzenstängel oder in Erdspalten oberhalb der Wasserlinie ab. Die Gelege sind häufig von einer Gallertmasse umgeben, die zu Beginn der Entwicklung bis zu 68 % Wasser aufnimmt. Diese wasserhaltige Gallerte wirkt beim Trockenfallen der Eier als Austrocknungsschutz.
Die Larven der Kriebelmücken sind ausschließlich in Gewässern zu finden, wobei die artspezifischen Ansprüche an die Wasserqualität, die Fließgeschwindigkeit und an andere Faktoren sehr stark variieren. Einige Arten der Kriebelmückenlarven dienen dementsprechend als Leit- oder Monitororganismen zur Bestimmung der Wassergüte und Wasserqualität mittels des Saprobiensystems. So werden einige Arten der Gattung Simulium und Prosimulium als Zeigerarten für Gewässergüten im Bereich von I bis II betrachtet.
Kennzeichnend für die Larven der Kriebelmücken ist der unpaare und einziehbare Brustfuß (Scheinfüßchen) sowie der Hakenkranz am Hinterende der Larve. Beide sind mit mehreren Hundert Häkchen bewehrt, die radiär angeordnet sind. Mit Hilfe des hinteren Hakenkranzes sind die Larven an Pflanzenteilen, Steinen oder anderen Substraten in einem Gespinst aus sehr elastischer Seide befestigt, die durch Drüsen im Bereich der Mundwerkzeuge (Labialdrüsen) gebildet wird und mit dem Brustfüßchen abgenommen und auf dem Substrat aufgetragen wird. Der Körper wird aus dieser Position heraus frei in die Strömung gestellt. Eine Fortbewegung der Larven geschieht nach Art der Spannerraupen, durch Klettern an einem Faden oder einfach durch Verdriftung. Die Atmung erfolgt über die Haut, außerdem dienen Analpapillen zur Osmoregulation durch Ionenaufnahme.
Die meisten Kriebelmückenlarven besitzen zur Nahrungsaufnahme einen „Fangkescher“. Auf der Oberlippe stehen dabei zwei jeweils einen Haarfächer tragende ein- und ausklappbare Fortsätze. Diese sind von einem zähen Schleim überzogen in dem sich mit der Strömung treibende Nahrungspartikel (Detritus und Kleinstorganismen) verfangen. Zur Nahrungsaufnahme werden diese Fächer an den Mandibeln entlang gezogen, der Schleim bleibt in den Haarborsten oberhalb der Mandibeln hängen. Einige Kriebelmückenlarven haben keinen Fangkescher und ernähren sich durch Abweiden des Substrates.
Nach sechs bis neun Larvenstadien sind die Larven ausgewachsen und spinnen einen pantoffelförmigen Kokon, welcher auf dem Substrat befestigt wird. In diesem findet die Verpuppung statt. Das Vorderende des Kokons ist dabei offen und gegen die Strömung gerichtet. An dieser Stelle liegen die Spirakulumkiemen der Puppe. Die Form und die Anzahl der Lamellen auf dieser Atmungsstruktur ist artspezifisch verschieden, genauso wie die Form des Kokons, in dem die Puppe mit Häkchen des Hinterendes verhakt ist. Das Innere der in der Kieme enthaltenen Kiemenfäden ist über eine basale Öffnung wassergefüllt, die äußere Wand besteht aus zahlreichen senkrecht abstehenden, reich verzweigten Stützen. Das Hohlraumsystem zwischen den Stützen ist luftgefüllt und entnimmt dem umgebenden Wasser Sauerstoff durch Diffusion. Durch eine bislang noch weitgehend unbekannte Struktur steht es mit dem Tracheensystem in Verbindung und ermöglicht so der Puppe die Atmung.
Die Überwinterung erfolgt in Mitteleuropa in der Regel als Larve, in Nordeuropa als Ei. Letztere sind frostresistent und können unversehrt eingefroren werden. Die Verpuppung erfolgt erst nach Erreichen einer Schwellentemperatur, welche etwa bei den untersuchten Simulium-Arten bei circa vier Grad Celsius liegt. Dadurch kommt es zu einer zeitgleichen Puppenentwicklung sowie zu einer Synchronisation des Schlüpfens aus der Puppenhülle im Frühjahr. In Mitteleuropa werden eine bis sechs Generationen pro Jahr gebildet, in tropischen Tieflandflüssen können sich bis zu 16 Generationen pro Jahr bilden. Bei einigen Arten, wie etwa Simulium erythrocephalum, gibt es deutliche Unterschiede zwischen der ersten Generation im Frühjahr und späteren Generationen (Saisondimorphismus).
Schadwirkung bei Mensch und Nutztieren
Bei Kriebelmücken sind Arten zu unterscheiden, die Menschen und Tiere belästigen und solchen, die zu Gesundheitsschäden führen können, etwa als Vektoren von Krankheitserregern. Zusammengenommen handelt es sich bei Menschen und Haustieren um etwa 10 bis 20 Prozent der Arten.
Kriebelmücken als Plageerreger
Eine Reihe häufiger Kriebelmückenarten können durch ihr massenhaftes Auftreten sehr lästig werden. Neben zahlreichen Stichen können bereits die wolkenartig dicht in manchen Lebensräumen auftretenden Schwärme zu einer Belästigung führen, indem etwa zahlreiche Tiere in Mund und Nase eindringen und unbeabsichtigt in die Lungen inhaliert werden. In Europa zählen dazu die Arten Simulium truncatum, S. maculatum, S. posticatum, S. reptans, S. erythrocephalum und alle Arten von Simulium, Untergattung Wilhelmia.[5]
Bei einigen Arten wird auch der Mensch als Wirt angenommen. Der Biss ist häufig schmerzhaft und hat eine lokale Blutverdünnung sowie Blutergüsse zur Folge, da mit dem Speichel der Mücke Blutgerinnungshemmer in die Wunde gelangen. Außerdem wird beim Biss Histamin in der Wunde freigesetzt, was nicht selten zu pseudoallergischen Reaktionen führt. Symptome sind Quaddel- und Knötchenbildung bis hin zu ausgedehnten Erythemen und Ödemen, begleitet von anhaltendem Juckreiz, gelegentlich schmerzend. Durch unkontrolliertes Kratzen kann eine Lymphangitis ausgelöst werden. Wiederholte Stiche führen zum Krankheitsbild der Simuliose (auch „black fly fever“) mit Kopfschmerz, Schüttelfrost, Übelkeit und Brechreiz, Anschwellung und Weichheit der Lymphknoten, akut schmerzenden Gelenken und Mattigkeit.[5]
Beim Weidevieh kommt es nach häufigen Stichen gelegentlich zum Krankheitsbild der Simuliotoxikose durch eine überempfindliche Reaktion auf die im Speichel der Mücken enthaltenen Toxine. Schlimmstenfalls droht eine Blutvergiftung (Toxämie).
Bei Massenbefall können Kriebelmücken so den Tod von Weidetieren herbeiführen. Neben Herz-Kreislauf-Versagen und massiven Hautirritationen kommen die Tiere besonders infolge der durch die Parasiten verursachten Panik und damit verbundenen unkontrollierten Flucht zu Schaden. Vorbeugend werden daher an Sammelplätzen Insektizide eingesetzt. Besonders berüchtigt ist die Kolumbatscher oder Golubatzer Mücke (Simulium colombaschense) in den Donauländern auf dem Balkan. Über diese Art kann man in Brehms Tierleben (1920) lesen:
- „Die berüchtigtste europäische Gnitze ist die Kolumbatscher Mücke, so genannt nach den serbischen Dorfe Kolubazs, wo sie der Aberglaube der Bevölkerung aus einer Felshöhle entkommen läßt, in der vermeintlich Ritter St. Georg den Lindwurm erlegte.“
Ferner heißt es dort:
- „In den Gegenden der ganzen unteren Donau verbreiten sie Furcht und Schrecken bei Mensch und Vieh. Zu Tausenden und Abertausenden kriechen die kaum flohgroßen Gnitzen den Weidetieren, Pferden, Rindern und Schafen in Nase, Ohren und Maul stechen und saugen Blut, so daß die gemarterten Tiere wie tollwütig davonrasen und schließlich vor Erschöpfung tot zusammenbrechen.“ (Anmerkung: Gnitzen und Kriebelmücken wurden zu dieser Zeit noch zu einer Familie zusammengefasst)
Früher wurde die Art für bis zu 22.000 Todesfälle an Vieh pro Jahr im Donautal verantwortlich gemacht. Der letzte große Ausbruch, im Jahr 1950, verursachte etwa 800 tote Tiere. Seitdem sind die Schäden stark zurückgegangen. Möglicherweise ist die Art durch den Bau von Staudämmen an der Donau unbeabsichtigt verdrängt worden, weil sich die Strömungsverhältnisse veränderten. Die Art kommt in den früher am stärksten betroffenen Bereichen in der Donau heute nicht mehr vor.[6]
Kriebelmücken als Krankheitsüberträger
Vor allem im subtropischen und tropischen Afrika, aber auch in Südamerika sind Vertreter der Kriebelmücken außerdem Überträger des Fadenwurmes Onchocerca volvulus auf den Menschen. Dieser Wurm ist der Erreger der Onchozerkose (Flussblindheit), die bei etwa zehn Prozent der Erkrankten zur Erblindung führt. Bei den Krankheitsüberträgern handelt es sich ausschließlich um einige Vertreter der Gattung Simulium, etwa S. damnosum und S. neavei in Afrika und S. callidum und S. metallicum in Mittelamerika, ferner S. ochraceum in Mittel- und Südamerika. Auch andere Filariose-Erreger, etwa Mansonella ozzardi werden auf den Menschen übertragen, diese vor allem in den Regenwaldgebieten Süd- und Mittelamerikas.
Siehe auch: Parasiten des Menschen
Phylogenie
In der traditionellen Systematik, aufbauend auf die Arbeiten von Willi Hennig, bildeten die Simuliidae zusammen mit den Gnitzen (Ceratopogonidae), den Zuckmücken (Chironomidae) und den Dunkelmücken (Thaumaleidae) die Überfamilie der Chironomoidea innerhalb der Teilordnung der Culicomorpha. Neuere Untersuchungen, auf morphologischer[7] und genetischer[8][9] Basis haben diese Gruppierung nur teilweise unterstützt. Zwar erwiesen sich die Culicomorpha übereinstimmend als monophyletisch. Die Überfamilie der Chironomoidea konnte allerdings nicht aufrechterhalten werden. Den Ergebnissen zufolge sind die Zuckmücken, das namengebende Taxon, nicht dazugehörend, während die anderen drei Familien vermutlich eine natürliche Einheit bilden (von Borkent, als Überfamilie, Simulioidea benannt). Schwestergruppe der Simuliidae sind den Ergebnissen zufolge die Thaumaleidae. Beide Familien sind als Imagines in der Gestalt morphologisch ähnlich (relativ robuste, kurzbeinige Formen, Antennen kurz, bei den Männchen nicht modifiziert), sie weisen allerdings keine unzweideutigen morphologischen Synapomorphien auf und galten bei Untersuchungen auf morphologischer Basis meist nicht als zusammengehörig.
Systematik
Die Kriebelmücken lassen sich in zwei Unterfamilien einteilen, die hier mit den zugehörigen Gattungen aufgeführt sind. Eine der beiden, Simuliinae, lässt sich noch weiter in zwei Tribus untergliedern: Die Simuliini und die Prosimuliini. Die große und artenreiche Gattung Simulium wird von zahlreichen Autoren aufgespalten (Gattungen Eusimulium, Nevermannia, Wilhelmia, Boophthora usw.). Diese werden heute meist als Untergattungen aufgefasst. Die Familie ist morphologisch sowohl im Imaginal- wie im Larvalstadium so einheitlich, dass es nach Jensen[10] vertretbar wäre, alle Arten (mit Ausnahme der amerikanischen Gattung Parasimulium) in eine einzige Gattung zu stellen.
Familie Kriebelmücken (Simuliidae)
- Parasimuliinae
- Parasimulium
- Simuliinae
- Prosimuliini
- Araucnephia
- Arauchnephoides
- Archicnephia
- Baisomyia
- Cnephia
- Cnesia
- Cnesiamima
- Crozetia
- Ectemnia
- Gigantodax
- Greniera
- Gydarina
- Gymnopais
- Kovalevimyia
- Letvitinia
- Lutzsimulium
- Mayacnephia
- Metacnephia
- Paracnephia
- Paraustrosiumulium
- Pedrowygomyia
- Prosimulium
- Simulimima
- Stegopterna
- Sulcicnephia
- Tlalacomyia
- Twinnia
- Simuliini
- Austrosimulium
- Simulium
- Prosimuliini
Fossile Belege
Die älteste bekannte fossile Kriebelmücke stammt aus dem Mittleren Jura Zentralasiens[11]. Darüber hinaus wurden Kriebelmücken in verschiedenen Bernsteinvorkommen gefunden, sind aber rar. Aus Baltischem Bernstein sind mindestens fünf Arten der Gattung Simulium beschrieben, ferner liegen aus anderen tertiären Bernsteinlagerstätten Einzelfunde vor (Sizilianischer Bernstein und Dominikanischer Bernstein).[12][13] Besonders erwähnenswert ist der Fund einer weiblichen Kriebelmücke im Baltischen Bernstein, die sich mit einer Zuckmücke in copula befindet. Die Fühler der männlichen Zuckmücke waren offenbar von Nematoden befallen, so dass der erwählte Geschlechtspartner nicht mehr exakt erkannt werden konnte.[14]
Literatur
- Roger W. Crosskey: The natural history of blackflies. John Wiley & Sons, Chichester/New York/Brisbane/Toronto/Singapore 1990. ISBN 0-471-92755-4.
- Klaus Honomichl, Heiko Bellmann: Biologie und Ökologie der Insekten. CD-ROM. Gustav Fischer, Stuttgart 1994. ISBN 0-271-00417-7.
- Ke Chung Kim, Richard W. Merritt (Hrsg.): Black flies. Ecology, population management, and annotated world list. Pennsylvania State University Press, University Park/London 1987. ISBN 0-271-00417-7.
- Vincenz Kollar: Beurtheilung des von Dr. Medovics an die serbische Regierung erstatteten Berichtes über die Entstehung und Vertilgung der Gollubatzer Mücke (Simulia columbaschensis). In: SB. Akad. Wissensch., Wien 1848, S. 92–107.
- M. Laird (Hrsg.): Blackflies. Academic Press, London 1981. ISBN 0-12-434060-1
- G. Seitz: Verbreitung und Ökologie der Kriebelmücken (Diptera: Simuliidae) in Niederbayern. in: Lauterbornia. Mauch, Dinkelscherben 11.1992, 1–230.
- Tobias Timm: Dormanzformen bei Kriebelmücken unter besonderer Berücksichtigung des Ei-Stadiums (Diptera: Simuliidae). in: Entomologia generalis. Schweizerbart, Stuttgart 12.1987, 133–142. ISSN 0340-2266
- Tobias Timm: Unterschiede in Habitatselektion und Eibiologie bei sympatrischen Kriebelmückenarten (Diptera, Simuliidae). in: Mitteilungen der Deutschen Gesellschaft für Allgemeine und Angewandte Entomologie. Bremen 6.1988, 156–158. ISSN 0344-9084
- Tobias Timm, Walter Rühm (Hrsg.): Beiträge zur Taxonomie, Faunistik und Ökologie der Kriebelmücken in Mitteleuropa. Essener Ökologische Schriften. Bd. 2. Westarp Wissenschaften, Magdeburg 1993. ISBN 3-89432-078-8.
- W. Wichard, W. Arens, G. Eisenbeis: Atlas zur Biologie der Wasserinsekten. Stuttgart 1994. ISBN 3-437-30743-6.
- H. P. Wirtz: Analyse der Histaminanteile im Speichel verschiedener Kriebelmückenarten (Diptera: Simuliidae). in: Mitteilungen der Deutschen Gesellschaft für Allgemeine und Angewandte Entomologie. Bremen 6.1988, 441–442. ISSN 0344-9084
- W. Lechthaler, M. Car: Simuliidae − Key to Larvae and Pupae from Central− and Western Europe. Eutaxa-Eigenverlag, Wien 2005. ISBN 3-9501839-3-0.
Weblinks
Einzelnachweise
- Douglas C. Currie, Peter H. Adler: Global diversity of black flies (Diptera: Simuliidae) in freshwater. In: Hydrobiologia. 595, 2008, S. 469–475, doi:10.1007/s10750-007-9114-1.
- Ivan Antonovich Rubtsov: Blackflies (Simuliidae). Fauna of the USSR, Diptera, Vol.6 part 6. 1956, engl. Übersetzung B.R. Sharma. E.J. Brill, Leiden etc., 2nd edition 1990. ISBN 90 04 08871 7, Part 1 (Introduction, Morphology, External Anatomy).
- Peter H. Adler, John W. McCready: Black Flies (Simuliidae). Chapter 13 in Gary R. Mullen, Lance A. Durden (editors): Medical and Veterinary Entomology. Elsevier, Amsterdam etc., 2nd edition 2009. ISBN 978 0 12 372500 4.
- Harald W. Krenn, Horst Aspöck (2012): Form, function and evolution of the mouthparts of blood-feeding Arthropoda. Arthropod Structure & Development 41: 101-118. doi:10.1016/j.asd.2011.12.001
- Doreen Werner & Jörg Grunewald (2010): Kriebelmücken (Diptera, Simuliidae) und ihre Rolle als Krankheitsüberträger. In: Horst Aspöck (Hrsg.): Krank durch Arthropoden. Denisia 30: 233–243 (zobodat.at [PDF]).
- Peter H. Adler, Tatiana Kúdelová, Matúš Kúdela, Gunther Seitz, Aleksandra Ignjatović-Ćupina (2016): Cryptic Biodiversity and the Origins of Pest Status Revealed in the Macrogenome of Simulium colombaschense (Diptera: Simuliidae), History’s Most Destructive Black Fly. PLoS ONE 11(1): e0147673. doi:10.1371/journal.pone.0147673 (open access)
- Art Borkent (2012): The Pupae of the Biting Midges of the World (Diptera: Ceratopogonidae), With a Generic Key and Analysis of the Phylogenetic Relationships Between Genera. Zootaxa 3879 (1): 1–327. doi:10.11646/zootaxa.3879.1.1
- Sujatha Narayanan Kutty, Wing Hing Wong, Karen Meusemann, Rudolf Meier, Peter S. Cranston (2018): A phylogenomic analysis of Culicomorpha (Diptera) resolves the relationships among the eight constituent families. Systematic Entomology 43 (3): 434-446. doi:10.1111/syen.12285
- Xiao Zhang, Zehui Kang, Shuangmei Ding, Yuyu Wang, Chris Borkent, Toyohei Saigusa, Ding Yang (2019): Mitochondrial Genomes Provide Insights into the Phylogeny of Culicomorpha (Insecta: Diptera). International Journal of Molecular Science 20, 747 doi:10.3390/ijms20030747
- Frank Jensen: Diptera Simuliidae, Blackflies. In: Anders N. Nilsson (Hrsg.): Aquatic Insects of North Europe. Apollo Books, Stenstrup 1997.
- R. W. Crosskey: The Natural History of Blackflies. Chichester 1990, zitiert in Poinar 1992.
- George O. Poinar, Jr.: Life in Amber. Stanford University Press, Stanford, Cal. 1992, ISBN 0-8047-2001-0.
- Wolfgang Weitschat, Wilfried Wichard: Atlas der Pflanzen und Tiere im Baltischen Bernstein. Pfeil, München 1998, ISBN 3-931516-45-8.
- Friedhelm Eichmann: Aus dem Leben im Bernsteinwald. In: Arbeitskreis Paläontologie Hannover, Hannover 2003.