Fibrate
Fibrate sind eine Stoffgruppe, die sich chemisch-strukturell von der Fibrinsäure (2-Methyl-2-phenoxypropansäure) ableiten und medizinisch zur Behandlung hoher Blutfettwerte angewendet werden.
Wirkungsmechanismus
Fibrate bewirken eine Aktivitätssteigerung des Fettsäureabbaus in Peroxisomen durch Bindung an den intrazellulären PPARα. Dabei führt, ähnlich dem Mechanismus von Glukokortikoidrezeptoren, die Bindung der Fibrate an PPARα zur Dimerisierung des Rezeptors und anschließender Bindung an die DNA. Dies führt unter anderem zu einem erhöhten Abbau des LDL-Cholesterins. Zudem wird die VLDL-Synthese vermindert. Die Folge ist eine Abnahme des LDL-Cholesterins um 10–20 % und eine Zunahme des „guten“ HDL-Cholesterins um 5–10 %. Die Triglyceride sinken um 20–40 %.
Fibrate führen über eine PPARα-vermittelte Downregulation der Cholesterol-7α-Hydroxylase und Sterol-27-Hydroxylase zur vermehrten Sekretion von Cholesterol in die Galle und damit zu einem erhöhten Risiko für cholesterolhaltige Gallensteine.[1]
Anwendungsgebiete
Die Einnahme von Fibraten ist bei Hypercholesterinämie und Hypertriglyceridämie angezeigt, wobei die Wirkung auf die LDL-Cholesterol-Plasmaspiegel nur mäßig ist.[2]
Fibrate können nicht für den Routineeinsatz im Rahmen der kardiovaskuslären Prävention empfohlen werden, da eindeutige und konsistente Belege zum Langzeitnutzen, insbesondere auch mit Blick auf die Mortalität, nicht vorliegen. Ihre Gabe kommt in Frage, wenn Statine kontraindiziert sind, nicht vertragen werden oder die erwünschte Wirkung nicht allein mit einem Statin zu erreichen ist. Zur Behandlung der KHK gelten sie als Lipidsenker der zweiten Wahl, insbesondere wenn Statine nicht vertragen werden oder die Hypertriglyceridämie dominiert.[3][4]
Interaktionen und Nebenwirkungen
Bei gleichzeitiger Einnahme anderer Medikamente kann es zu Wechselwirkungen kommen. Ebenso kann es zu verstärkter Antikoagulation bei gleichzeitiger Einnahme oraler Antikoagulantien sowie zu einer verstärkten Blutzuckersenkung bei gleichzeitiger Einnahme oraler Antidiabetika und Insulin kommen. Auch besteht ein erhöhtes Risiko von Myopathien bei gleichzeitiger Einnahme von Statinen und Nikotinsäurederivaten.
Als Nebenwirkung besteht häufig eine Neigung der Bildung von Gallensteinen. Beschwerden des Gastrointestinaltraktes werden gleichsam beobachtet.
Vertreter
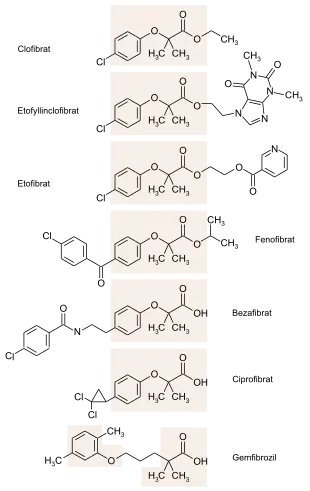
Die erste therapeutisch verwendete Substanz aus der Gruppe der Fibrate war Clofibrat, der Ethylester der Clofibrinsäure, die seither die Leitstruktur der Fibrate darstellt. Es wurde 1962 in den UK und 1967 in den USA im Markt als Lipidsenker (Atromid-S) eingeführt, in Deutschland 1964 als Skleromexe.[5] Clofibrat wurde breit zur Lipidsenkung eingesetzt und kam auch zum Einsatz in der ersten großen Studie, die den Zusammenhang zwischen Cholesterinsenkung und möglichen kardioprotektiven Effekten untersuchte. Diese Studie sowie auch Folgestudien zeigten nur einen begrenzten Nutzen für Clofibrat und führten, zusätzlich vor dem Hintergrund der ausgeprägten Nebenwirkungen, zur Entwicklung von Derivaten, die ein besseres Nutzen-Risiko-Verhältnis aufweisen sollten.[6] Es folgten Fenofibrat (1975, zum Beispiel Lipidil), Bezafibrat (1977, zum Beispiel Cedur), Gemfibrozil (1981, zum Beispiel Gevilon) und Ciprofibrat (1995, Lipanor). Ciprofibrat war in Deutschland nicht auf dem Markt, jedoch das Etofibrat (1974, Lipo-Merz[7]), dessen Anwendungsgebiete denen der anderen Fibrate entsprachen. Ein weiteres in Deutschland auf den Markt gebrachtes Fibrat war Etofyllinclofibrat (1981, Duolip[5]). Clofibrat selbst wurde in Deutschland mit Wirkung ab Januar 1979 als Medikament verboten.[8] Der Langzeitnutzen der Fibrate wurde über Jahre in Frage gestellt.[9][10][11] Im Oktober 2010 verkündete der Ausschuss für Humanarzneimittel (CHMP) der europäischen Arzneimittelagentur, eine Neubewertung von Nutzen und Risiken der vier Fibrate abgeschlossen zu haben. So bestünden keine speziellen Sicherheitsbedenken gegen die Fibrate, dennoch sollten sie nur als Mittel der zweiten Wahl eingesetzt werden, da ihre lipidsenkende Wirkung zwar gut belegt, ihr Langzeitnutzen im Hinblick auf „harte“ Endpunkte wie kardiovaskuläre Mortalität jedoch weniger gut dokumentiert sei als bei den Statinen.[12]
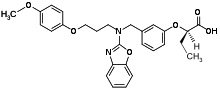
Ein Vertreter einer neuen Fibrat-Generation ist der selektive PPARα-Modulator (SPPARM) Pemafibrat, der in vitro eine hohe Spezifität für diesen Rezeptor zeigt. In Japan ist das Mittel unter dem Namen Parmodia seit 2017 zur Behandlung der Hyperlipidämie zugelassen.[13][14] In der PROMINENT-Studie wird untersucht, ob Patienten mit hohem Diabetes-Risiko und erhöhten Triglyceriden unter gleichzeitiger Statintherapie von Pemafibrat profitieren.[15]
Abbau
Clofibrat, Etofibrat und Etofyllinclofibrat werden im Körper zu Clofibrinsäure metabolisiert. Diese reichert sich wegen ihrer hohen mikrobiellen Persistenz und geringen Sorptionsfähigkeit im Grundwasser an.[16] Somit galt das Vorkommen von Clofibrinsäure als Anzeichen für eine mögliche Kontamination des Grundwassers allgemein mit Arzneimittel-Rückständen mit ähnlichen Stoffeigenschaften. Durch den Rückgang der therapeutischen Bedeutung der Fibrate verliert Clofibrinsäure in für Monitoring-Programme an Bedeutung, da der Eintrag in die Umwelt deutlich zurückgeht.[17]
Literatur
- Pharmakologie und Toxikologie 2006, Karow/Lang-Roth
- Medizinische Chemie 2005, Steinhilber/Schubert-Zsilavecz/Roth
Einzelnachweise
- S. M. Post, H. Duez, P. P. Gervois et al. Fibrates suppress bile acid synthesis via peroxisome proliferator-activated receptor-alpha-mediated downregulation of cholesterol 7alpha-hydroxylase and sterol 27-hydroxylase expression. Arterioscler Thromb Vasc Biol. 21(11), 2001, S. 1840–5.
- G. Geisslinger, S. Menzel, T. Gudermann, B. Hinz, P. Ruth: Mutschler Arzneimittelwirkungen. Pharmakologie – Klinische Pharmakologie – Toxikologie. Begründet von Ernst Mutschler, 11. Auflage. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2020, ISBN 978-3-8047-3663-4. S. 405.
- Arzneimittelkommission der deutschen Ärzteschaft: Handlungsleitlinie Fettstoffwechselstörungen, Mai 2012, abgerufen am 31. Januar 2014.
- Fenofibrate for dyslipidaemia (Memento des Originals vom 4. März 2016 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis., Rational Assessment of Drugs and Research, National Medicines Policy, Australia Februar 2006, abgerufen am 31. Januar 2014.
- Pharmaceutical Manufacturing Encyclopedia, 3. Auflage, William Andre Publishing, 2007, S. 1083, 1520.
- A. Gaw, C.J. Packard, J. Shepherd: Fibrates. In: Schettler G., Habenicht A.J.R. (eds) Principles and Treatment of Lipoprotein Disorders. Handbook of Experimental Pharmacology, Band 109, 1994. Springer, Berlin, Heidelberg. doi:10.1007/978-3-642-78426-2_12
- A. Kleemann, J. Engel et al.: Pharmaceutical Substances, 5th Edition, 2009: Syntheses, Patents and Applications of the most relevant APIs, Georg Thieme Verlag, 2014, Monografie „Etofibrat“.
- Tödliche Kosmetik. Nr. 52. In: Der Spiegel. 24. Dezember 1978.
- Restriktionen für Lipidsenker gefordert, arznei-telegramm, 1993.
- Umstrittene Arzneimittelarznei-telegramm, 1998.
- Fenofibrat bei Typ 2-Diabetikern: Herzinfarktrisiko nicht wie erwartet gesenkt, Deutsche Apothekerzeitung, Nr. 13, 2006.
- Europäische Arzneimittelagentur: Fibrates. 21. Oktober 2010, abgerufen am 15. Mai 2021.
- S. Yamashita, D. Masuda, Y. Matsuzawa: Pemafibrate, a New Selective PPARα Modulator: Drug Concept and Its Clinical Applications for Dyslipidemia and Metabolic Diseases. In: Current Atherosclerosis Reports. Band 22, 2020, doi:10.1007/s11883-020-0823-5.
- Pharmaceutical Evaluation Division, Pharmaceutical Safety and Environmental Health Bureau Ministry of Health, Labour and Welfare: Review report (Parmodia Tab. 0.1 mg ), 13. Juni 2017 (PDF; 672 kB).
- Eiichi Araki et al.: Effects of Pemafibrate, a Novel Selective PPARα Modulator, on Lipid and Glucose Metabolism in Patients With Type 2 Diabetes and Hypertriglyceridemia: A Randomized, Double-Blind, Placebo-Controlled, Phase 3 Trial. In: Diabetes Care. Band 41, 2018, doi:10.2337/dc17-1589.
- Traugott Scheytt, Susanne Grams, Holger Fell: Vorkommen und Verhalten eines Arzneimittels (Clofibrinsäure) im Grundwasser. In: Grundwasser. Band 3, Nr. 2, 1. Juni 1998, S. 67–77, doi:10.1007/s767-1998-8568-1.
- Arzneimittel in der Umwelt - Zu Risiken und Nebenwirkungen fragen Sie das Umweltbundesamt, Texte 29/05, Umweltbundesamt, 2005.