Europium(III)-hydroxid
Europium(III)-hydroxid ist eine anorganische chemische Verbindung des Europiums aus der Gruppe der Hydroxide.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
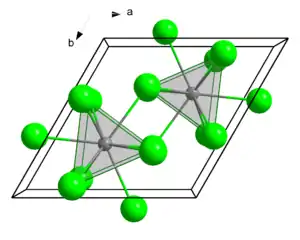 | ||||||||||||||||
| _ Eu3+ _ OH− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Europium(III)-hydroxid | |||||||||||||||
| Andere Namen |
Europiumtrihydroxid | |||||||||||||||
| Verhältnisformel | Eu(OH)3 | |||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 202,99 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Europium(III)-hydroxid kann durch Reaktion von Europium mit Wasser gewonnen werden. Es entsteht auch durch Zersetzung des instabilen Europium(II)-hydroxid Hydrates.[3]
Europium(III)-hydroxid kann auch durch Reaktion von Europium(III)-nitrat mit Hexamethylentetramin bei 95 °C oder Ammoniumhydroxid gewonnen werden.[4][5]
Eigenschaften
Europium(III)-hydroxid ist ein weißer Feststoff, der praktisch unlöslich in Wasser ist.[1] Er besitzt eine hexagonale Kristallstruktur mit der Raumgruppe P63/m (Raumgruppen-Nr. 176).[6] Bei Temperaturen zwischen 225 und 300 °C zersetzt sich die Verbindung zu Europiumoxidhydroxid EuOOH, welche sich bei Temperaturen über 425 °C zu Europium(III)-oxid zersetzt.[7]
Verwendung
Europium(III)-hydroxid wird als Phosphoraktivator für Farbkathodenstrahlröhren und Flüssigkristallanzeigen verwendet.[1]
Einzelnachweise
- metall.com.cn: Europium Hydroxide 99.9%-99.999% from Metall Rare Earth Limited, abgerufen am 2. Januar 2018
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Leroy Eyring: Progress in the Science and Technology of the Rare Earths. Elsevier, 2016, ISBN 978-1-4831-5777-1, S. 455 (eingeschränkte Vorschau in der Google-Buchsuche).
- Handbook on the Physics and Chemistry of Rare Earths. Elsevier, 2010, ISBN 978-0-444-53591-7, S. 330 (eingeschränkte Vorschau in der Google-Buchsuche).
- Ross J. Hunter, Victor R. Preedy: Nanomedicine and the Cardiovascular System. CRC Press, 2011, ISBN 978-1-4398-7989-4, S. 373 (eingeschränkte Vorschau in der Google-Buchsuche).
- D.F. Mullica, W.O. Milligan, G.W. Beall: Crystal structures of Pr(OH)3, Eu(OH)3 and Tm(OH)3. In: Journal of Inorganic and Nuclear Chemistry. 41, 1979, S. 525, doi:10.1016/0022-1902(79)80438-8.
- ROBERT C. RAU, W. J. GLOVER: Thermal Decomposition of Europium Hydroxide. In: Journal of the American Ceramic Society. 47, 1964, S. 382, doi:10.1111/j.1151-2916.1964.tb13836.x.