Cyclopropylgruppe
Als Cyclopropylgruppe wird in der Chemie ein Substituent bezeichnet, der sich von dem alicyclischen Kohlenwasserstoff Cyclopropan ableitet. Mit der Summenformel C3H5 ist er der kleinste Cycloalkyl-Substituent.
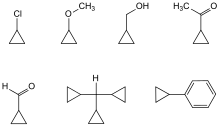
Eigenschaften
In der homologen Reihe der Cycloalkyl-Substituenten hebt sich die Cyclopropylgruppe durch besondere Eigenschaften ab, da sie die im Cyclopropan vorliegenden gebogenen Bindungen enthält. Ihr Charakter ähnelt der "ungesättigten" Vinylgruppe, sie kann mit benachbarten Doppelbindungssystemen (π-Elektronensystemen) als π-Donor in Konjugation treten. Dafür ist aber eine definierte räumliche Lage des Dreirings im Molekül (Konformation) nötig (siehe unten). Hinweise und starke Indizien lieferten spektroskopische Untersuchungen von cyclopropylsubstituierten Verbindungen, z. B. Cyclopropylbenzol oder Cyclopropancarbaldehyd, vor allem jedoch Cyclopropylmethyl-Derivaten, wenn daraus Carbokationen als Zwischenstufen gebildet werden.
Beispiele
Cyclopropylbenzol
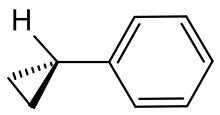
Dieser Kohlenwasserstoff besteht aus zwei starren Ringen, jedoch ist eine Rotation um die verknüpfende C-C-Bindung möglich. Für die Rotationsbarriere wurde durch eine NMR-Studie ein Wert um 2,0 kcal·mol−1 (8,4 kJ·mol−1) ermittelt.[1] Das Energieminimum entspricht einer Konformation, bei welcher die Ebene des Benzolrings (Phenylring) in der Projektion die gegenüberliegende C-C-Bindung des Cyclopropanrings (Atome C-2 und C-3) symmetrisch in zwei Hälften schneidet. Diese Konformation wurde im Englischen "bisected" genannt; das tertiäre Wasserstoffatom des Cyclopropylsubstituenten liegt dann in der vom Benzolring definierten Ebene.[2] Auf der Basis des Walsh-Modells hat man argumentiert, dass in dieser Anordnung die Wechselwirkung zwischen einem HOMO der Cyclopropylgruppe und einem LUMO des Phenylrings ein Maximum erreiche, und daher die Konjugation optimal sei. Mit diesem Modell können auch die unterschiedlichen C-C-Bindungslängen der Cyclopropylgruppe erklärt werden: Die beiden vicinalen Bindungen sind länger (151,4 pm) als die distale Bindung (150,7 pm).[2]
Cyclopropancarbaldehyd
Hier wurden zwei Energieminima identifiziert. Beide Konformationen sind "bisektisch", unterscheiden sich nur durch die Position des Carbonylsauerstoffatoms. Im einen Fall zeigt das O-Atom zum Dreiring hin, im anderen das H-Atom; beide Mal sollte die Konjugation optimal sein.[3]
Solvolyse von 4-Cyclopropylcumylchlorid
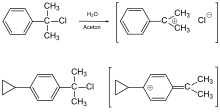
Bei der Reaktion von 2-Chlor-2-phenylpropan („Cumylchlorid“) mit Wasser, das zur Vermittlung besserer Löslichkeit mit Aceton vermischt wurde, entsteht unter Dissoziation des Chlorids ein Carbokation als reaktive Zwischenstufe. Ein Cyclopropylsubstituent in para-Stellung beschleunigt diese Hydrolyse („Solvolyse“) bei 25 °C um das über hundertfünfzigfache, im Gegensatz zum Cyclobutyl-, Cyclopentyl- und Cyclohexylrest, welche nur ca. zwanzigmal rascher reagieren.[4][5]
Cyclopropylmethyl-Verbindungen
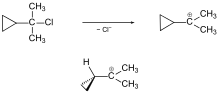
Die Solvolyse von 2-Cyclopropyl-2-chlorpropan erfolgt rascher als die des 2-Chlor-2-methylpropans (tert-Butylchlorid), bei dem das tert-Butylium-Ion als Intermediat auftritt.[6]
Im Falle der Cyclopropylverbindung entsteht ein Cyclopropylmethyl-Kation (früher auch Cyclopropylcarbinyl-Kation genannt). Dieses konnte in dem stark ionisierenden Medium SbF5-SO2ClF sogar durch NMR-Spektroskopie untersucht werden.[7]
Das persistenteste („stabilste“) bekannte Carbokation in dieser Reihe ist das Tricyclopropylmethyl-Kation.[8][9]

Literatur
- Zvi Rappoport (Hrsg.), The Chemistry of the Cyclopropyl Group, Band 1, Wiley, Chichester u. a. O., 1987. Band 2, Wiley, Chichester 1995. ISBN 0-471-94074-7
Einzelnachweise
- William J. E. Parr, Ted Schaefer: A proton magnetic resonance investigation of the preferred conformation and the barrier to internal rotation of phenylcyclopropane. In: J. Amer. Chem. Soc., 99 (4), S. 1033–1035. (1977), doi:10.1021/ja00446a010.
- Quang Shen, Christopher Wells, Marit Traetteberg, Robert K. Bohn, Amanda Willis, Joseph Knee: Molecular Structure and Conformation of Cyclopropylbenzene As Determined by ab Initio Molecular Orbital Calculations, Pulsed-Jet Fourier Transform Microwave Spectroscopic, and Gas-Phase Electron Diffraction Investigations. In: J. Org. Chem. 66 (17), S. 5840–5845 (2001), doi:10.1021/jo010293u.
- H. N. Volltrauer, R. H. Schwendeman: Microwave Spectra, Dipole Moments, and Torsional Potential Constants of cis‐ and trans‐Cyclopropanecarboxaldehyde. In: J. Chem. Phys. 54 (1971), S. 260, doi:10.1063/1.1674602.
- H. C. Brown, J. D. Cleveland, J. Org. Chem. 41, S. 1792 (1976).
- H. C. Brown, B. G. Gnedin, K. Takeuchi, E. N. Peters, JACS 97, S. 610 (1975).
- D. P. Kelly, H. C. Brown, JACS 97, S. 3879 (1975).
- G. A. Olah, C. L. Jeuell, D. P. Kelly, R. D. Porter, JACS 94, S. 146 (1972).
- Norman C. Deno, Herman G. Richey, Jane S. Liu, James D. Hodge, John J. Houser, Max J. Wisotsky. Physical Properties of the Tricyclopropylmethyl Cation In: Journal of the American Chemical Society 84, S. 2016–2017 (1962).
- Harold Hart, Paul A. Law. The Solvolysis of Tricyclopropylcarbinyl Benzoate, In: Journal of the American Chemical Society 86, S. 1957–1959 (1964).
