Azeotroprektifikation
Die Azeotroprektifikation, auch Schleppmittelverfahren genannt, ist ein chemisch-technisches Trennverfahren zur Gewinnung reiner Stoffe aus azeotropen Gemischen.
Prinzip
Bei der Azeotroprektifikation wird dem azeotropen Gemisch ein Schleppmittel zugesetzt, das ein ternäres leichtsiedendes Heteroazeotrop bildet. Das Heteroazeotrop wird dazu verwendet, eine Komponente aus einem binären Gemisch auszuschleppen. Ein Heteroazeotrop zeichnet sich dadurch aus, dass bei der Zusammensetzung des Azeotrops eine Mischungslücke in der flüssigen Phase auftritt. Die Flüssigkeit entmischt dabei in zwei Phasen mit unterschiedlicher Zusammensetzung. Diese Eigenschaft wird dazu verwendet, das Schleppmittel zurückzugewinnen.
Beispiel Ethanol-Absolutierung
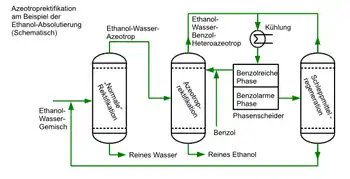
Im Falle der Ethanol-Absolutierung werden vier wesentliche Prozessschritte vorgenommen:[1][2]
- Rektifikation des Ethanol/Wasser-Gemischs. Dieser erste Schritt liefert bereits reines Wasser (Siedetemperatur 100 °C) am Sumpf der Kolonne, jedoch ein azeotropes Gemisch von etwa 96 Mol-% Ethanol und 4 Mol-% Wasser (Siedetemperatur 78,15 °C) am Kolonnenkopf (bei Normaldruck). Eine höhere Anreicherung lässt sich über eine Rektifikation nicht mehr erreichen.
- Das azeotrope Gemisch wird in eine zweite Trennkolonne gepumpt, in der zusätzlich ein Schleppmittel hinzugegeben wird. Als Schleppmittel wurde früher zumeist Benzol verwendet, heute jedoch werden Stoffe wie Cyclohexan und Toluol bevorzugt. Das Benzol bildet mit Wasser und Ethanol ein leichtsiedendes ternäres Azeotrop (Siedepunkt ca. 65 °C, Zusammensetzung ca. 22,8 Mol-% Ethanol, 53,8 Mol-% Benzol und 23,4 Mol-% Wasser)[3], das über den Kopf der Kolonne abgezogen werden kann. Mit Cyclohexan als Schleppmittel ist die Zusammensetzung etwa 7 Mol-% Wasser, 17 Mol-% Ethanol und 76 Mol-% Cyclohexan bei einem Siedepunkt von 63,4 °C. Über Kopf wird damit das gesamte restliche Wasser abgedampft. Obwohl damit über Kopf auch Ethanol abgezogen wird, kann im Sumpf reines Ethanol (ca. 99,7 Mol-%, Siedetemperatur 78,3 °C) abgezogen werden, da es bereits in großem Überschuss in diese Kolonne eingespeist wurde.
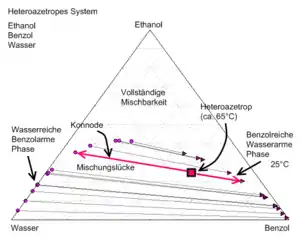
- Das ternäre Gemisch wird kondensiert und zerfällt dabei in zwei Phasen, eine davon reich und eine arm an Benzol. In einem Phasenscheider (auch als Dekanter bezeichnet), werden die beiden Phasen getrennt. Die benzolreiche Phase (>80 Mol-%) wird der vorherigen Säule direkt wieder zugeführt.
- Die benzolarme und damit wasserreiche Phase wird in einer weiteren Kolonne aufgespalten. Am Sumpf dieser Regenerationskolonne kann ein Wasser-Ethanol-Gemisch abgezogen werden, das der ersten Säule wieder zugeführt wird. Am Kopf dieser Kolonne entsteht das ternäre Azeotrop, dass wieder dem Phasenabscheider zugeführt wird.
Bei diesem Prozess, wie bei allen Rektifikationsverfahren, kann kein hundertprozentig reines Produkt erreicht werden, da dies nur mit unendlich hohen Trennkolonnen möglich wäre. Daher wird zum einen kein Benzol mehr verwendet, da es cancerogen ist, zum anderen wird das hier erzeugte Ethanol außerdem noch mit anderen Verfahren weiter gereinigt.
Schleppmittelauswahl
Ein geeigneter Zusatzstoff wird heute zumeist durch Recherchen in Faktendatenbanken, die in wissenschaftlicher Literatur veröffentlichte experimentelle azeotrope Punkte enthalten, gesucht. Alternativ werden Vorhersageverfahren zur Berechnung der azeotropen Punkte und auch der Mischungslücke verwendet. Hierbei sind i. a. größere Abweichungen zu erwarten, die daher vor der großtechnischen Anwendung mit Messungen verifiziert werden.
Siehe auch
- Dortmunder Datenbank (Datenbank für experimentelle azeotrope Punkte)
Weblinks
- ChemgaPedia (Tutorial)
Literatur
- Manfred Baerns, Arno Behr, Axel Brehm, Jürgen Gmehling, Kai-Olaf Hinrichsen, Hanns Hofmann, Ulfert Onken, Regina Palkovits, Albert Renken: Technische Chemie. John Wiley & Sons, 2014, ISBN 978-3-527-67409-1, S. 323 (eingeschränkte Vorschau in der Google-Buchsuche).
- Klaus Schwetlick: Organikum. Wiley, 2009, ISBN 978-3-527-32292-3, S. 56 (eingeschränkte Vorschau in der Google-Buchsuche).
- Swietoslawski W., Karpinski B., C.R.Hebd.Seanc.Acad.Sci.Paris, 198, S. 2166–2167, 1934.