Adsorptionswasser
Das Adsorptionswasser beschreibt die Adsorption, d. h. Anlagerung, von Wasser an die Oberfläche von Bodenpartikeln, dabei bildet sich ein Film von Wassermolekülen. Die Wassermenge, die diesen Film bildet, ist nicht konstant, sondern abhängig von der Bodenwasserspannung. Die Wasseranlagerungen an den Grenzflächen der Bodenteilchen stehen in Zusammenhang bzw. Gleichgewichtszustand mit den Menisken des kapillar gebundenen Wassers. Kapillarwasser und Adsorptionwasser bilden zusammen das Haftwasser, das im Boden gegen die Schwerkraft gehalten wird.
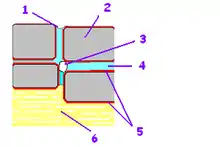
Adsorptionswasser und Bodenfeuchte
Bei einer hohen Bodenfeuchte im Bereich der Feldkapazität eines Bodens sind die Wasserfilme um die Bodenteilchen stärker ausgeprägt. Sind die Kapillaren im Porenvolumen eines Bodens dagegen weitgehend ausgetrocknet, werden die verbleibenden dünnen Schichten an Wassermolekülen sehr stark adsorbiert. Die erste Molekülschicht um die Bodenpartikel wird mit einer Bindungsdruck von 6×104 N·cm−2 (entsprechend einem pF-Wert von etwa 6,8) adsorbiert.
Auswirkung auf das Bodengefüge und Standfestigkeit
Bei Sandböden sind die spezifischen Oberflächen je Volumen Boden viel kleiner, als bei Böden mit feinerer Korngröße. Auch der strukturelle Aufbau der Tonminerale führt zu größeren Oberflächen bei Tonböden. Daher ist die Menge des Adsorptionswassers und die Auswirkung auf das Bodengefüge bei Sandböden nur gering, bei Lehmböden höher und bei Tonböden sehr hoch. Das Adsorptionswasser bewirkt eine Zunahme der Plastizität von Böden – mit negativen Folgen für die Standfestigkeit. Diese Eigenschaft ist nicht nur feuchte-, sondern auch druckabhängig. Bei einem hohen Druck lässt sich auch ein lufttrockener Tonboden plastisch verformen.
Ursache und Mechanismen
Die Wassermoleküle werden sowohl osmotisch wie auch als Dipole elektrostatisch an die Oberflächen der Minerale und Humuskolloide im Boden gebunden. Wasserstoffbrücken, Van-der-Waals-Kräfte und das Hydratationswasser vorhandener Kationentauscher stellen zusätzliche Bindungskräfte für das Wasser zur Verfügung. Dabei spielt die Wertigkeit der Bindungen dieser Ionen eine Rolle. In der Regel binden einwertige Ionen mehr Wasser, als zwei- oder dreiwertige Ionen. Besonders stark wirkt sich der Verlust von Kalium-Ionen bei Tonmineralen aus. Durch eine Strukturveränderung (Zuklappen) der Silikatschichten verringert sich die Oberfläche für die Wasseradsorption.
Eigenschaften des adsorbierten Wassers
Das adsorbierte Wasser gibt einen Teil der Bewegungsenergie als Benetzungswärme an die Umgebung ab. Die Wärmekapazität ist geringer, als die des freien Wassers; die Gefriertemperatur wird in einem feinkörnigen Boden herabgesetzt. Auch die Dichte, Viskosität und der Dampfdruck werden durch die Adsorption beeinflusst.
Rückwirkungen auf den Boden
Die Adsorption von Wassermolekülen verändert die physikalischen Eigenschaften der Bodenpartikel. In der Tonfraktion des Bodens wird durch die Wasserdipole eine Peptisation (bei Abstoßungsbedingungen) bzw. Flockung oder Koagulation der Tonminerale bei überwiegenden Anziehungsbedingungen der Tonkolloide bewirkt. Quellungs- und Schrumpfungsvorgänge verändern die Wasserhaltefähigkeit des Bodens und führen schließlich zu einer Hysterese der Wasserspannungskurve.
Literatur
- Karl Heinrich Hartge: Einführung in die Bodenphysik. Stuttgart 1978, ISBN 3-432-89681-6, S. 94–96.