Von-Braun-Reaktion
Die Von-Braun-Reaktion ist eine Namensreaktion der organischen Chemie. Sie wurde nach ihrem Entdecker, dem deutschen Chemiker Julius von Braun (1875–1939), benannt. Im Unterschied zum Von-Braun-Abbau dient diese Reaktion der Synthese von substituierten Cyanamiden aus tertiären Aminen. Die gewonnenen Cynanamide können anschließend durch Hydrolyse in sekundäre Amine umgewandelt werden. Damit eignet sich die Von-Braun-Reaktion beispielsweise zur Gewinnung von sekundären aus tertiären Aminen.[1]
Übersichtsreaktion
Die Von-Braun-Reaktion wird zur Substitution einer der Alkyl- oder Arylgruppen eines tertiären Amins verwendet. Als neuer Substituent wird mittels Bromcyan eine Cyanogruppe eingeführt. Die folgende Reaktionsgleichung veranschaulicht dies am Beispiel der Reaktion von Trimethylamin zu Dimethylcyanamid:
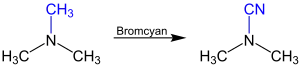
Reaktionsmechanismus
Im Folgenden soll ein möglicher Reaktionsmechanismus für die Von-Braun-Reaktion entsprechend der Übersichtsreaktion beschrieben werden:[2]

Zunächst reagiert das Trimethylamin mit dem Bromcyan unter Aufnahme einer Cyanogruppe. Dabei entsteht ein quartäres Ammoniumsalz, welches im nächsten Schritt durch Abspaltung von Brommethan zum Dimethylcyanamid reagiert. Es handelt sich hierbei um eine nukleophile Substitution zweiter Ordnung (SN2).
Beispielreaktion
Das folgende Reaktionsschema zeigt ein Beispiel für den Einsatz der Von-Braun-Reaktion zur Umwandlung eines tertiären in ein sekundäres Amin. Bei dem Produkt der Reaktion handelt es sich um den Arzneistoff Fluoxetin, welcher als Antidepressivum eingesetzt wird:[2][3]
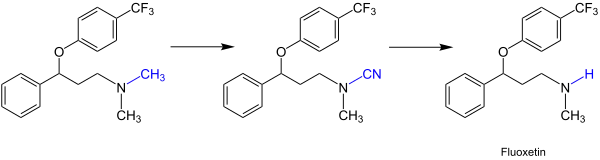
Atomökonomie
Da es sich bei dieser Reaktion um eine Substitutionsreaktion handelt, ist eine hundertprozentige Atomeffizienz ausgeschlossen. Es ist zu bedenken, dass bei der Von-Braun-Reaktion Bromcyan in stöchiometrischen Mengen eingesetzt wird. Außerdem fällt ein Bromalkan ebenfalls in stöchiometrischen Mengen als Abfallstoff an. Die Atomökonomie dieser Reaktion ist dementsprechend umso größer, je kleiner die molekulare Masse der substituierten Alkylgruppe und je größer die molare Masse des eingesetzten tertiären Amins insgesamt ist.
Einzelnachweise
- Julius von Braun: Die Aufspaltung cyclischer Basen durch Bromcyan. In: Berichte der deutschen chemischen Gesellschaft. Band 40, Nr. 3, 1907, S. 3914–3933, doi:10.1002/cber.190704003198.
- Jie Jack Li: Name reactions: A collection of detailed mechanisms and synthetic applications. 5. edition Auflage. Springer, Cham 2014, ISBN 978-3-319-03979-4, S. 619, doi:10.1007/978-3-319-03979-4.
- Michael Freissmuth, Stefan Offermanns, Stefan Böhm: Pharmakologie & Toxikologie: Von den molekularen Grundlagen zur Pharmakotherapie. Springer, Berlin, Heidelberg 2012, ISBN 978-3-642-12353-5, S. 283–294.