Vakuumbiopsie
Die Vakuumbiopsie ist ein Verfahren zur Gewinnung einer Gewebeprobe aus krankheitsverdächtigen Körperregionen zum Zweck einer feingeweblichen (histologischen) Untersuchung. Dabei wird eine gefensterte Hohlnadel in das zu untersuchende Gewebe eingebracht. Das Gewebe wird mittels Vakuumsog in das Innere der Nadel befördert, wo es dann abgetrennt und herausgezogen wird. Zumeist wird die Vakuumbiopsie an der weiblichen Brust und der Prostata eingesetzt.
Die stereotaktisch gestützte Vakuumbiopsie der weiblichen Brust
| OPS-Codes[1] | |
|---|---|
| Vakuumbiopsie d. Mamma ohne Clip-Markierung | 1-494.31 |
| Vakuumbiopsie d. Mamma mit Clip-Markierung | 1-494.32 |
| Mammographie mehr als zwei Projektionen | 3-100.2 |
| Präparatradiographie | 3-100.3 |
Geschichte
Die stereotaktisch gestützte Vakuumbiopsie der Mamma wurde 1996 von Burbank und Parker erstmals beschrieben und in den USA eingesetzt. In Europa wurde die Methode erstmals 1997 von Heywang-Köbrunner an der Universität Halle eingesetzt und findet seither zunehmend Verbreitung.
Indikation zur Untersuchung
Die Indikation zur Vakuumbiopsie wird nach den BI-RADS-Kriterien (Breast Imaging Reporting and Data System) des American College of Radiology aufgrund einer Mammographie in zwei Ebenen gestellt.
- Die als wahrscheinlich gutartig eingestuften Läsionen (BI-RADS II und BI-RADS III) werden im Allgemeinen nicht feingeweblich untersucht, es sei denn, die Patientin hat ein entsprechendes Risikoprofil, eine gesteigerte Angst vor bösartigen Tumoren (Karzinophobie), oder es besteht eine Inkongruenz von Klinik und radiologischen Befunden.
- Befunde, die als BI-RADS IV (wahrscheinlich bösartig) eingestuft werden, sind vor einer Operation histologisch zu sichern.
- Befunde, die als BI-RADS V (mit großer Wahrscheinlichkeit bösartig) eingestuft werden, sollten zur Operationsplanung biopsiert werden.
- Frustrane Probengewinne mit anderen Biopsiemethoden sollten definitiv mit der Vakuumbiopsie abgeklärt werden.
- Es sind vorzugsweise Mikrokalzifikationen und solche Befunde zu untersuchen, die nicht mit anderen Biopsieverfahren abgeklärt werden können. (Leitlinie, S. 25)[2]
Kontraindikationen
Kontraindikation zur Durchführung einer Vakuumbiopsie sind:
- nicht ausreichende Blutgerinnung
- die Patientin kann nicht in Bauchlage untersucht werden
- Befund liegt nahe der Brustwarze oder der Haut
- flaue Verdichtungen auf der Mammographie (das digitale Stereotaxiesystem hat eine schlechtere Auflösung als die Mammographie, Befunde sind so u. U. nicht anpeilbar)
Technik der Vakuumbiopsie
Unter Lokalanästhesie wird die Patientin auf dem Fischer-Tisch in Bauchlage untersucht, wobei die betreffende Brust durch eine Lücke im Tisch frei nach unten hängt und in der gewünschten Ebene senkrecht zur Thoraxwand komprimiert wird.
Die Kompressions- und Einstichrichtung wird so gewählt, dass die Veränderung auf kürzest möglichem Weg erreicht wird; andererseits darf das spätere operative Vorgehen nicht gestört werden. Es wird dann die Veränderung im kleinen Feld des Stereotaxietisches eingestellt und mit einer geraden Aufnahme (parallel zur Kompressionsrichtung = 0°) sowie einer nach links und einer nach rechts verkippten Aufnahme (+15°; −15°) dargestellt.
Aus diesen Bildern kann mit Hilfe der gedrehten Aufnahmen trigonometrisch die genaue Tiefe der Läsion ermittelt werden. Einstichwinkel und -tiefe sind so berechnet, dass das Fenster der 11-G-Hohlnadel (entspricht 2,95 mm) genau an der Läsion platziert wird. Nach einer Hautinzision wird die Biopsienadel bis an die errechneten Koordinaten an die Läsion vorgeschoben. Durch digitale stereotaktische Zielaufnahmen wird die korrekte Position der Nadel am Befund überprüft. Dann wird die Biopsienadel so in die Läsion eingeschoben, dass die Läsion durchbohrt wird und auf Höhe des Entnahmefensters liegt. Die Biopsienadel besitzt zwei Lumina, an denen unabhängig voneinander je ein Vakuum erzeugt werden kann.
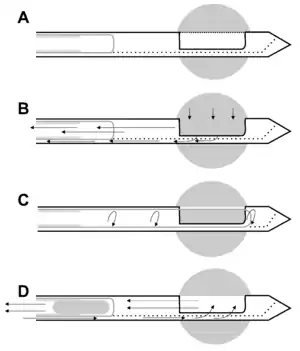
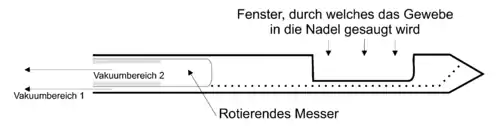
Im ersten Schritt wird das Biopsiefenster geöffnet, und ein Vakuumsog am Fenster der Nadel befördert das direkt anliegende Gewebe in das Innere der Nadel, wo es im zweiten Schritt von einem rotierenden Messer abgetrennt wird. Nun wird der Sog am Vakuumbereich 1 abgeschaltet, anschließend im dritten Schritt durch weiteren Sog im Vakuumbereich 2 und Herausziehen des Nadelkerns das abgeschnittene Biopsat zum hinteren Nadelende transportiert, wo es abgenommen wird. Dabei verbleibt die Nadel selbst in der Brust.
Nachdem der Nadelkern wieder zum Entnahmefenster fährt, kann die nächste Gewebsentnahme in gleicher Weise erfolgen. Durch schrittweises Drehen der Nadel um die eigene Achse (z. B. im Uhrzeigersinn) kann das Gewebe um die Nadel auf Höhe des Entnahmefensters quasi von innen abgetragen werden. Die Entnahme wiederholt sich für jede mögliche Position des Fensters, bis in bis zu 24 Vorgängen (Entnahme in zwei Runden jeweils bei jeder Uhrzeigerstunde) insgesamt bis zu 6 cm³ Gewebe in Zylinderform entfernt wurden.
Die korrekte Entnahme wird am Ende des Vorgangs durch stereotaktische Zielaufnahmen überprüft. Zur Ermittlung der korrekten und ggf. kompletten Entfernung des anvisierten Herdes erfolgt nach blutungsstillender Kompression der Brust und Verschluss der kleinen Hautwunde mit Pflaster eine Kontrollmammografie in zwei orthogonalen Ebenen sowie im Falle von Mikrokalk eine Präparatradiografie.
Die Gewebezylinder werden in Formalin fixiert und in Paraffin eingebettet. Davon werden mit einem Mikrotom dünne (5 µm) Schnitte angefertigt, gefärbt und von einem Facharzt für Pathologie unter dem Mikroskop beurteilt.
Weiteres Vorgehen in Abhängigkeit vom histologischen Ergebnis
Bei benigner Histologie wird eine mammografische Nachkontrolle entsprechend dem Standard nach 6 Monaten empfohlen.
Bei maligner (z. B. ductales Carcinoma in situ = DCIS oder invasives Karzinom) oder Borderline-Histologie (z. B. Lobuläres Karzinom in situ = lobuläres Karzinom in situ oder atypische duktale Hyperplasie = atypische duktale Hyperplasie – ADH) erfolgt immer eine Nachresektion des biopsierten Areals mit ausreichendem Sicherheitssaum. Das biopsierte Areal wird dabei üblicherweise präoperativ markiert. Die Markierung kann stereotaktisch erfolgen, wobei die zusätzliche exakte Dokumentation der Koordinaten bei Vakuumbiopsie hilfreich sein kann. Ist die Entnahmehöhle, was häufig der Fall ist, sonografisch erkennbar, kann die Markierung auch sonografisch gestützt durchgeführt werden. Wird bei Vakuumbiopsie eines kleinen Herdes zentral in einer großen Brust der gesamte Herd oder Mikrokalk entfernt, besteht zudem die Möglichkeit einer Clipmarkierung am Ende der Vakuumbiopsie. Die präoperative Drahtmarkierung kann sich am Clip orientieren.
Sicherheit der Vakuumbiopsie
Die Vakuumbiopsie hat eine Treffsicherheit (Sensitivität) von nahezu 100 % und eine Spezifität von ebenfalls nahezu 100 %. Es traten bisher keine wesentlichen Komplikationen auf, in manchen Fällen wurden Kreislaufreaktionen, Blutergüsse bis 5 cm oder übersteigertes Schmerzempfinden beobachtet. Sie besitzt für nicht-tastbare Befunde eine bessere Treffsicherheit als die Operation.
Der große Vorteil dieser Methode ist, dass nicht wie bei der Operation eine Vollnarkose nötig ist und dass keine sichtbaren Narben oder Gewebsdefekte entstehen. Zudem sind die Mammografien, die zur Kontrolle in den Folgejahren durchgeführt werden, nicht beeinträchtigt, da keine radiologisch relevante Narbenbildung auftritt.
Empfehlung
Laut aktuellen Brustkrebs-Leitlinien ist die stereotaktisch gestützte Vakuumbiopsie die Methode der Wahl zur Klärung suspekter, nicht-tastbarer Befunde der Mamma, die nicht mittels sonografischer Stanzbiopsie abgeklärt werden können. (Leitlinie, S. 25)[2]
Einzelnachweise
- Deutsches Institut für Medizinische Dokumentation und Information: ICD- und OPS-Klassifikation online (Memento des Originals vom 15. April 2008 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. Abgerufen: 12. April 2008
- Dt. Gesellschaft f. Senologie: S3-Leitlinie Brustkrebs Abgerufen: 12. April 2008
Literatur
- Heywang-Köbrunner, Schreer, Decker und Böcker: Interdisciplinary consensus on the use and technique of vacuum assisted stereotactic breast biopsy. In: European Journal of Radiology, 3(47):232-236, September 2003.
- Sylvia Helen Heywang-Köbrunner, Ingrid Schreer: Bildgebende Mammadiagnostik. Georg Thieme Verlag Stuttgart – New York, 1996. 2. Aufl. 2003
- Fred Burbank, Steve H. Parker und Thomas J. Fogarty: Stereotactic breast biopsy: Improved tissue harvesting with the mammotome. In: The American Surgeon, 62:738-744, 1996.
- Rotter, Haentschel, Koethe, Goetz, Bornhofen-Poschke, Lebrecht, Koelbl und Heywang-Koebrunner: Evaluation of mammographic and clinical follow-up after 755 stereotactic vacuum-assisted breast biopsies. In: The American Journal of Surgery, 2(186):134-142, August 2003.
- Nico Vondung: Einfluss von stereotaktischer Vakuumbiopsie versus primärer Operation auf das weitere Procedere bei Patientinnen mit Verdacht auf Brustkrebs. Dissertation, Universität Halle-Wittenberg 2008 (Dissertation online).