T5-Exonuklease
Die T5-Exonuklease (englisch T5 flap endonuclease) ist ein Enzym aus der Gruppe der Nukleasen (Exonukleasen) und wird vom Bakteriophagen T5 gebildet.
| T5-Exonuklease | ||
|---|---|---|
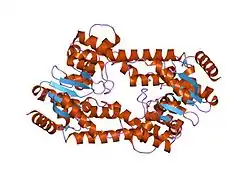 | ||
| C-terminale Domäne, nach PDB 1UT5 | ||
| Andere Namen |
5'-3' exonuclease, T5 flap endonuclease, Escherichia phage T5 Exonuclease, T5 D15 gene product | |
| Masse/Länge Primärstruktur | 291 Aminosäuren, 33.448 Da | |
| Bezeichner | ||
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 3.1.11.- | |
| Orthologe (Escherichia Phage T5) | ||
| Entrez | 2777611 | |
| UniProt | P06229
| |
| PubMed-Suche | 2777611 | |
Eigenschaften
Die T5-Exonuklease dient während der Infektion von Escherichia coli dem Bakteriophagen bei der DNA-Replikation des viralen Genoms. Sie katalysiert als Exonuklease die Hydrolyse der endständigen Nukleotide von DNA-Doppelsträngen mit blunt ends in 5'→3'-Richtung unter Freisetzung von Nukleosid-5'-Phosphat. Bei 5'-gabelnder DNA schneidet die T5-Exonuklease als Endonuklease an der Verbindung zwischen einzelsträngiger und doppelsträngiger DNA. Die einzelsträngige DNA muss dafür ein freies 5'-Ende aufweisen. Die T5-Exonuklease bindet DNA mit Pseudo-Y-Struktur mit einer Dissoziationskonstante von 5 nM−1.[1] Cofaktoren sind drei zweiwertige Magnesiumionen, wovon zwei für die Nukleaseaktivität notwendig sind.[2] Die Reaktion erfolgt auch mit anderen zweiwertigen Kationen außer Calciumionen.[3] Das pH-Optimum der Exonuklease liegt bei 9,3 und bei 5,5 für die Endonuklease.
Anwendungen
Die T5-Exonuklease wird in der Biochemie unter anderem zum Gibson Assembly eingesetzt.[4][5]
Weblinks
Einzelnachweise
- S. J. Garforth, T. A. Ceska, D. Suck, J. R. Sayers: Mutagenesis of conserved lysine residues in bacteriophage T5 5'-3' exonuclease suggests separate mechanisms of endo-and exonucleolytic cleavage. In: Proceedings of the National Academy of Sciences. Band 96, Nummer 1, Januar 1999, S. 38–43, PMID 9874768, PMC 15089 (freier Volltext).
- K. Syson, C. Tomlinson, B. R. Chapados, J. R. Sayers, J. A. Tainer, N. H. Williams, J. A. Grasby: Three metal ions participate in the reaction catalyzed by T5 flap endonuclease. In: The Journal of biological chemistry. Band 283, Nummer 42, Oktober 2008, S. 28741–28746, doi:10.1074/jbc.M801264200, PMID 18697748, PMC 2568906 (freier Volltext).
- S. J. Garforth, D. Patel, M. Feng, J. R. Sayers: Unusually wide co-factor tolerance in a metalloenzyme; divalent metal ions modulate endo-exonuclease activity in T5 exonuclease. In: Nucleic acids research. Band 29, Nummer 13, Juli 2001, S. 2772–2779, PMID 11433022, PMC 55779 (freier Volltext).
- R. M. Benoit, C. Ostermeier, M. Geiser, J. S. Li, H. Widmer, M. Auer: Seamless Insert-Plasmid Assembly at High Efficiency and Low Cost. In: PloS one. Band 11, Nummer 4, 2016, S. e0153158, doi:10.1371/journal.pone.0153158, PMID 27073895, PMC 4830597 (freier Volltext).
- D. G. Gibson: Enzymatic assembly of overlapping DNA fragments. In: Methods in enzymology. Band 498, 2011, S. 349–361, doi:10.1016/B978-0-12-385120-8.00015-2, PMID 21601685.