Strahlenbiologie
Die Strahlenbiologie (auch: Radiobiologie) untersucht die biologischen Wirkungen ionisierender Strahlung, das heißt von Alpha, Beta- und Gammastrahlen und Röntgenstrahlen auf Lebewesen. Neben der akuten Strahlenkrankheit (z. B. durch Unfälle mit Kernkraftwerken) sind vor allem chronische Wirkungen an Tumor- und Normalgeweben im Zusammenhang mit der Strahlentherapie Forschungsgegenstand.
Wirkung auf Zellen
Ionisierende Strahlen beeinflussen Körperzellen durch Ionisation und Anregung der Moleküle. Bedingt durch die viel höhere Konzentration sind nicht die wenigen direkten Treffer an den Makromolekülen, sondern weit überwiegend die Bildung von Radikalen des Gewebewassers von Bedeutung (Radiolyse). Die Radikale oxidieren wichtige zelluläre Makromoleküle und stören deren Funktion (indirekte Strahlenwirkung).
Dabei ist nur der im Gewebe absorbierte Anteil der eingestrahlten Energie wirksam. Eine Strahlung kann durch die Energiemenge, die ein Strahlungsteilchen pro Mikrometer abgibt, charakterisiert werden (Linearer Energietransfer LET, Einheit keV/μm). Beispielsweise hat Röntgenstrahlung einen LET von 2,5 keV/μm, schnelle Neutronen von >20 keV/μm. In der Strahlenbiologie wird stattdessen auch die relative biologische Wirksamkeit RBW verwendet, ein Faktor, der die Schädlichkeit einer Strahlung im Vergleich zu 250-kV-Röntgenstrahlen angibt. Im Strahlenschutz verwendet man statt der exakten RBW grob abgeschätzte, ganzzahlige Qualitätsfaktoren.
Strahlenschäden an Biomolekülen wie Proteinen und Lipiden können problemlos ertragen werden; ihre Auswirkungen auf die Zellfunktionen sind minimal. Dagegen führen Radikalreaktionen mit der DNA (Erbsubstanz) manchmal zum Zelltod oder zur Entartung, da jede Zelle nur über zwei Kopien verfügt und die Reparaturmechanismen begrenzte Kapazität haben. Die Chromosomen im Zellkern sind das Hauptziel der biologischen Strahlenwirkung. Pro Gray absorbierte Energie entstehen in jeder Zelle ca. 1000 Einzelstrang- und 40 Doppelstrangbrüche, die allerdings fast alle reparabel sind.
Folge von unreparierten DNA-Schäden sind Störungen der Zellfunktion, Mutation oder Tod der betroffenen Zelle. Die meisten Strahlenfolgen sind erst ab einer gewissen Mindestdosis nachweisbar, das heißt Strahlung in der Größenordnung der natürlichen Hintergrundstrahlung gilt in dieser Beziehung als ungefährlich. Da theoretisch eine einzelne mutierte Zelle zum Krebs heranwachsen oder eine embryonale Fehlbildung verursachen kann, gibt es für diese sogenannten stochastischen Strahlenschäden keine bekannte Mindestdosis. Man nimmt gegenwärtig eine lineare Dosis-Wirkungs-Beziehung an, für Röntgenstrahlung z. B. 5 % Krebstodesfälle pro Sievert; diese Angaben sind allerdings Gegenstand einer intensiven Debatte.
Neben der Mutation und dem Zelltod kommt es in Säugetierzellen nach Bestrahlung auch zu Verzögerungen des Zellzyklus, und zuvor unbegrenzt teilungsfähige Stammzellen und Krebszellen können nach Bestrahlung ausdifferenzieren und ihre Klonbildungsfunktion verlieren. Experimentelle Überlebenskurven erfassen neben dem direkten Zelltod auch diesen klonogenen Zelltod, der eine wichtige Rolle in der Strahlentherapie spielt. Sie haben immer eine charakteristische, S-förmige Gestalt, die mathematisch mit einer linear-quadratischen Modellfunktion beschrieben werden kann.
Wirkung im Gewebe

.jpg.webp)
Unterschiedliche Gewebe sind unterschiedlich strahlenempfindlich. Dazu tragen der Anteil an sich teilenden Zellen, die Durchblutung und die Sauerstoffkonzentration bei. Je niedriger der Sauerstoffpartialdruck im Gewebe, desto unempfindlicher ist es auf ionisierende Strahlen. Es wird daher in der Strahlentherapie empfohlen, das Rauchen einzustellen und eine eventuelle Blutarmut vor Beginn der Behandlung auszugleichen.
Auch die proliferative Organisation des Gewebes ist wichtig: wenn es eine streng abgegrenzte Stammzellfraktion besitzt, aus der abgestorbene Zellen ersetzt werden (sogenannte hierarchische oder Wechselgewebe wie z. B. Blutzellen oder Darmschleimhaut), dann wird einige Tage nach Zerstörung dieser Stammzellen das gesamte Gewebe bzw. Organ zugrunde gehen. Gewebe mit flexibler Proliferation haben keine eindeutige Trennung von Stamm- und Funktionszellen (z. B. Leber, Lunge, Gehirn) und können sich von einem subletalen Schaden besser erholen.
Wechselgewebe reagieren früh (Stunden bis max. 6 Monate) nach der Bestrahlung. Flexible Gewebe können Spätreaktionen ausbilden (definitionsgemäß sind das Strahlenfolgen, die nach sechs Monaten noch andauern). Da die meisten Organe aus unterschiedlichen Geweben zusammengesetzt sind (Stroma, Parenchym, Blutgefäße etc.), sind die Verhältnisse in der Praxis komplizierter; jedes Organ kann durch Spätfolgen einer Bestrahlung dauerhaft geschädigt werden, wenn auch in unterschiedlichem Maß.
Auch der makroskopische Aufbau der Organe spielt eine Rolle: Linear aufgebaute Organe wie der Dünndarm oder das Rückenmark sind wesentlich stärker gefährdet als parallel aufgebaute wie z. B. Drüsen. Auf Basis der Spätfolgen, die wesentlich gefürchteter sind als die frühe Strahlungswirkung, hat man für die meisten Organe und Gewebe Toleranzdosen definiert. In der Literatur sind meist TD5/5 angegeben, das heißt die Dosis, bei der ein bestimmter Schaden innerhalb von 5 Jahren bei 5 % der Probanden auftritt. Beispielsweise liegt die TD5/5 der Augenlinse für die Linsentrübung bei 10 Gy (Emami 1991, PMID 2032882). Zur Beschreibung der Strahlenfolgen an Normalgeweben gibt es weltweit standardisierte Kriterienkataloge (CTC für frühe Strahlenfolgen, LENT-SOMA für Spätfolgen).[1]
Wirkung auf Tumoren
Die Empfindlichkeit von Tumoren gegenüber ionisierender Strahlung ist in der Regel höher als die von gesunden Geweben. Sie sind gekennzeichnet durch eine kürzere Zellzykluszeit (< 2 Tage) und einen höheren Anteil an sich teilenden Zellen (Wachstumsfraktion > 40 %). Die Dosis-Wirkung-Beziehung ist S- oder sigmaförmig ebenso wie bei normalen Geweben, allerdings in Richtung zur niedrigeren Dosis (nach links) verschoben. Mathematisch haben die Tumorgewebe ein höheres α/β-Verhältnis (α und β sind die Koeffizienten der linearquadratischen Modellgleichung).
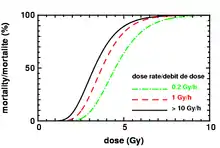
Die Verträglichkeit von Strahlung ist höher, wenn die Dosisleistung (= Dosis pro Zeiteinheit) gering ist oder die Strahlung auf viele kleine Behandlungen verteilt wird. Das liegt an den sofort nach Strahleneintritt anlaufenden Gewebereaktionen, die der kalifornische Strahlenbiologe Hubert Rodney Withers 1975 als 4 R's zusammengefasst hat:
- Reparatur (enzymatische Korrektur der Einzel- und Doppelstrangbrüche und Basenfehler in der DNA)
- Redistribution (Fortsetzung der unterbrochenen Zellzyklen, sodass wieder Zellen aus allen Phasen vorliegen)
- Reoxygenierung (erhöhte Sauerstoffversorgung im Gewebe)
- Repopulation (Nachwachsen von Zellen)
In der Strahlentherapie sind ein bis zwei Behandlungen pro Tag üblich. Zwischen den Behandlungen müssen Pausen von mindestens sechs Stunden liegen. Schnellwachsende Tumoren sind einer verkürzten Strahlentherapie besser zugänglich (wobei nur die Gesamtbehandlungszeit wichtig ist, nicht die Dosis pro Behandlung). Andererseits wird die Empfindlichkeit eines zerfallenden, schlecht durchbluteten Tumors wegen der Hypoxie reduziert. Außerdem werden immer Normalgewebe mitbestrahlt, die wegen ihres niedrigem α/β-Verhältnis für Spätfolgen besonders empfindlich sind und langsamer, mit kleineren Tagesdosen bestrahlt werden sollten. In der Praxis muss deshalb ein Kompromiss geschlossen werden, der vom jeweiligen Tumor und den vorhandenen technischen Möglichkeiten abhängt.
Methodik
Die strahlenbiologische Forschung arbeitet mit molekularbiologischen, zytogenetischen und zytometrischen Methoden an unterschiedlichen Organismen und Zellsystemen. Auf DNA-Niveau wird die strahlenbedingte Mutagenese und deren Reparatur untersucht.
Weitere Themen der Strahlenbiologie
- Der Mensch im Strahlenfeld:
- Erhöhung der Strahlensensibilität, um die Strahlentherapie bei Tumoren effektiver zu machen
- Erhöhung der Strahlenresistenz, um gesundes Gewebe bei der Strahlentherapie zu schonen
- Grundlagen des Strahlenrisikos, Strahlenschäden
- Klinische Strahlenbiologie
- Niedrigstrahlung, negative und positive Strahlenwirkungen im niedrigen Dosisbereich[2]
- Radioaktivität in der Nahrungskette
- Strahlenbelastung, Strahlenschutz
- Zellbiologische Grundlagen der Strahlentherapie
Bekannte Strahlenbiologen
- Otto Hug (1913–1978)
- Hedi Fritz-Niggli (1921–2005), Begründerin der Strahlenbiologie in der Schweiz. Sie erforschte die Schädigungen durch niedrige Strahlendosen insbesondere beim Ungeborenen und in der empfindlichen Entwicklungsphase der Lebewesen
- Wolfgang Köhnlein (* 1933), Universität Münster, emeritiert
- Edmund Lengfelder (* 1943), Professor an der Universität München. Er erforscht seit 1986 die gesundheitlichen Folgen der Katastrophe von Tschernobyl
- Boris Rajewsky (1893–1974)
- Hermann Rink (* 1935), Chemiker, Strahlenbiologe und Emeritus der Medizinischen Fakultät der Universität Bonn
- Christian Streffer (* 1934), Universität Essen, emeritiert
- Joachim Wattendorff (1928–2008), Biologe und Strahlenbiologe, Universität Freiburg in der Schweiz
- Paul Wels (1890–1963), Pharmakologe und Strahlenbiologe. Sein Forschungsinteresse galt insbesondere den Auswirkungen von Röntgenstrahlung auf verschiedene Zellen und von Ultraviolettstrahlung auf die Haut sowie der pharmakologischen Wirkung bestrahlter Substanzen
Siehe auch
Literatur
- Eric J. Hall: Radiobiology for the Radiologist. Philadelphia: Lippincott, Williams & Wilkins, 2000 (5th. ed.), ISBN 0-7817-2649-2
- Thomas Herrmann, Michael Baumann, Wolfgang Dörr: Klinische Strahlenbiologie kurz und bündig. Urban & Fischer Verlag/Elsevier GmbH; 4. Auflage 2006, ISBN 3-437-23960-0
- Hedi Fritz-Niggli: Strahlengefährdung/Strahlenschutz. Verlag Hans Huber, 4. Aufl. 1997
- G. Gordon Steel: Basic Clinical Radiobiology. London: Arnold, 1997 (2nd ed.), ISBN 0-340-70020-3
Weblinks
- Schweizerische Gesellschaft für Strahlenbiologie und Medizinische Physik
- Deutsche Gesellschaft für Biologische Strahlenforschung
- Das Institut für Strahlenbiologie des Helmholtz – Forschungszentrum für Umwelt und Gesundheit bei München erforscht die Wirkung von ionisierender Strahlung auf lebende Zellen und Organismen.
- Die Strahlenschutz-Kommission SSK ist ein Gremium unabhängiger Wissenschaftler, das die deutsche Bundesregierung in allen Aspekten der Strahlenwirkung und des Strahlenschutzes berät.
Einzelnachweise
- Michael Wannenmacher, Jürgen Debus, Frederik Wenz: Strahlentherapie. Springer, 3 November 2006, ISBN 978-3-540-22812-7, S. 279–82 (Abgerufen am 23. Februar 2013).
- Ralph Graeub: Der Petkau-Effekt, Verlag Zytglogge Gümligen, ISBN 3-7296-0222-5