Pronyl-Lysin
Pronyl-Lysin (aus Pyrrolinon-Reduktonyl-Lysin) ist eine Verbindung, die beim Erhitzen von Lysin oder lysinhaltigen Proteinen mit Zuckern entsteht und in vielen Lebensmitteln wie Brot, Bier und Kaffee enthalten ist. Es gehört zu den niedermolekularen Melanoidinen.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
hexanoate_200.svg.png.webp) | |||||||||||||
| Strukturformel ohne Stereochemie | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Pronyl-Lysin | ||||||||||||
| Andere Namen |
Methyl-2-acetamido-6-(2,4-dihydroxy-2,5-dimethyl-3-oxopyrrol-1-yl)hexanoat (IUPAC) | ||||||||||||
| Summenformel | C15H24N2O6 | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 328,36 g·mol−1 | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Geschichte
Nach der Entdeckung der positiven gesundheitlichen Eigenschaften der Melanoidine im Jahre 2001 wurde verstärkt versucht, diese Substanzen aus Lebensmitteln zu extrahieren und ihre Struktur aufzuklären. Da die Stoffgruppe sehr inhomogen ist und Polymere mit Massen bis zu 100.000 Dalton vorkommen, gelang es zunächst nicht, einzelne Melanoidine zu extrahieren. Erst 2002 konnte das Pronyl-Lysin aus der Kruste von Roggenmischbrot isoliert und seine antioxidativen Eigenschaften bewiesen werden.[2]
Darstellung und Eigenschaften
Pronyl-Lysin entsteht durch Erhitzen einer Hexose wie Glucose und Lysin unter Wasserabspaltung. Dabei wird zunächst die Glucose zum Acetylformoin kondensiert, das dann mit Lysin zu einer Vorstufe des Pronyl-Lysins reagiert. Die Carbonsäure-Gruppe des Moleküls wird mit Methanol verestert und die Vorstufe dann mit Essigsäure zum Endprodukt umgesetzt:[3]
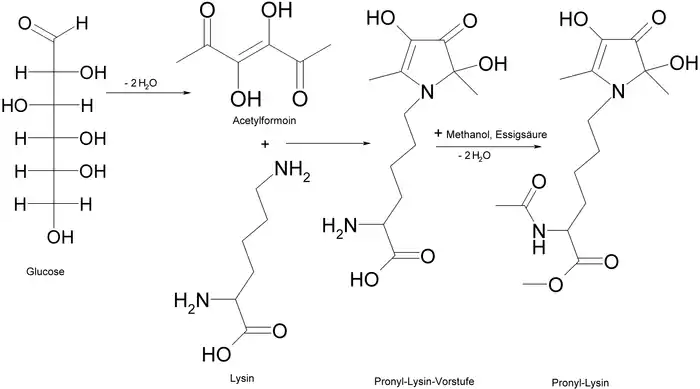
Im Laborversuch zeigte Pronyl-Lysin bei menschlichen Darmkrebszellkulturen eine Erhöhung der Aktivität der Glutathion-S-Transferase (GST) und eine Hemmung der NADPH-Cytochrom-c-Reduktase. Daraus leiteten die Forscher eine antioxidative und chemopräventive Aktivität ab, die auch in aktuellen Untersuchungen an Ratten belegt werden konnte.[4] Die Wirkung als Krebsinhibitor wird dagegen zurzeit von seriösen Quellen wie dem Bundesinstitut für Risikobewertung eher vorsichtig beurteilt.[5]
Siehe auch
Einzelnachweise
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- M. Lindenmeier, V. Faist, T. Hofmann: Structural and functional characterization of pronyl-lysine, a novel protein modification in bread crust melanoidins showing in vitro antioxidative and phase I/II enzyme modulating activity. In: Journal of agricultural and food chemistry. Band 50, Nummer 24, November 2002, S. 6997–7006, PMID 12428950.
- Anke Förster: Quantitative Studie zu Vorkommen und metabolischem Transit alimentärer Maillard-Reaktions-Produkte, TU Dresden, 15. Februar 2006.
- V. Somoza, E. Wenzel, M. Lindenmeier, D. Grothe, H. F. Erbersdobler, T. Hofmann: Influence of feeding malt, bread crust, and a pronylated protein on the activity of chemopreventive enzymes and antioxidative defense parameters in vivo. In: Journal of agricultural and food chemistry. Band 53, Nummer 21, Oktober 2005, S. 8176–8182, doi:10.1021/jf0512611, PMID 16218661.
- BfR: Brotkruste gegen Krebs (Memento vom 2. Februar 2007 im Internet Archive), Stellungnahme vom 13. Dezember 2002.