Per-
Die Vorsilbe Per wird in der Chemie benutzt, um organische und anorganische Verbindungen zu benennen. Per (abgeleitet von per = ganz) bezeichnet stets eine Vollständigkeit. Perhydroverbindungen sind vollständig hydriert, in Perchlorverbindungen sind alle Wasserstoffatome durch Chloratome ersetzt.[1]
| Nutzung der Silbe Per |
 |
 |
Organische Chemie
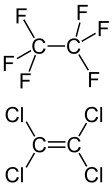
Organische Verbindungen, die neben Kohlenstoff die maximale Anzahl von Atomen einer Elementsorte (meist außer Wasserstoff) enthalten, können im Namen die Silbe per enthalten, z. B. Perchlorethan für Hexachlorethan oder Perfluorethen für Tetrafluorethen. Perchlorethylen (Per-, Tetrachlorethen, C2Cl4) wird im Chemikerjargon auch schlicht „Per“ genannt.[2]
Perfluorierte organische Verbindungen sind sehr stabil, also reaktionsträge Stoffe. Perfluorierte Kunststoffe (Teflon) werden aus Perfluoralkenen hergestellt und besitzen eine beachtliche technische Bedeutung.[3] Benennungen wie „Perchlor...“ oder „Perfluor...“ sind nach der IUPAC-Regel C-105.1 erlaubt.[4]
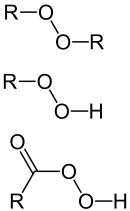
Die Vorsilbe "Per" wird in der Chemie auch zur Benennung benutzt, wenn ein Molekül der Verbindungsklasse der Peroxide, Hydroperoxide oder Percarbonsäuren angehört und somit die Atomgruppierung –O–O– enthält. Bekannte Percarbonsäuren sind die Peressigsäure, die Perbenzoesäure und die m-Chlorperbenzoesäure (MCPBA, von englisch m-chloro perbenzoic acid).
Dekalin – C10H18 – wird auch Perhydronaphthalin genannt.
Anorganische Chemie
Mit der Vorsilbe Per werden Verbindungen gekennzeichnet, die ein Element in seiner höchsten oder wenigstens in einer hohen Oxidationsstufe enthalten, z. B. Perchlorate, Permanganate.
Einzelnachweise
- Wolfgang Holland: Die Nomenklatur in der organischen Chemie, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1969, Seite 38.
- Otto-Albrecht Neumüller (Hrsg.): Römpps Chemie-Lexikon. Band 4: M–Pk. 8. neubearbeitete und erweiterte Auflage. Franckh'sche Verlagshandlung, Stuttgart 1985, ISBN 3-440-04514-5, S. 3041.
- Otto-Albrecht Neumüller (Hrsg.): Römpps Chemie-Lexikon. Band 4: M–Pk. 8. neubearbeitete und erweiterte Auflage. Franckh'sche Verlagshandlung, Stuttgart 1985, ISBN 3-440-04514-5, S. 3045–3046.
- Otto-Albrecht Neumüller (Hrsg.): Römpps Chemie-Lexikon. Band 4: M–Pk. 8. neubearbeitete und erweiterte Auflage. Franckh'sche Verlagshandlung, Stuttgart 1985, ISBN 3-440-04514-5, S. 3042.