PDZ-Domäne
Eine PDZ-Domäne ist ein Teil eines Proteins, welcher mit anderen Proteinen interagieren kann. Es handelt sich um eine modular aufgebaute Proteininteraktionsdomäne, die sequenzspezifisch an kurze Peptide innerhalb anderer Proteine bindet. Solche spezifischen Bindestellen nennt man PDZ-Bindemotiv. Diese Bindestellen liegen oftmals am C-terminalen Ende eines Proteins, können sich aber auch innerhalb eines Proteins befinden, beispielsweise in anderen PDZ-Domänen.
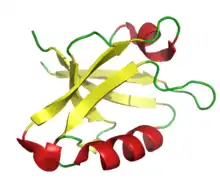
Durch PDZ-Domänen gebildete Proteinkomplexe sind an der Signalübertragung von Zellen bis hin zum Aufbau und Erhalt von Zellpolarität beteiligt.
Geschichte
PDZ-Domänen wurden 1991 zum ersten Mal beobachtet und beschrieben. Die ersten Proteine, in denen PDZ-Domänen gefunden wurden, waren das synaptische Protein PSD95/SAP90 (PSD steht für Post synaptic density), das Septate-junction-Protein Discs large aus Drosophila melanogaster und das Tight-junction-Protein Zonula occludens-1. Aufgrund dieser drei Proteine hat die PDZ-Domäne ihren Namen erhalten. Nicht mehr so häufig verwendete Bezeichnungen lauten auch DHR (Dlg homologous region) oder GLGF (ein relativ gut konserviertes Tetrapeptid in diesen Domänen).
Aufbau und Funktion
PDZ-Domänen bestehen aus etwa 90 Aminosäuren und besitzen eine globuläre Form. Die dreidimensionale Struktur verschiedener PDZ-Domänen wurde inzwischen mittels Röntgenkristallstrukturanalyse aufgeklärt und veröffentlicht.
Proteine, die PDZ-Domänen enthalten, sind in der Regel so genannte „scaffold proteins“, also Gerüstproteine, welche die Grundlage für die Organisation von größeren Proteinkomplexen an spezifischen, subzellulären Kompartimenten bilden. Die PDZ-Domänen vermitteln hier die direkte Interaktion zwischen den Proteinen. Bis zu 13 PDZ-Domänen können in einem Protein enthalten sein.
| PDZ-Domäne | Konsensus-Bindesequenz | Ligand |
|---|---|---|
| Klasse I | -X-S/T-X-L/V-COOH | |
| Syntrophin | -E- S -L- V | Na+-Kanal |
| PSD-95 (PDZ-1 & -2) | -E- T -D- V | K+-Kanal |
| NHERF (PDZ-1) | -D- S -S- L | Adrenozeptor |
| Klasse II | -X-Φ-X-Φ-COOH | |
| hCASK | -E-Y-Y-V | Neurexin |
| Erythrocyte p55 | -E-F-Y-I | Glycophorin C |
| CASK | -E-Y-F-I | SynCAM[1] |
| Klasse III / Andere | ||
| Mint-1 | -D-H-W-C | Ca2+-Kanal |
| nNOS | -V-D-S-V | Melatonin-Rezeptor |
Die als erste identifizierte und bei weitem häufigste Funktion von PDZ-Domänen ist die Erkennung und Interaktion mit spezifischen C-terminalen Motiven von Partnerproteinen. Die letzte und die drittletzte Aminosäure scheinen hauptsächlich für die Spezifität der Interaktion entscheidend zu sein, so dass anhand dieser Sequenzen die PDZ-Domänen in drei Klassen eingeteilt wurden. Weiterhin wurden inzwischen auch einige Beispiele von durch PDZ-Domänen vermittelten Interaktionen mit nicht-C-terminalen Motiven entdeckt. So bilden manche Proteine interne Bindungsstellen für PDZ-Domänen, welche in einer β-Haarnadelschlaufen-Struktur die Konsensussequenz präsentieren und so einen C-Terminus imitieren. Eine solche Struktur existiert auch in bestimmten PDZ-Domänen, so dass hier PDZ mit PDZ-Domänen interagieren, eine so genannte „Head to Tail oligomerization“.
Verbreitung
PDZ-Domänen wurden in diversen Proteinen von Bakterien, Hefen, Pflanzen, Insekten und Vertebraten gefunden. Beim Menschen wurden bislang über 240 Proteine entdeckt, welche diese Domäne enthalten. In der Regel sind dies zytoplasmatische Proteine. Bekanntere Beispiele sind PSD-95, ein Mitglied der MAGUK-Proteinfamilie mit Bedeutung für den Aufbau von Synapsen von Nervenzellen, nNOS, eine neuronale NO-Synthase, Harmonin, einem Gerüstprotein mit Funktion in Sinneszellen sowie hHtrA, einer humanen Serinprotease.
Referenzen
- T. Biederer u. a.: SynCAM, a synaptic adhesion molecule that drives synapse assembly. In: Science. 297, 2002, S. 1525–1531. PMID 12202822.
Literatur
- C. Nourry, S. G. Grant, J. P. Borg: PDZ domain proteins: plug and play! In: Sci.STKE. 179, 2003, S. re7.
- M. Sheng, C. Sala: PDZ domains and the organization of supramolecular complexes. In: Annu.Rev.Neurosci. 24, 2001, S. 1–29.