Neodym(II)-chlorid
Neodym(II)-chlorid ist eine anorganische chemische Verbindung des Neodyms aus der Gruppe der Chloride. Zu beachten ist, dass es im Phasendiagramm von Neodym und Chlor zwischen Neodym(II)-chlorid NdCl2 und Neodym(III)-chlorid NdCl3, mit NdCl2,25 und NdCl2,36 zwei weitere nachgewiesene Phasen gibt.[3]
| Kristallstruktur | |||||||
|---|---|---|---|---|---|---|---|
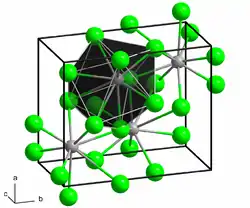 | |||||||
| _ Nd2+ _ Cl− | |||||||
| Raumgruppe |
Pbnm (Nr. 62, Stellung 3) | ||||||
| Allgemeines | |||||||
| Name | Neodym(II)-chlorid | ||||||
| Andere Namen |
Neodymdichlorid | ||||||
| Verhältnisformel | NdCl2 | ||||||
| Kurzbeschreibung |
schwarzer Feststoff[1] | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 215,15 g·mol−1 | ||||||
| Aggregatzustand |
fest[1] | ||||||
| Schmelzpunkt | |||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Gewinnung und Darstellung
Neodym(II)-chlorid kann durch Reduktion von Neodym(III)-chlorid mit Neodym im Vakuum bei 800 bis 900 °C gewonnen werden.[1]
Eigenschaften
Neodym(II)-chlorid ist ein schwarzer Feststoff, der in Pulverform dunkelgrün erscheint. Die Verbindung ist äußerst hygroskopisch und kann nur unter sorgfältig getrocknetem Schutzgas oder im Hochvakuum aufbewahrt und gehandhabt werden. An Luft oder bei Kontakt mit Wasser geht er unter Feuchtigkeitsaufnahme in Hydrate über, die aber instabil sind und sich mehr oder weniger rasch unter Wasserstoff-Entwicklung in Oxidchloride bzw. Neodym(III)-hydroxid[4] verwandeln. Die Verbindung besitzt eine orthorhombische Kristallstruktur vom Blei(II)-chlorid-Typ[1] mit der Raumgruppe Pbnm (Raumgruppen-Nr. 62, Stellung 3)[5].
Einzelnachweise
- Georg Brauer, unter Mitarbeit von Marianne Baudler u. a. (Hrsg.): Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I. Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 1081.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- G. Meyer, Lester R. Morss: Synthesis of Lanthanide and Actinide Compounds. Springer, 1991, ISBN 0-7923-1018-7, S. 161 (eingeschränkte Vorschau in der Google-Buchsuche).
- Advances in Inorganic Chemistry and Radiochemistry. Academic Press, 1977, ISBN 0-08-057869-1, S. 18 (eingeschränkte Vorschau in der Google-Buchsuche).
- G. Ferguson, J. Trotter: Structure Reports for 1985, Volume 52A: Section I Metal Section II Inorganic ... Springer, 1986, ISBN 90-277-2385-0, S. 130 (eingeschränkte Vorschau in der Google-Buchsuche).