Mekoniumaspiration
Eine Mekoniumaspiration (Mekoniumaspirationsyndrom, MAS) bezeichnet das Eindringen von Mekonium in die Lungen des Neugeborenen vor oder unter der Geburt und die damit verbundene Folgesymptomatik. Mekonium, auch „Kindspech“ genannt, ist der Darminhalt des Feten und der Kot des Neugeborenen in den ersten Lebenstagen.
| Klassifikation nach ICD-10 | |
|---|---|
| P24.0 | Mekoniumaspiration durch das Neugeborene |
| ICD-10 online (WHO-Version 2019) | |
Dem Mekoniumaspirationssyndrom geht ein vorzeitiger Abgang des Mekoniums ins Fruchtwasser voraus. Mekoniumhaltiges Fruchtwasser ist keineswegs selten, denn 13 % aller lebenden Neugeborenen werden aus mekoniumhaltigem Fruchtwasser geboren. Von diesen Kindern entwickeln 5 % – 12 % ein MAS.[1]
Auslösendes Ereignis für ein MAS
Der Entwicklung eines MAS geht in der Regel eine fetale Notsituation (z. B. Sauerstoffminderversorgung der Gewebe = Hypoxie) oder ein unzureichender Blutfluss beim Feten (Ischämie) voraus. Auf Grund der fetalen Stress- oder Schocksituation mit Blutfluss-Umverteilung zu den lebenswichtigen Organen (Herz und Gehirn) wird der Magen-Darm-Trakt des Feten zunächst unzureichend durchblutet, wobei es jedoch im weiteren Verlauf zu einer reaktiven Hyperperistaltik (vermehrte Darmbewegung) und in Verbindung mit einer Analsphinkter-Relaxierung (Schließmuskel-Erschlaffung) zum Abgang von Mekonium in die Fruchthöhle kommt. Da beim Ungeborenen im Rahmen des Sauerstoffmangels kräftige Atembemühungen (unter Umständen Schnappatmung) ausgelöst werden, kann das im Fruchtwasser schwimmende Mekonium bis tief in die Atemwege eindringen.[2][3]
Mit MAS assoziierte Erkrankungen
Folgende Erkrankungen sind gehäuft mit einem MAS assoziiert:
- Schwieriger und verlängerter Geburtsverlauf
- Infektion des Feten (pränatale Infektion)
- Übertragung (Gestationsalter > 42 SSW (Schwangerschaftswochen))
- Mütter mit Drogenkonsum (Drogenabusus), insbesondere Nikotin, Alkohol, Kokain
- Mütterliche Erkrankungen wie Diabetes mellitus, Bluthochdruck oder andere Erkrankungen des Herz-Kreislaufsystems
- Fehlbildungen oder krankhafte Veränderungen der Nabelschnur
- Nicht ausreichendes kindliches Wachstum (Intrauterine Wachstumsretardierung)
- Die Frühgeburtlichkeit stellt dagegen kein erhöhtes Risiko für ein MAS dar. Ein MAS bei Frühgeborenen unter der 32. SSW ist eher selten.
Klinische Zeichen eines MAS
Mekoniumverschmierte Kinder müssen nicht zwingend eine Mekoniumaspiration entwickelt haben. Nicht wenige Kinder entleeren durch den Geburtsstress Mekonium. Vor allem in der Austreibungsphase, wenn das Kind durch die Presswehen zeitweise einen Sauerstoffmangel erfährt, kann es Mekonium entleeren. Ist der Kopf des Kindes jedoch erst in den Geburtskanal eingetreten, kann es kein Mekonium aspirieren. Zeigt das Kind unmittelbar nach der Geburt keine normale Vitalität und sind gleichzeitig nachfolgende Symptome vorhanden, muss eine Mekoniumaspiration mit hoher Wahrscheinlichkeit angenommen werden:
- Kein oder stark herabgesetzter Muskeltonus (das Kind ist schlaff)
- Keine oder keine normale Atmung (statt kräftigem Schreien wimmert oder stöhnt das Kind nur), es hat offensichtliche Mühe beim Atmen und zeigt Einziehungen in den Zwischenrippenräumen, am Zwerchfell und Jugulum, ein Nasenflügeln und eine Blauverfärbung der Haut und Schleimhäute (Zyanose)
- Sichtbar mekoniumverschmierte Haut, Mekonium in den Hautfalten und in den Körperöffnungen wie Ohren, Naseneingänge, Mund und Rachen
- Grünlich verfärbte Haut, Fingernägel oder Nabelschnur (zeigt meist einen bereits länger zurückliegenden Mekoniumabgang an)
Behandlungsstrategie einer Mekoniumaspiration
Es wird angenommen, dass ein erheblicher Anteil der Neugeborenen mit MAS dieses bereits vor Beginn des eigentlichen Geburtsvorganges erlitten haben und Maßnahmen im unmittelbar postnatalen Verlauf zur Vermeidung einer MAS bei diesen Kindern letztlich nur marginalen Erfolg bringen. Das früher noch empfohlene Vorgehen bei mekoniumhaltigem Fruchtwasser, die Kinder generell nach Entwicklung des kindlichen Kopfes und Schulter im Rachen abzusaugen (intrapartales Absaugen), gefolgt von einem trachealen Absaugen nach vollständiger Geburt des Kindes, konnte die Inzidenz (Erkrankungshäufigkeit) eines MAS jedenfalls nicht signifikant nachweisbar reduzieren.[4][5] Liegt mekoniumhaltiges Fruchtwasser vor oder ist das Kind mekoniumverschmiert, sollte es dennoch möglichst frühzeitig gründlich im Mund und Rachen abgesaugt werden. Sofern das Kind danach eine unbeeinträchtigte Atmung und einen ausreichenden Muskeltonus zeigt, kann es zunächst wie ein gesund geborenes Kind weiter betreut werden, wobei es im weiteren Verlauf bei der Atmung engmaschiger überwacht werden sollte. Bei Kindern mit unzureichendem oder fehlendem Muskeltonus, die nicht oder unzureichend atmen, sollte dagegen durch medizinisches Fachpersonal ein Beatmungsschlauch (Endotrachealtubus) in die Luftröhre eingelegt werden (Endotracheale Intubation) und möglichst viel aspiriertes Mekonium durch einen Absauger entfernt werden.[1] Bei dickflüssigem Mekonium im Larynx (Kehlkopf) kann unter Umständen auch eine Spülung der Trachea und Bronchien (endotracheale Lavage) mit einer verdünnten Surfactantlösung zum Auswaschen des Mekoniums versucht werden. Anschließend wird maschinell beatmet, gegebenenfalls Maßnahmen zur Kreislaufstabilisierung ergriffen und das Kind einer intensivmedizinischen Überwachung und Therapie auf einer Kinderintensivstation zugeführt.
Krankhafte Abläufe nach der Mekoniumaspiration
Gelangt eine größere Menge Mekonium in die Atemwege, kann das Kind unmittelbar nach der Geburt seine Lungen nicht ausreichend belüften, es entsteht eine Atemnot. Das Kind zeigt klassische Zeichen einer nachgeburtlichen Anpassungsstörung der Atmung, mit beschleunigter Atmung (Tachypnoe), erschwerter Atmung (Dyspnoe), ein stöhnendes oder karchelndes Atemgeräusch, Einziehungen der Zwischenrippen-Räume (intracostale Einziehungen) und des Brustbeines (sternale Einziehungen) sowie eine sichtbare Blauverfärbung der Haut und Schleimhäute (Zyanose). Abhängig von Dauer und Ausprägung der Atemnot und der daraus resultierenden Hypoxie kann das Kind auch eine schwere Herz-Kreislauf-Depression erfahren. Bei schwerwiegenden und vor allem länger andauernden (protrahierten) intrauterinen Sauerstoffmangel-Zuständen kann das Kind auch schon ohne Lebenszeichen (Asphyxie palladia = weiße Asphyxie) geboren werden und muss sofort einer Herz-Kreislauf-Wiederbelebung (Reanimation) zugeführt werden.
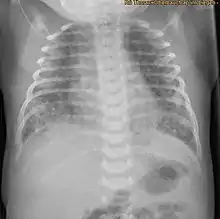
Durch das eingeatmete Mekonium entstehen in der Lunge des Kindes Bereiche mit unzureichender Belüftung (Atelektasen), während andere Bereiche dagegen überdehnt bzw. überbläht (Lungenemphysem) werden. Bei der Überblähung wirkt das in den Atemwegen befindliche zähe Mekonium wie ein Ventil. Atemgas wird bei der Überdruckbeatmung zwar am Mekonium vorbei in die nachgeschalteten Lungenbläschen eingeblasen, kann aber bei der Ausatmung nicht mehr am Mekonium vorbei entweichen und verbleibt in der Lunge. Die betroffenen Lungenbezirke können nicht mehr ausreichend ausatmen und werden so überbläht. Die Folgen eines solchen ungleichmäßigen Belüftungsverhaltens einzelner Lungenbereiche sind in der Röntgenaufnahme der Lunge (Röntgen-Thorax) deutlich zu sehen. Der Radiologe befundet ein "Mischbild aus diffuser Minderbelüftung (Atelektasen) bei gleichzeitig vorhandenen Bereichen der Überblähung (Emphysem)". Sehr häufig tritt in einer solchen Situation ein Pneumothorax auf. Die sehr dünne Membran der überdehnten Lungenbläschen zerreißt und Atemgas gelangt dann aus den Alveolen in das Lungen-Bindegewebe (interstitielles Emphysem). Findet diese außerhalb der Alveolen gelegene Gasansammlung dann Anschluss an den Pleuraspalt, wird dort die Haftung der beiden Pleurablätter aufgehoben und die Lunge zieht sich auf Grund der Eigenelastiziät zusammen. Hierdurch kann eine akut lebensbedrohliche Situation für das Kind resultieren. Als weitere Komplikation der Mekoniumansammlung in den Atemwegen entsteht eine reaktive Pneumonie (Lungenentzündung) und eine Inaktivierung von lungenstabilisierendem Faktor (Surfactant). Während bis vor 15–20 Jahren ein MAS noch eine schwer zu behandelnde Erkrankung des Neugeborenen mit hoher Sterblichkeit darstellte, sind die Behandlungsergebnisse des MAS heute durch spezielle Beatmungstechniken, antibiotische Therapie, inhalative Stickoxidtherapie (iNO) und vor allem der Gabe von aus Tierlungen extrahiertem lungenstabilisierendem Faktor (Surfactantsubstitution) erheblich verbessert worden. So ist der ECMO-Bedarf bei Neugeborenen mit diesem Krankheitsbild über die letzten 10 Jahre kontinuierlich gesunken.[6]

Literaturhinweis
- T. E. Wiswell, C. M. Gannon u. a.: Delivery room management of the apparently vigorous meconium-stained neonate: results of the multicenter, international collabrative trial. In: Pediatrics. 2000; 105, S. 1–7.
- M. Obladen: Neugeborenenintensivpflege. 6. vollständig überarbeitete Auflage. Springer Verlag.
- S. N. Ahanya, J. Lakshmanan, B. L. Morgan, M. G. Ross: Meconium passage in utero: mechanisms, consequences, and management. In: Obstet Gynecol Surv. 2005 Jan; 60(1), S. 45–56.
- H. S. Falciglia: Failure to prevent meconium aspiration syndrome.
- R. O. Davis, J. B. Philips, B. A. Harris, Jr, E. R. Wilson, J. F. Huddleston: Fatal meconium aspiration syndrome occurring despite airway management considered appropriate. In: Am J Obstet Gynecol. 1985;151, S. 731–736.
- R. F. Soll, P. Dargaville: Surfactant for meconium aspiration syndrome in full term infants. In: Cochrane Database Syst Rev. 2000;(2), S. CD002054.