Magnesiumtitanoxid
Magnesiumtitanoxid ist eine anorganische chemische Verbindung des Magnesiums aus der Gruppe der Titanate.
| Kristallstruktur | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
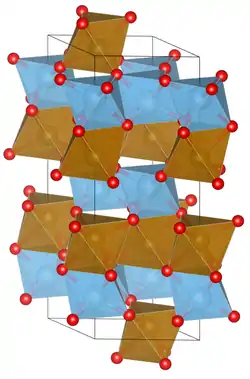 | |||||||||||||
| _ Mg2+ _ Ti4+ _ O2− | |||||||||||||
| Kristallsystem |
rhomboedrisch | ||||||||||||
| Raumgruppe |
R3 (Nr. 148) | ||||||||||||
| Gitterparameter |
a = 5,05478 Å, c = 13,8992 Å,Z = 6 | ||||||||||||
| Allgemeines | |||||||||||||
| Name | Magnesiumtitanoxid | ||||||||||||
| Andere Namen |
Magnesiumtitanat | ||||||||||||
| Verhältnisformel | MgTiO3 | ||||||||||||
| Kurzbeschreibung |
weißer geruchloser Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 120,21 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Dichte |
3,36 g·cm−3[1] | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Gewinnung und Darstellung
Die Magnesiumtitanate MgTiO3, Mg2TiO4 und MgTi2O5 können auf nasschemischen Peroxidweg bei niedrigen Temperaturen synthetisiert werden. Der erste Schritt der Herstellung ist die Fällung von Peroxovorläufern bestimmter Stöchiometrie, die durch thermische Zersetzung in die entsprechenden Titanate überführbar sind.[3]
Die Verbindung kann auch durch Reaktion von Eisentitanat mit Magnesiumoxid und Kohlenstoff dargestellt werden.[4]
Eigenschaften
Magnesiumtitanoxid ist ein weißer geruchloser Feststoff, der praktisch unlöslich in Wasser ist.[1] Er besitzt eine Ilmenit Kristallstruktur mit der Raumgruppe R3 (Raumgruppen-Nr. 148) und den Gitterkonstanten a = 5,05478 Å und c = 13,8992 Å. In einer Elementarzelle sind sechs Formeleinheiten.[5]
Verwendung
Magnesiumtitanoxid wird als Zwischenprodukt zur Herstellung anderer chemischer Verbindungen und in der chemischen Forschung eingesetzt.[1] Es wird auch als Dielektrikum in Kondensatoren, Resonatoren und Filtern für die Kommunikationselektronik eingesetzt.[6][7]
Einzelnachweise
- Datenblatt Magnesium titanium oxide, 99% (metals basis) bei AlfaAesar, abgerufen am 13. April 2019 (PDF) (JavaScript erforderlich).
- Geikielite: Mineral information, data and localities.: Geikielite: Mineral information, data and localities., abgerufen am 13. April 2019
- Richard C. Ropp: Encyclopedia of the Alkaline Earth Compounds. Newnes, 2012, ISBN 0-444-59553-8, S. 660 (eingeschränkte Vorschau in der Google-Buchsuche).
- Chen, Chao, Ti-Chang Sun, Jue Kou, Xiao-Ping Wang, and Yong-Qiang Zhao. "Feasibility study on preparation of magnesium titanate in carbonthermic reduction of vanadium titanomagnetite concentrates". Physicochemical Problems of Mineral Processing 55 no. 2 (2019): 417-425. doi:10.5277/ppmp18151.
- B. A. Wechsler, R. B. Von Dreele: Structure refinements of Mg2TiO4, MgTiO3 and MgTi2O5 by time-of-flight neutron powder diffraction. 45, 1989, S. 542, doi:10.1107/S010876818900786X.
- Bill Lee, Rainer Gadow, Vojislav Mitic: Proceedings of the IV Advanced Ceramics and Applications Conference. Springer, 2017, ISBN 978-94-6239-213-7, S. 147 (eingeschränkte Vorschau in der Google-Buchsuche).
- Takuro Sato, Ryoichi Miyamoto, Atsushi Fukasawa: Deviation of Dielectric Properties in Magnesium Titanate Ceramics. In: Japanese Journal of Applied Physics. 20, 1981, S. 151, doi:10.7567/JJAPS.20S4.151.