Insulintherapie
Die Insulintherapie ist eine Behandlungsmethode in der Diabetologie, bei der zur Therapie eines erhöhten Blutzuckers bei Diabetes mellitus ein Insulinpräparat verabreicht wird, um den relativen oder absoluten Mangel des körpereigenen Stoffwechselhormons Insulin auszugleichen.
Insulin wurde in den ersten Jahrzehnten des 20. Jahrhunderts als der blutzuckersenkende Stoff aus dem Bauchspeicheldrüsengewebe erkannt und chemisch isoliert. 1922 erfolgte durch Frederick Banting die erste Therapie mit Insulin an einem Menschen mit Diabetes mellitus Typ 1.
Möglichkeiten der Insulinzufuhr
Die bisher zugelassenen Möglichkeiten, sich Insulin zuzuführen, sind Injektionen mittels Pen, Insulineinmalspritze, oder die kontinuierliche subcutane Insulininfusion (CSII) mit einer Insulinpumpe. Die Injektion wird üblicherweise im Unterhaut-Fettgewebe (= subcutan) vorgenommen, seltener intramuskulär oder intravenös. Bei der subcutanen Injektion in die Unterhaut muss die Lokalisation häufig gewechselt werden, da sonst eine Lipohypertrophie auftreten kann.[1]
Insulinpräparate zur Inhalation werden zwar weiterhin erforscht, das einzige bisher in der EU zugelassene Produkt (Exubera) wurde aber vom Hersteller 2007 wieder zurückgezogen.[2]
Spritze
Spritzen waren bis zur Ära der Insulinpens die Norm. Ältere Typ-1-Diabetiker kennen noch die Mehrwegspritzen und die dicken Mehrwegnadeln, die lange Zeit für den Schrecken der Insulintherapie verantwortlich waren. Abgelöst wurden diese durch Einwegspritzen mit sehr dünnen Einwegnadeln. Heutzutage werden in Deutschland überwiegend Insulinpens verwendet. Als Notfallausrüstung sind Einwegspritzen und -nadeln nach wie vor im Handel. Es gibt Insulinspritzen für Insulin U40 (= 40 Einheiten Insulin pro Milliliter) und Insulin U100 (= 100 Einheiten Insulin pro Milliliter).
Länge der Injektionsnadeln:Es gibt unterschiedliche Nadellängen z. B. 4-6 mm bei Kindern und sehr schlanken Erwachsenen, weiterhin 8 mm;10 mm und 12 mm.
Insulinpen
Sogenannte Insulinpens sehen dickeren Kugelschreibern ähnlich und lassen sich mit einer Insulinpatrone bestücken. Die Insulindosis wird an einem Drehrad eingestellt, welches bei Knopfdruck den Hub eines Stempels begrenzt, der den Kolben in der Patrone weiterschiebt. Es gibt unterschiedliche Größen der Patronen, die übliche Füllmenge ist 3 ml (mit Insulin U100, d. h. 100 IE pro ml). Die dazu passenden Injektionskanülen sind beidseitig angespitzt und in der Mitte mit einem Plastikgewinde versehen. Sie werden meist nur einmal verwendet, also vor jeder Injektion aufgeschraubt und stechen sich dabei durch die Gummimembran der Patrone. Sie sind in verschiedenen Längen verfügbar.
Fertigpen
Fertig- oder Einwegpens sind fest mit einer Insulinpatrone bestückt und werden nach Aufbrauchen des Insulins entsorgt.
Insulinpumpe
Insulinpumpen dienen der kontinuierlichen Abgabe von Insulin ins Unterhautfettgewebe. Die vorprogrammierte Menge an Basalinsulin (langwirksames Insulin) die durch die Pumpe verabreicht wird dient der Grundversorgung des Körpers mit Insulin und wird auch als Basalrate bezeichnet. Das Mahlzeiteninsulin (kurzwirksames Insulin) wird nach Bedarf zusätzlich als Bolus verabreicht (Bolusgabe).
Therapieformen
In den vergangenen Jahrzehnten wurden von verschiedenen Diabetologen und Diabeteskliniken unterschiedliche Therapie-Varianten um die Insulintherapie entwickelt, die oft jeweils einen bestimmten Patientenkreis oder bestimmte Problemstellungen im Auge hatten. Zur Vereinfachung gab man den Therapieformen einprägsame Akronyme (CT, ICT, FIT, BOT, SIT, CSII), die im Folgenden kurz erklärt werden.
Konventionelle Insulintherapie (CT)
Bei der konventionellen Insulintherapie wird zu festgesetzten Zeiten eine bestimmte Menge Insulin gespritzt. Die CT findet ihre Anwendung typischerweise beim insulinpflichtigen Diabetes mellitus Typ 2, vorwiegend bei älteren Patienten, da vor allem diese einen festen Tagesrhythmus haben. Zwei- bis dreimal täglich wird meist ein Mischinsulin gespritzt. Diese Therapieform erfordert die pünktliche Einnahme von Mahlzeiten mit genau festgelegter Menge an blutzuckerwirksamen Kohlenhydraten. Aufgrund der Insulinwirkung müssen auch Zwischenmahlzeiten vor- und nachmittags sowie eine Spätmahlzeit eingehalten werden. Weil diese Therapie ein praxisfernes, schematisches Ernährungsverhalten voraussetzt, ist keine flexible Gestaltung der täglichen Mahlzeiten möglich. Hinzu kommt, dass bei Auslassen von Mahlzeiten eine erhebliche Gefahr der Unterzuckerung (Hypoglykämie) besteht.
Intensivierte konventionelle Insulintherapie (ICT)
(siehe auch Basis-Bolus-Therapie)
Die intensivierte konventionelle Insulintherapie (ICT) wird vorwiegend bei Typ-1-Diabetikern, bei unzureichender Insulinsekretion bzw. fortgeschrittener Erkrankung jedoch auch bei Typ-2-Diabetikern angewandt. Sie besteht aus einer sog. Zwei-Spritzen-Therapie, d. h. einerseits wird schnell wirksames Insulin zu den Mahlzeiten und zur Korrektur gespritzt (Bolus), andererseits braucht der Körper, unabhängig von den zugeführten Kohlenhydraten, eine Grundversorgung mit Insulin, die mit Verzögerungsinsulin gewährleistet wird (Basis). Dieses Basis-Bolus-Prinzip ahmt die Insulinsekretion der gesunden Bauchspeicheldrüse nach. Das Basisinsulin wird je nach Insulinart und Blutzuckerverlauf ein- bis dreimal am Tag gespritzt; das Bolusinsulin zu den Mahlzeiten bzw. bei zu hohen Blutzuckerwerten.
Die Basalrate muss an unterschiedliche körperliche Belastungen angepasst werden.
Die ICT ermöglicht eine variablere Lebensführung als die Konventionelle Therapie, da hier besser Anpassungen an die aktuelle Lebenssituation (Bewegung, Ruhen, Arbeit, Sport usw.) vorgenommen werden können. In Verbindung mit Stoffwechselkontrollen (Blutzuckermessung) und der Protokollierung aller den Glucose-Stoffwechsel beeinflussenden Faktoren lässt sich eine rasche Umsetzung veränderter Ergebnisse und Anpassung vornehmen.
Die österreichische Diabetologin Kinga Howorka prägte den Begriff Funktionelle Insulintherapie.[3] Sie entspricht im Wesentlichen der heutzutage angewendeten ICT.
Supplementäre Insulintherapie (SIT)
Die Supplementäre Insulintherapie wendet sich primär an Diabetiker, die noch über eine eigene Insulinsekretion verfügen. Beim Diabetiker vom Typ 2 steht man vor allem vor dem Problem, dass eine Wirkstörung des Insulins vorliegt und somit eigentlich viel zu viel Insulin vorhanden ist. Gleichzeitig ist der schnelle Anstieg des Insulinspiegels nach Mahlzeiten gedämpft. Dafür gibt man — neben einer insulinunabhängigen Therapie mit Metformin — zu den Mahlzeiten ein schnellwirksames Insulin. So werden Blutzuckerspitzen nach den Mahlzeiten zuverlässig und wirkungsvoll gekappt. Die optimierte Insulinanpassung zur Mahlzeit verbessert die Stoffwechsellage und senkt das Risiko einer Unterzuckerung. Da Zwischenmahlzeiten ausgelassen werden können, ist die Gewichtsabnahme erleichtert.
Basal unterstützte orale Therapie (BOT)
Der Typ-2-Diabetiker erhält z. B. zu Beginn der Therapie orale Antidiabetika. Wenn sich dann insbesondere in den Morgenstunden erhöhte Nüchternblutzuckerwerte zeigen, wird ein Basal-Insulin in den Abendstunden verabreicht, das die endogene Gluconeogenese der Leber in den frühen Morgenstunden unterdrückt.
Kontinuierliche subkutane Insulininfusion (CSII): Pumpentherapie
Die Insulin-Pumpentherapie (Insulinpumpe) als kontinuierliche subkutane Insulininfusion ist eine teilautomatisierte Behandlung überwiegend für Typ-1-Diabetiker und kann als die fortschrittlichste Therapieform angesehen werden. Ihr wesentlicher Nachteil ist, dass sie insgesamt deutlich teurer ist als die ICT. Daher benötigen die Krankenkassen eine nachvollziehbare Begründung, warum der behandelnde Arzt bei seinem Patienten diese Form der Therapie empfiehlt. Langfristig gesehen spart sie aber durch die Verminderung von Spätfolgen auch Geld für die Kassen.
Die Vorteile gegenüber anderen Therapieformen sind:
- geringere Insulindepots im Unterhaut-Fettgewebe (geringeres Unterzuckerungsrisiko)
- bessere Einstellbarkeit auf Bewegungsunterschiede durch Senken oder Anheben der Basalrate
- genauere Dosierbarkeit der Basalrate als auch des mahlzeitenbezogenen Insulins
- bessere Steuerung eines Dawn-Phänomens (Morgendämmerungs-Phänomen = morgendlicher hormoneller Anstieg der Insulinresistenz)
- bessere Eingriffsmöglichkeiten bei Stoffwechselschwankungen
- ideale Insulinreduktionsmöglichkeiten vor sportlichen Ereignissen mit weitaus geringerer Gewichtszunahme durch mahlzeitenbezogene Zwangskohlenhydrate zur Kompensation eines erhöhten Wirkungsgrades der basalen Insuline/ Wirkungsverbesserung an den Rezeptoren (Basalrate lässt sich abschalten oder reduzieren)
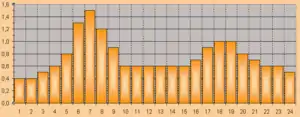
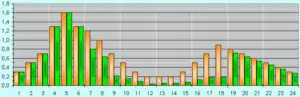 Beispiel für ein Profil mit Absenkungen
Beispiel für ein Profil mit Absenkungen - weniger Hypoglykämieepisoden durch Absenkung des aktuell zugeführten Insulins bei gleichzeitig geringen im Körper bereits vorhandenen Insulindepots, die nun nicht mehr durch die Aufnahme von zusätzlichen Kohlenhydraten aufgefangen werden müssen
- mitunter Unterstützung beim Ermitteln der Insulinmengen für eine Mahlzeit mit Dokumentationsunterstützung; nicht bei allen Pumpen.
Weitere Indikationen können sein:
- stark schwankende Blutzuckerwerte wie bei ausgeprägtem Dawn-Phänomen (starker Anstieg des Blutzuckers in den frühen Morgenstunden)
- geringer Insulinbedarf (Kleinkinder, Personen mit hoher körperlicher Bewegung während des Tages)
- Schichtarbeit
- ungenügend einstellbarer Blutzucker mit zu hohem HbA1c
- Schwangerschaft mit sonst nicht einstellbarem Zuckerstoffwechsel.
Wichtige Aspekte
Bei allen Therapieformen sind bestimmte gemeinsame Aspekte zu beachten, um die Therapie erfolgreich anzuwenden.
Blutzucker-Selbstkontrollen
- Hauptartikel: Blutzucker, Blutzuckermessgerät, Kontinuierlich messender Glucosesensor
Mit einem Blutzuckermessgerät kann der Diabetiker seinen Blutzucker selbst kontrollieren. Für den Typ-1-Diabetiker immer, aber oft auch für den Typ-2-Diabetiker ist das Messen des eigenen Blutzuckers während der Insulinbehandlung unerlässlich für die Therapie. Bei insulinpflichtigen Patienten werden die Kosten für die Blutzuckerselbstkontrolle von den gesetzlichen Krankenkassen erstattet[4]. Die Blutzuckermessung mit einem kontinuierlich messenden Glucosesensor (CGM-System) liefert engmaschigere Blutzuckerwerte im Minutentakt. Die Werte werden dabei grafisch auf einem CGM-System oder alternativ auf der Insulinpumpe abgebildet. Die Gefahr von Über- oder Unterzuckerungen kann durch individuell einstellbare Grenzwerte am CGM-System abgefangen werden.
Protokollführung
Das Protokoll soll in einem machbaren Rahmen alle Daten enthalten, die zu einer korrekten Beurteilung der Stoffwechselentwicklung und damit zu angemessenen Insulingabe nötig sind. Dies geht in der Regel nur, wenn alle den Blutzucker beeinflussenden Faktoren notiert werden. Hierzu zählen neben dem eigentlichen Blutzuckerwert vor allem der genaue Zeitpunkt der Messung, ob vor oder nach einer Mahlzeit, sowie Angaben zum Kohlenhydratgehalt der aufgenommenen Nahrung. Daneben sind all jene Daten wichtig, die zur Senkung des Blutzuckerwertes führen, wie Perioden intensiver Bewegung (Sport), Schwitzen, aber auch Faktoren wie Arbeitsbelastung oder Stress. Je zuverlässiger diese Eintragungen sind, desto sicherer sind die Schlüsse, die aus einem solchen Protokoll gezogen werden können (BE-Faktoren, Basalratenveränderungen, Einschätzungen von Lebensmitteln usw.).
Das Protokoll kann auf Papier oder mithilfe spezieller, so genannter Diabetes Management Software elektronisch geführt werden; zahlreiche Blutzuckermessgeräte können heute die gemessenen Werte samt Zusatzangaben speichern und verwalten sowie per Interfacekabel oder via Bluetooth oder Mail an einen Rechner und/oder in eine Patientenakte im Internet übertragen, was den Vorteil des Fernmonitorings bietet: Der Patient kann dem Arzt den Zugriff auf die Daten erlauben, was z. B. für telefonische Beratungen und Notfallsituationen sinnvoll ist.
Wechselschicht und ungleicher Tagesrhythmus
Ein wechselnder Tagesrhythmus erschwert die Insulintherapie insbesondere dann, wenn hierdurch Schlafstörungen auftreten. Diese können dazu führen, dass der Körper insulinunempfindlicher wird (bis zu ca. 40 %). Insbesondere Wechselschicht kann – wenn sie Schlafstörungen zur Folge hat – verstärkte Probleme mit der Stoffwechselführung mit sich bringen.
Hierbei zu beachten wäre insbesondere ein verschobenes Dawn- und Dusk-Phänomen (durch die Tageszeitrhythmik verursachte, erhöhte, hormononelle Blutzuckerspitzen am Morgen bzw. am Abend).
Stoffwechselschwankungen
Eine Insulintherapie ohne Stoffwechselschwankungen ist nicht führbar. Der Blutzucker kann – je nach Einflussfaktor und Intensität – schon innerhalb von einer Stunde gravierenden Veränderungen unterliegen. In der Regel sind diese Schwankungen aber durch den Diabetiker selbst erklärbar und über einen gewissen Zeitraum vorhersehbar, so dass sie innerhalb gewisser Bandbreiten (Erwartungen) auch berechenbar bzw. abschätzbar sind. Ursachen für starke Blutzuckerschwankungen können auf Prozessen wie dem Dawn-Phänomen oder dem Somogyi-Effekt beruhen. Als Brittle-Diabetes (engl. schwankend) bezeichnet man einen schwer einstellbaren Diabetes aufgrund unsystematischer, nicht erklärbarer Blutzuckerschwankungen. Nach Beginn einer Insulin-Therapie bei einem Typ-1-Diabetiker kann es zu einer s.g. "Honeymoon-Phase" (eng.: Flitterwochen) kommen. Aus noch nicht vollständig geklärter (u. a. immunologischer) Ursache produziert hierbei das Pancreas des Patienten vorübergehend wieder mehr eigenes Insulin, als vor Therapiestart, sodass der Bedarf an exogenem Insulin zunächst sinkt bzw. vermehrt Hypoglykämien beobachtet werden.[5]
Insulintherapie bei Typ-2-Diabetes
Beim Typ-2-Diabetes liegt zu Beginn kein absoluter Insulinmangel, sondern eine Wirkstörung des Insulins (Insulinresistenz) oder ein relativer Insulinmangel aufgrund von Übergewicht vor, so dass hier eine Insulintherapie erst in dritter Linie indiziert ist. Die initiale Therapie besteht aus einer Schulung und Ernährungsberatung, um durch eine Umstellung der Lebensweise mit regelmäßiger Bewegung und angepasster Ernährung eine Verbesserung der Blutzuckerwerte und ggf. eine Reduktion des Körpergewichts zu erreichen. Bei Misserfolg werden in zweiter Linie orale Antidiabetika eingesetzt, erst bei Versagen dieser Therapie kommt Insulin zusätzlich hinzu.
Die Insulintherapie beim Typ-2-Diabetes führt häufig als unerwünschte Nebenwirkung zu einer Erhöhung des Körpergewichtes, was wiederum zu einer höheren Insulinresistenz führen kann. Insofern muss der übergewichtige Typ-2-Diabetiker versuchen, sein Körpergewicht zu normalisieren und über eine adäquate Ernährung, regelmäßige Bewegung und ggf. orale Antidiabetika die notwendige Insulindosis so niedrig wie möglich zu halten.
Beim Typ-2-Diabetiker lässt sich bald ein relativer Insulinmangel nachweisen, der vor allem die erste Phase der Insulinsekretion nach Nahrungsaufnahme betrifft. Dass die frühe Phase der Insulinsekretion (engl. first-phase insulin secretion) postprandiale Blutzucker-Spitzen „abfedert“, ist ein plausibles pathophysiologisches Konzept ; es wird quasi schon im Anstieg der Meßgröße Blutzucker die Regelgröße Insulin ausgeschüttet. Es bestehen jedoch Zweifel[6], dass diese an den insulin-abhängigen Organen wirksam ankommt. Darüber hinaus gibt es zwar indirekte Hinweise (über Surrogatparameter), jedoch keine direkten Hinweise, dass postprandiale Blutzuckerspitzen einen Einfluss auf die kardiovaskulären Folgen des Diabetes haben[7]. Das liegt insbesondere daran, dass alle bisherigen Medikamente inkl. Insulin sowohl den postprandialen wir den präprandialen Blutzucker senken , was in Studien sauber getrennt werden müsste. Sie sind somit – statistisch gesehen – keine unabhängigen Messgrößen.
Moderne Insulin-Analoga können postprandiale Spitzen der BZ abschwächen, indem sie schneller im Blut anfluten. Es folgten viele Studien über den Nutzen dieser schnell wirksamen Analoga, . Die Cochrane Foundation fand beim Typ-2-Diabetes keine Vorteile von schnell wirksamen Analog-Insulinen gegenüber normalem Humaninsulin, was Hypoglykämien und Spätkomplikationen betrifft[8]. Das hatte Konsequenzen für Preisverhandlungen in Deutschland.
Kriterien der Insulinempfindlichkeit
Der Insulinbedarf schwankt im Laufe des Tages. Morgens ist der Insulinbedarf aufgrund der zeitgleich ausgeschütteten körpereigenen Hormone wie z. B. Cortisol am höchsten. Mittags ist der durchschnittliche Insulinbedarf am niedrigsten, um dann am Abend wieder anzusteigen. Am späten Abend sinkt der Insulinbedarf wieder und erreicht sein absolutes Minimum, um dann ab 3:00 Uhr nachts wieder anzusteigen.
Bei normaler körperlicher Bewegung rechnet man annäherungsweise mit einem Verhältnis von ca. 50 % Basalinsulin und 50 % mahlzeitenbezogenem Insulin. Der durchschnittliche Insulinbedarf wird mit ca. insgesamt 40 E pro Tag berechnet oder nach Körpergewicht bei ca. 0,5 -1,0 Einheiten/kg Körpergewicht.
Die Insulinempfindlichkeit ist von vielen Einzelfaktoren abhängig:
- Art des Insulins (in aufsteigender Reihenfolge: sehr schnell wirkende Analoginsuline, Normalinsuline, NPH-Insuline, langwirksame Analoginsuline)
- Stelle der Insulininjektion (z. B. schnellere Wirkung bei Injektion in den Bauch, langsamer und verzögert bei Injektion in den Oberschenkel)
- Art der Insulingabe (intravenös, intramuskulär, subcutan)
- Länge der Injektionsnadel (die Längen liegen zwischen 4 und 12 mm, eine zu kurze Nadel bringt das Insulin nicht tief genug an die versorgenden Blutgefäße, eine zu lange Nadel kann in den Muskel treffen, das Insulin wirkt schneller)
- Durchblutung der Injektionsstelle (kann durch Sonneneinstrahlung, heißes Bad beschleunigt werden, bei Kälte wird die Wirkung verlangsamt)
- Ausgangsblutzucker (bei hohen Werten besteht eine relative Insulinresistenz, bei tiefen Werten reagiert der Blutzucker sehr empfindlich)
- Nahrungsaufnahme (fett- und eiweißreiche Mahlzeiten lassen den Blutzucker nur langsam ansteigen, schnell resorbierbare Kohlenhydrate schnell)
- Bewegung (Ausdauersport vor- oder nachher lässt den Blutzucker schneller abfallen)
- Alkohol (am Vorabend genossen, kann am frühen Morgen zu Unterzuckerungen führen, da die Leber – statt Glucose freizusetzen – mit dem Alkoholabbau beschäftigt ist)
- Krankheit (ein Infekt erhöht die Insulinresistenz)
- Stress (kann sowohl zu ausgeprägten Blutzuckeranstiegen wie auch zu Unterzuckerungen führen – je nach Reaktionstyp des Menschen)
- Insulindosis (eine hohe Insulindosis auf eine Stelle gespritzt braucht zur maximalen Wirkung länger, als wenn die Dosis auf mehrere Einzelgaben verteilt wird.)
Der Korrekturfaktor gibt an, um wie viel der Blutzucker pro gegebener Einheit Insulin sinkt. Er ermöglicht eine Annäherung, wie viele Einheiten Insulin der Körper benötigt, um von einem höheren Blutzucker auf einen Zielwert zu gelangen. Der Zielbereich liegt bei den meisten Diabetikern zwischen 80 und 120 mg/dl.
Bei normalgewichtigen Erwachsenen und fehlender Insulinresistenz liegt der Korrekturfaktor meist zwischen 30 und 50 mg/dl pro IE Insulin. Bei zierlichen Personen und Kindern ist der Korrekturfaktor jedoch deutlich höher (geringeres Verteilungsvolumen) und bei größeren und dickeren Personen merklich niedriger (höheres Verteilungsvolumen). Die jeweils benötigte Insulindosis muss daher stets durch vorsichtiges Herantasten individuell ermittelt werden.
Bei Übersäuerung des Blutes durch eine hyperglykämische Stoffwechsellage bei absolutem Insulinmangel beim Typ-1-Diabetiker (Ketoazidose) gelten spezielle Regelungen, die mit den Schulungen vermittelt werden.
Geschichte der Insulintherapie
Zu Beginn der Insulintherapie gab es nur tierische Insuline mit der Wirkdauer des Normalinsulins von ca. 4 bis 7 Stunden. Ferner waren Blutzuckerselbsttests lange Jahre nicht machbar, so dass man sich in der ambulanten Medizin viele Jahre mit Urinzuckerkontrollen behelfen musste. Diese zeigen naturgemäß erst sehr zeitverzögert und indirekt die Konzentration des Blutzuckers an. Aufgrund der kurzen Dauer der Wirkung des Insulins strebte man danach, eine Vereinfachung für den Diabetiker zu erzielen. Hans Christian Hagedorn, ein dänischer Forscher, entwickelte 1936 aus Protamin und Schweine-Insulin das erste langwirkende Insulinpräparat, das unter der Bezeichnung Neutral Protamine Hagedorn beziehungsweise NPH-Insulin heute noch verwendet wird (nur nicht mehr in Verbindung mit Insulin aus tierischen Produkten).
Die zunehmende Verbesserung der Blutzuckerselbsttests gestattete den Diabetikern in immer weiterem Ausmaß, ihre Therapie eigenverantwortlich zu übernehmen. In den 1970er-Jahren konnten mit Hilfe von Farbveränderungen der mit Blut benetzten Teststreifen relativ genau die Blutzuckerhöhe bestimmt werden. Dann kamen die ersten handlichen elektrischen Geräte, die nach wenigen Minuten den Wert anzeigten. Heute liegen die Zeiten bei bis unter 5 Sekunden für den Messvorgang.
Begleitend zu den verbesserten Techniken lockerte sich auch das Therapieregime, das in den ersten Jahrzehnten kaum Freiheiten in der Ernährung mit wenig Entscheidungsfreiheit des Patienten kombinierte. Heute ist der Patient aufgefordert, bei fast völliger Freiheit in der Ernährung auch seine Therapie im Idealfall eigenständig zu managen. Und aus der 6-8 Mal täglich notwendigen Gabe von Insulin ist oft genug die Therapie mit einer Insulinpumpe geworden, deren Nadel nur noch alle 2-3 Tage gewechselt werden muss.
Ein wichtiger Meilenstein für die eigenverantwortliche Therapie war die DCCT-Studie, die neben anderen Studien den Beweis erbrachte, dass die selbständige intensivierte Insulintherapie Vorteile im Hinblick auf die Vermeidung von Spätschäden bot.[9]
Literatur
- Helmut Hasche (Hrsg.): Diabetes mellitus im Alter. Ein Handbuch für Pflegeberufe. Schlüter, Hannover 1996, ISBN 3-87706-403-5.
- Michael Nauck, Georg Brabant, Hans Hauner (Hrsg.): Kursbuch Diabetologie. Kurs- und Prüfungsinhalte der Weiterbildung zum Diabetologen (DDG). Kirchheim, Mainz 2005, ISBN 3-87409-403-0.
- Andreas Thomas: Das Diabetes-Forschungs-Buch. Neue Medikamente, Geräte, Visionen. 2. überarbeitete und erweiterte Auflage. Kirchheim + Co, Mainz 2006, ISBN 978-3-87409-411-5.
- Hellmut Mehnert, Eberhard Standl, Klaus-Henning Usadel, Hans-Ulrich Häring (Hrsg.): Diabetologie in Klinik und Praxis. Georg Thieme Verlag. 2003, ISBN 3-13-512805-9; books.google.de.
- Renate Jäckle, Axel Hirsch, Manfred Dreyer: Gut leben mit Typ-1-Diabetes. 7. Auflage. Urban und Fischer-Verlag, 2010, ISBN 978-3-437-45756-2.
- Eva Fritzsche & Sabine Hancl (Hrsg.): Tierisches Insulin – Ein bewährtes Medikament in der modernen Diabetestherapie. Trafo-Verlag, 2006, ISBN 3-89626-616-0.
Weblinks
- Typ-1-Diabetes – Informationen bei Gesundheitsinformation.de (Online-Angebot des Instituts für Qualität und Wirtschaftlichkeit im Gesundheitswesen)
- Typ-2-Diabetes – Informationen bei Gesundheitsinformation.de (Online-Angebot des Instituts für Qualität und Wirtschaftlichkeit im Gesundheitswesen)
- Leitlinien der Deutschen Diabetesgesellschaft
- diabetes-symposium.de (Fachvorträge zu Diabetes)
- modernes-tierisches-insulin.de Tierisches Insulin als lebensnotwendiges Medikament – Website über Schweine- u. Rinderinsulin, Rechtliches, Bezugsquellen u. a.
Einzelnachweise
- Peter Hien, Bernhard Böhm: Diabetes-Handbuch: eine Anleitung für Praxis und Klinik. 5. Aufl. 2007, ISBN 978-3-540-48551-3, S. 178.
- Eintrag zu Exubera, Inhalationspräparat auf ema.europa.eu, der Website der Europäischen Arzneimittelagentur; letzter Abruf am 5. November 2010
- Howorka, Kinga: Funktionelle Insulintherapie. Springer Verlag. 4. Aufl. 1996. ISBN 3-540-60254-2
- Zum grundsätzlichen Versorgungsanspruch vgl. SGB V. Abgerufen am 28. Januar 2011. Die Verordnungspraxis differiert je nach KV, vgl. beta Institut gemeinnützige GmbH: Verordnung von Blutzuckerteststreifen. (PDF; 41 kB) 2014, abgerufen am 10. September 2014.
- Aly H, Gottlieb P: The honeymoon phase: intersection of metabolism and immunology.. In: Current opinion in endocrinology, diabetes, and obesity. 16, Nr. 4, Aug 2009, S. 286–92. doi:10.1097/med.0b013e32832e0693. PMID 19506474.
- A. Caumo , L. Luzi; First-phase insulin secretion: does it exist in real life? Considerations on shape and function: Am J Physiol Endocrinol Metab . 2004 . doi: 10.1152/ajpendo.00139.2003.
- S. Madsbad;Impact of postprandial glucose control on diabetes-related complications:how is the evidence evolving? Journal of Diabetes and Its Complications (2015) doi: 10.1016/j.jdiacomp.2015.09.019
- Fullerton B, et al. Short-acting insulin analogues versus regular human insulin for adult, non-pregnant persons with type 2 diabetes mellitus. Cochrane Database of Systematic Reviews 2018, DOI: 10.1002/14651858.CD013228
- diabetes-deutschland.de UKPDS und DCCT – lohnt sich eine gute Diabeteseinstellung? Aus notabene medici 34 (2004), S. 19–20