Hämine
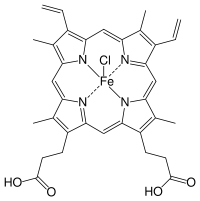
Hämine (Chloroeisen(III)-Porphyrin-Koordinationskomplexe) sind Komplexverbindungen der Häme mit dem Eisen-Ion in der Oxidationsstufe (+III) und einem Chlorid-Ion als axialen Liganden.
Eigenschaften

Das Hämin b des Häm b wird kurz als Hämin[1] bezeichnet (Summenformel C34H32N4O4·FeCl, Molmasse 651,94 g/mol). Es bildet längliche, dünne Plättchen oder charakteristisch abgeschrägte Prismen, die in Durchsicht braun, bei Auflicht stahlblau glänzend erscheinen.
Hämin a bildet grüne Kristalle.
Hämine sind in Wasser und verdünnten Säuren unlöslich, in starken Basen dagegen löslich. Hämine bilden in anorganischen Basen Hämatine, in organischen Basen Hämi- bzw. Hämochrome.
Geschichte
Der Krakauer Anatom Ludwig Karol Teichmann (Ludwik Karol Teichmann-Stawiarski; 1823–1895)[2] kristallisierte 1853 erstmals Hämin aus Blut.[3][4] Für die Synthese des Hämins erhielt der deutsche Chemiker Hans Fischer 1930 den Nobelpreis für Chemie.[5]
Nachweis
Hämin in Form typischer Kristalle[6] entsteht beim sogenannten Teichmann-Test[7] aus Hämoglobin beim Erhitzen mit Essigsäure (Eisessig, gesättigt mit Kochsalz) zum Nachweis von Blutspuren.
Verwendung
Humanes, aus menschlichem Blut gewonnenes Hämin wird in Form eines Infusionslösungskonzentrats (Normosang, Orphan Europe, Frankreich) zur Behandlung akuter Schübe bei Patienten mit akuter hepatischer Porphyrie eingesetzt und unterliegt der ärztlichen Verschreibungspflicht. Porphyrien sind meist angeborene Bildungsstörungen der Häm-Gruppe, gekennzeichnet durch den teilweisen Ausfall von Enzymen, die die 8 nacheinander folgenden Schritte des Häm-Aufbaus katalysieren. Die Häm-Gruppe kommt hauptsächlich im Hämoglobin (roter Blutfarbstoff) vor, aber auch in Enzymen wie dem Cytochrom P450, das unter anderem beim Abbau/Entgiftung von Xenobiotika (z. B. Medikamente) in der Leber eine Rolle spielt. Müssen vermehrt Medikamente abgebaut werden, kommt es zu einem erhöhten Bedarf an Cytochrom P450 und einer positiven Rückkopplung auf den Häm-Syntheseweg. Bei einer Störung des Synthesewegs aber führt die positive Rückkopplung zu einer Anreicherung des Stoffwechselproduktes, das nicht mit der normalen Rate umgesetzt (weiterverarbeitet) werden kann und ein Porphyrie-Schub entsteht (Porphyrinvorläufer sind toxisch für den Körper).
Hämin-Arginat besetzt die positive Rückkopplungsstelle im Syntheseweg (es suggeriert dem Körper, dass eine ausreichende Menge Häm vorhanden ist) und bewirkt eine Entkopplung der Rückkopplung.
Siehe auch
Einzelnachweise
- Externe Identifikatoren von bzw. Datenbank-Links zu Hemin: CAS-Nummer: 16009-13-5, EG-Nummer: 240-140-1, ECHA-InfoCard: 100.036.475, PubChem: 455658, ChemSpider: 21160444, DrugBank: DB03404, Wikidata: Q425165.
- J. Stahnke: Ludwik Teichmann (1823–1895). Anatom in Krakau. In: Würzburger medizinhistorische Mitteilungen 2, 1984, S. 205–267.
- L. Teichmann: Ueber die Krystallisation der organischen Bestandtheile des Bluts. In: Zeitschrift für rationelle Medicin (neue Folge). Band 3, Nr. 3, 1853, S. 375–388 (Vollansicht in der Google-Buchsuche).
- Ludwik Teichmann: Über das Hämatin. In: Zeitschrift für rationelle Medizin, Neue Folge 8, 1859, S. 141–148.
- Informationen der Nobelstiftung zur Preisverleihung 1930 an Hans Fischer (englisch).
- Jürgen Thorwald: Die Stunde der Detektive. Werden und Welten der Kriminalistik. Droemer Knaur, Zürich und München 1966, S. 31–35.
- J. Stahnke: Häminkristalle. Ludwik Teichmanns Blutnachweis. In: Medizinhistorisches Journal. Band 16, 1981, S. 391–413.