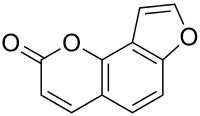
Furocumarine
Furocumarine (auch Furanocumarine) kommen häufig in Doldenblütlern vor wie Bärenklau (Riesen-Bärenklau, Wiesen-Bärenklau) und Arznei-Engelwurz, außerdem in Rautengewächsen wie Zitruspflanzen (darunter Bergamotte, Zitrone, Limette, Grapefruit, Bitterorange u. a.) sowie in einer Reihe weiterer Pflanzen. Furocumarine gehören zu den sekundären Pflanzenstoffen und dienen als Phytoalexine (ein Typ Abwehrstoffe).
Eigenschaften
Im Grundgerüst der Furocumarine ist Cumarin mit einem Furanring anelliert. Bekannte Furocumarine sind Psoralen, Bergapten und Xanthotoxin. In der Rautenart Ruta chalepensis wurde unter anderem auch Chalepensin[1] (Xylotensin) festgestellt.
Wie die meisten α,β-ungesättigten Carbonylverbindungen sind Furocumarine sehr reaktiv. Unter Einwirkung von Sonnenlicht (UVA- und UVB-Strahlung) werden Furocumarine photoaktiviert. Prominentes Beispiel ist der giftige Saft des Riesen-Bärenklaus (Herkulesstaude). Die darin enthaltenen Furocumarine schädigen den menschlichen Organismus auf zweierlei Weise:
- Photosensibilisierend/Phototoxisch: Gelangen Furocumarine auf die Haut und werden anschließend dem Sonnenlicht (UV-Strahlung) ausgesetzt, kommt es je nach Schwere zu verbrennungsähnlichen Symptomen (Hautrötung, Schwellung, Blasenbildung, Läsionen, Photopigmentierung, Narbenbildung).[2][3] Siehe auch Berloque-Dermatitis, Photodermatitis.
- Krebserregend: Furocumarine gehen unter UV-Einwirkung kovalente Bindungen mit den Pyrimidinbasen der DNA ein, vernetzen so die DNA-Doppelstränge irreversibel miteinander (DNA-Vernetzung) und wirken dadurch krebserregend.[4][5][6]
In der Medizin werden Furocumarine wie Bergapten, Trioxsalen, Xanthotoxin oder Trimethylpsoralen zur Behandlung von Psoriasis im Rahmen der Phototherapie und Photochemotherapie eingesetzt.[3]
Übersicht[7]
| Psoralen-Typ | |||||
| Bild | 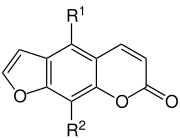 | ||||
| Name | Psoralen | Bergapten | Xanthotoxin | Isopimpinellin | Imperatorin |
| R1 | H | OCH3 | H | OCH3 | H |
| R2 | H | H | OCH3 | OCH3 | O–CH2–CH=C(CH3)2 |
| CAS-Nummer | 66-97-7 | 484-20-8 | 298-81-7 | 482-27-9 | 482-44-0 |
| PubChem | 6199 | 2355 | 4114 | 68079 | 10212 |
| Summenformel | C11H6O3 | C12H8O4 | C12H8O4 | C13H10O5 | C16H14O4 |
| Molare Masse | 186,16 g·mol−1 | 216,19 g·mol−1 | 216,19 g·mol−1 | 246,21 g·mol−1 | 270,28 g·mol−1 |
| Angelicin-Typ | ||||
| Bild | 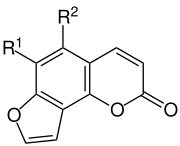 | |||
| Name | Angelicin | Pimpinellin | Isobergapten | Sphondin |
| R1 | H | OCH3 | H | OCH3 |
| R2 | H | OCH3 | OCH3 | H |
| CAS-Nummer | 523-50-2 | 131-12-4 | 482-48-4 | 483-66-9 |
| PubChem | 10658 | 4825 | 68082 | 108104 |
| Summenformel | C11H6O3 | C13H10O5 | C12H8O4 | C12H8O4 |
| Molare Masse | 186,16 g·mol−1 | 246,21 g·mol−1 | 216,19 g·mol−1 | 216,19 g·mol−1 |
Vorkommen in der Natur (Auswahl)
_white_bg.jpg.webp) Grapefruit
Grapefruit Orange
Orange Zitrone
Zitrone Arznei-Engelwurz (Angelica archangelica)
Arznei-Engelwurz (Angelica archangelica) Riesen-Bärenklau (Heracleum mantegazzianum)
Riesen-Bärenklau (Heracleum mantegazzianum) Wiesen-Bärenklau (Heracleum sphondylium)
Wiesen-Bärenklau (Heracleum sphondylium)
Einzelnachweise
- R. M. Brooker, J. N. Eble, N. A. Starkovsky: Chalepensin, chalepin and chalepin acetate, three novel furocoumarins from Ruta chalepensis. In: Lloydia. Band 30, 1967, S. 73.
- Furanocoumarins as potent chemical defenses.
- Jeannette Aryee-Boi: Dusch-PUVA : Ein innovatives Verfahren der lokalen PUVA-Therapie Klinische und pharmakokinetische Ergebnisse bei Psoriasis vulgaris. Inaugural-Dissertation Freie Universität Berlin, 2002.
- Oskar Schimmer: Die mutagene und cancerogene Potenz von Furocumarinen. In: Pharmazie in unserer Zeit. Band 10, Nr. 1, 1981, S. 18–28.
- Eberhart Teuscher: Biogene Gifte. 1987, S. 233.
- Andreas Herde: Untersuchung der Cumarinmuster in Früchten ausgewählter Apiaceae. (PDF 2,3 MB) Dissertation Universität Hamburg, 2005, S. 29 f.
- Eintrag zu Furocumarine. In: Römpp Online. Georg Thieme Verlag, abgerufen am 19. Mai 2015.
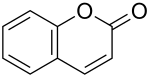
chromen-7-one_200.svg.png.webp)