Eisleb-Alkylierung
Die Eisleb-Alkylierung ist eine Namensreaktion in der Organischen Chemie, welche 1941 erstmals von dem deutschen Chemiker Otto Eisleb (1887–1948) vorgestellt und nach ihm benannt wurde.[1]
Übersichtsreaktion
Bei dieser Reaktion handelt es sich um eine Alkylierung von Verbindungen mit aktiven Wasserstoff mittels eines Alkylhalogenids und der Behandlung mit Natriumamid. CH-acide Verbindungen sind dabei u. a. Desoxybenzoin, Diphenylmethan, Phenylacetonitril, Fluoren, Benzylphenylsulfon und 2-Pyridylacetonitril.[1]
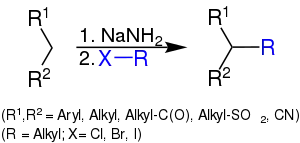
Reaktionsmechanismus
In dieser Reaktion wird durch das Natriumamid zunächst ein Proton abstrahiert, wobei ein Carbanion entsteht. Aus dem Amid entsteht in diesem Schritt Ammoniak. Anschließend kann ein nucleophiler Angriff auf den positiv polarisierten Alkyl-Rest des Alkylhalogenids erfolgen. Das Natriumhalogenid kann entfernt werden und das alkylierte Produkt bleibt übrig.[1]

Beispielreaktion
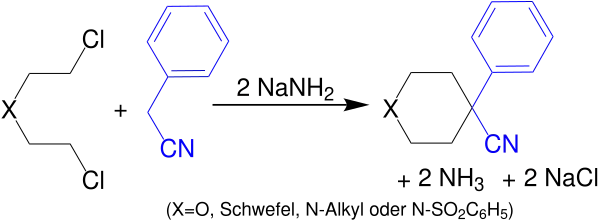
Eisleb beschreibt die Reaktion selbst für die Dialkylierung von Benzylcyanid mittels Natriumamid unter Bildung von Heterocyclen. Dies kann mit Verbindungen aus der Gruppe der Loste erfolgen:[2]
Anwendung
Diese Reaktion wird zur Alkylierung von Verbindungen mit aktiven Wasserstoffatomen verwendet.[1]
Einzelnachweise
- Zerong Wang: Eisleb Alkylation. In: Comprehensive Organic Name Reactions and Reagents. Wiley, 2010, ISBN 978-0-470-63885-9, S. 974–976, doi:10.1002/9780470638859.conrr211.
- Otto Eisleb: Neue Synthesen mittels Natriumamids. In: Berichte der deutschen chemischen Gesellschaft (A and B Series). Band 74, Nr. 8, 6. August 1941, S. 1433–1450, doi:10.1002/cber.19410740814.