Calciumnitrid
Calciumnitrid ist eine anorganische chemische Verbindung des Calciums aus der Gruppe der Nitride.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
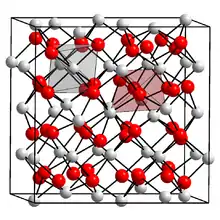 | ||||||||||||||||
| _ N3− _ Ca2+ | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Calciumnitrid | |||||||||||||||
| Verhältnisformel | Ca3N2 | |||||||||||||||
| Kurzbeschreibung |
Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 148,25 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
2,63 g·cm−3 (25 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Calciumnitrid kann durch Reaktion von Calcium (unter anderem auch bei dessen Verbrennung an Luft[2]) mit Stickstoff gewonnen werden.[3]
Ebenso kann es durch Zersetzung von Calciumamid gewonnen werden.[4]
Eigenschaften
Calciumnitrid liegt je nach Darstellungstemperatur schwarz bis goldgelb oder in Mischfarben vor. α-Calciumnitrid (C-Sesquioxid-Typ bzw. Anti-Bixbyit-Struktur, Raumgruppe Ia3 (Raumgruppen-Nr. 206) mit dem Gitterparameter a = 10,40 Å[4]) geht bei 700 °C in β-Calciumnitrid über.
Mit Wasser erfolgt Zersetzung zu Calciumhydroxid und Ammoniak.[3]
Einzelnachweise
- Datenblatt Calcium nitride, −200 mesh, 95% bei Sigma-Aldrich, abgerufen am 31. Oktober 2021 (PDF).
- Mary Eagleson: Concise Encyclopedia Chemistry. Walter de Gruyter, 1994, ISBN 3-11-011451-8, S. 160 (eingeschränkte Vorschau in der Google-Buchsuche).
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 929.
- Richard C. Ropp: Encyclopedia of the Alkaline Earth Compounds. Newnes, 2012, ISBN 0-444-59553-8, S. 205 (eingeschränkte Vorschau in der Google-Buchsuche).
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. The authors of the article are listed here. Additional terms may apply for the media files, click on images to show image meta data.

