Boride
Bei Boriden handelt es sich um chemische Verbindungen, die das Element Bor enthalten und bei denen der Reaktionspartner in der Regel eine niedrigere Elektronegativität besitzt. Eine Ausnahme würde zum Beispiel das Arsenborid darstellen. Gegenbeispiele sind Bornitrid und Borcarbid, die rein formal nicht zu den Boriden gezählt werden.
Bei den meisten Boriden handelt es sich um Verbindungen mit Metallen, von denen viele keramische Eigenschaften aufweisen und so zu den Nichtoxidkeramiken gezählt werden. Beispielsweise haben die Boride von Titan und Zirconium gegenüber den entsprechenden Metallen eine vielfach höhere elektrische und thermische Leitfähigkeit. Dieses Phänomen erklärt sich, wie später näher erläutert, durch ihre Struktur.
Herstellung
Es gibt diverse Möglichkeiten, Boride im industriellen Maßstab herzustellen. Die drei gängigsten sind die Bildung durch:
- die Vereinigung der Elemente oder Reaktion des Hydrides mit Bor
- die Elektrolyse geschmolzener Salze
- die Reduktion der entsprechenden Metalloxide mit Kohlenstoff und Borcarbid
Bindungsverhältnisse bei den Boriden
Die Veranschaulichung der Bindungsverhältnisse bei Boriden ist ein komplexeres Thema. Die Bindungsmodelle ändern sich mit steigendem Boranteil wie im Folgenden kurz benannt (von niedrigem zu hohem Gehalt):
- Boride mit isolierten Boratomen, sogenannte borarme Boride (z. B. M4B, M3B, M2B, M5B2, M5B3, M7B3)
- Boride mit Einfach- und Doppelketten von Boratomen
- Boride mit zweidimensionalem Netzwerken (MB2, M2B5)
- Boride mit dreidimensionalem Netzwerken (MB4, MB6, MB12)
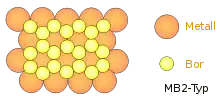
Dabei enthält die dritte Gruppe einige der am besten stromleitenden, härtesten und höchstschmelzenden Typen wie das Titanborid (TiB2). Aufgebaut ist dieser Typ durch alternierende Schichten dichtest-gepackter Metallatome und hexagonaler Bornetzwerke wie in der nachfolgenden Abbildung dargestellt. Durch den Schichtaufbau erklären sich die guten oben erwähnten Leitfähigkeiten.
Verwendung
Die Verwendung der Boride beschränkt sich in der Regel auf Spezialanwendungen, da es häufig günstigere Verbindungen mit ähnlichen Materialeigenschaften gibt. Bedeutsam sind jedoch die Boride der Lanthanoiden, welche sich als hervorragende Elektronenemitter eignen. Wegen ihrer Härte, ihrer chemischen und thermischen Resistenz sind die Boride Werkstoffe mit höchsten Ansprüchen und werden beispielsweise in Hochtemperaturöfen, Turbinenflügeln und Raketendüsen eingesetzt. Das wohl bedeutsamste Borid ist Titanborid (TiB2), welches sich durch seine hohe Härte, den hohen Schmelzpunkt bei über 3200 °C und seine elektrische Leitfähigkeit auszeichnet und unter entsprechenden Extrembedingungen Anwendung findet.
Im Jahr 2001 wurde entdeckt, dass Magnesiumdiborid MgB2 ein Supraleiter mit einer kritischen Temperatur von TC = 39 K ist. Dieses Material besitzt alle Voraussetzungen (gute Verarbeitbarkeit, hohe kritische Stromdichte, hohes kritisches Magnetfeld) um das bisher kommerziell als Tieftemperatursupraleiter (z. B. in MRT-Geräten) verwendete Triniobzinn Nb3Sn in den nächsten Jahren zu ersetzen. Durch Dotierung mit Kohlenstoff kann die kritische Temperatur noch um einige Kelvin erhöht werden.
Lanthanhexaborid (LaB6) hat eine extrem niedrige Elektronenaustrittsarbeit.[1] Keramiken aus Lanthanhexaborid finden in der Plasmatechnik und in einigen Elektronenmikroskopen als Elektronenquelle Verwendung.[2]
Beispiele
Literatur
Einzelnachweise
- Lexikon der Physik: Austrittsarbeit
- sindlhauser.de: PeroLan - Kathoden Lanthanhexaborid (LaB6) - Kathoden für die Plasmatechnik (Memento vom 17. März 2011 im Internet Archive)