Boekelheide-Reaktion
Die Boekelheide-Reaktion ist eine Namensreaktion der organischen Chemie. Es ist die zweistufige Umsetzung von 2-Methylpyridin-N-oxid zu 2-Hydroxymethylpyridin und analoger Umwandlungen.
Sie wurde nach dem US-amerikanischen Chemiker Virgil Boekelheide (1919–2003) benannt, welcher die Reaktion 1954 erstmals publizierte.[1]
Übersichtsreaktion
Bei der Reaktion wird 2-Methylpyridin-N-oxid 1 mit Trifluoressigsäureanhydrid behandelt, sodass es zur Umlagerung kommt und als Produkt nach der hydrolytischen Aufarbeitung letztendlich 2-Hydroxymethylpyridin 2 erhalten wird:
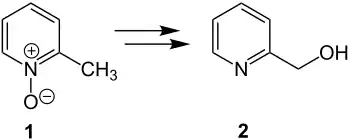
Reaktionsmechanismus
Folgender Reaktionsmechanismus wird in der Literatur[2] beschrieben:
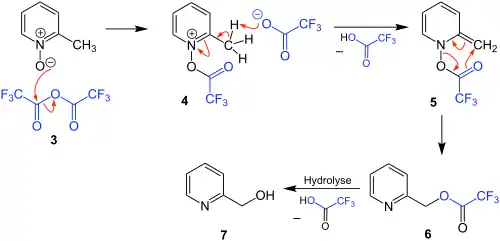
Ein freies Elektronenpaar des negativ geladenen Sauerstoffatoms lagert sich an das Trifluoressigsäureanhydrid 3 an. Dadurch kommt es zur Elektronenumlagerung im Trifluoressigsäureanhydrid, sodass dieses gespalten wird. Die dabei entstehende Zwischenstufe 4 wird im nächsten Schritt deprotoniert und Trifluoressigsäure abgespalten. Dabei entsteht die Zwischenstufe 5. Eine [3.3]-sigmatrope Umlagerung von 5 führt zum Trifluoracetylester 6. Die darauffolgende Hydrolyse führt zu einer weiteren Abspaltung eines Trifluoressigsäuremoleküls, als Produkt wird 2-Hydroxymethylpyridin 7 erhalten.
Anwendungsbeispiele
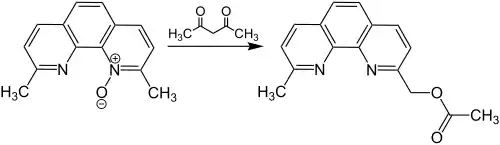
Diese Reaktion zeigt auf, dass die Boekelheide-Reaktion nicht nur mit Trifluoressigsäureanhydrid funktioniert. Auch die Reaktion mit Essigsäureanhydrid ist möglich. Zudem kann die Reaktion auch schon eher gestoppt werden, sodass als Produkt ein Ester erhalten wird.[3]
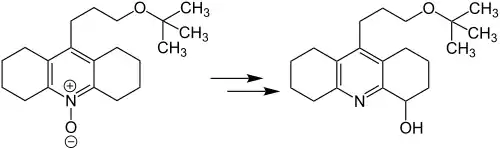
An dieser Reaktion ist zu erkennen, dass als Edukt nicht nur 2-Methylpyridin-N-oxid gewählt werden kann. Die Reaktion ist auch mit anderen Aminoxiden möglich.[4]
Einzelnachweise
- V. Boekelheide und W. J. Linn: Rearrangements of N-Oxides. A Novel Synthesis of Pyridyl Carbinols and Aldehydes In: Journal of the American Chemical Society 76, 1954, S. 1286–1291, doi:10.1021/ja01634a026.
- Jie Jack Li: Name Reactions, Springer, 2006, ISBN 978-3-642-01052-1, S. 54–56, doi:10.1007/978-3-642-01053-8_131.
- G. R. Newkome, K. J. Theriot, V. K. Gupta, F. R. Fronczek, G. R. Baker: 124. Mono-.alpha.-functionalization of 2,9-dimethyl-1,10-phenanthroline In: The Journal of Organic Chemistry 54, 1989, S. 1766–1769, doi:10.1021/jo00268a055.
- C. Fontanes, E. Bejan, H. A. Haddou, G. G. A. Belavoine: The Boekelheide Reaction: Trifluoroacetic Anhydride as a Convenient Acylating Agent In: Synthetic Communications 25, 1995, S. 629–633, doi:10.1080/00397919508011399.