Porphobilinogen-Desaminase
Porphobilinogen-Deaminase (PBG-D) (auch: Hydroxymethylbilan-Synthase, HMBS) ist das Enzym, das in allen Lebewesen die Eliminierungsreaktion und anschließende Polymerisation von vier Porphobilinogen-Molekülen zu Hydroxymethylbilan katalysiert. PBG-D ist daher notwendig für die Porphyrin-Biosynthese. Mutationen am HMBS-Gen des Menschen mit folgendem Mangel an PBG-D können zur akuten intermittierenden Porphyrie führen.[1]
| Porphobilinogen-Desaminase | ||
|---|---|---|
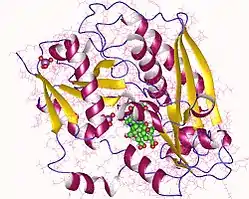 | ||
| Porphobilinogen desaminase monomer, Human | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 361 Aminosäuren | |
| Kofaktor | Dipyrromethan | |
| Isoformen | 2 | |
| Bezeichner | ||
| Gen-Name | HMBS | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 2.5.1.61, Transferase | |
| Substrat | 4 Porphobilinogen + H2O | |
| Produkte | Hydroxymethylbilan + 4 NH3 | |
| Vorkommen | ||
| Homologie-Familie | PBG-D | |
| Übergeordnetes Taxon | Lebewesen | |
Von PBG-D gibt es beim Menschen zwei Isoformen, eine nur in Erythrozyten anzutreffende, die andere wird in den restlichen Gewebetypen exprimiert.
Katalysierte Reaktion
4 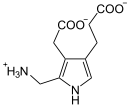 + H2O ⇒
+ H2O ⇒
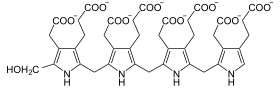 + 4 NH3
+ 4 NH3
Vier Moleküle Porphobilinogen polymerisieren zu einem Molekül Hydroxymethylbilan, wobei Wasser verbraucht wird und Ammoniak entsteht. Als Kofaktor ist Dipyrromethan notwendig, das gebunden wird und an welches die einzelnen Porphobilinogen-Moleküle zuerst schrittweise addiert werden.[1]
Weblinks
- Jassal, D'Eustachio / reactome: Four PBGs combine through deamination to form hydroxymethylbilane (HMB)
- OMA: PBG-D Homologe