Ortho-Metallierung
Unter einer Ortho-Metallierung (oder auch englisch directed ortho metalation und abgekürzt DoM) versteht man die Metallierung von entsprechend substituierten Aromaten mit Alkyllithiumverbindungen. Die Substituenten werden als direct metalation group (oder abgekürzt DMG) bezeichnet und dirigieren die Metallierung, durch ihre intermediäre Deprotonierung, in die ortho-Position des Aromaten.[1] Beispiele für DMG sind Gruppen wie Methylether, tertiäre Amine oder die Amid-Gruppe.
Mechanismus
Der Aromat mit einer DMG-Gruppe tritt in Wechselwirkung mit der Organolithium-Verbindung wie n-Butyllithium und bricht das Aggregationscluster (R-Li)n auf. Dies aktiviert die Organolithium-Verbindung in direkter Nachbarschaft zum ortho-ständigen Wasserstoffatom so, dass es von dem Carbanion abstrahiert wird und damit das entsprechende Kohlenstoff-Atom metalliert wird. Da es sich bei der DMG um eine Lewis-Base handelt und Lithium-Kationen Lewis-Säuren sind, wird der metallierte Aromat stabilisiert.
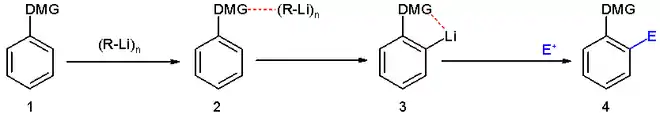
In einem weiteren Schritt wird dieser metallierte Aromat dann mit einem Elektrophil umgesetzt und es wird das Produkt einer normalen nucleophilen Substitution oder Addition erhalten.
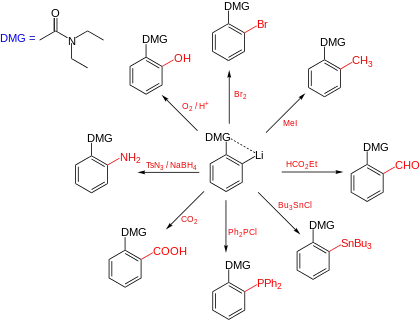
Diese Art der Reaktion wurden unabhängig voneinander von Henry Gilman[2] und Georg Wittig[3] im Jahr 1939 bzw. 1940 publiziert.
Einzelnachweise
- V. Snieckus: In Directed ortho metalation. Tertiary amide and O-carbamate directors in synthetic strategies for polysubstituted aromatics Chem. Rev. 1990, 90, 879-933.
- H. Gilman, R.L. Bebb: In Relative Reactivities of Organometallic Compounds. XX.* Metalation J. Am. Chem. Soc. 1939, 61, 109-112.
- G. Wittig et al. Chem. Ber. 1940, 73, 1197.