Miller-Dieker-Syndrom
Beim Miller-Dieker-Syndrom (MDS, auch Miller-Dieker-Lissenzephalie oder 17-p-Syndrom) handelt es sich um ein Krankheitsbild als Folge einer Chromosomenanomalie im Chromosom 17. In der Folge kommt es zu einer schweren Fehlentwicklungen des Großhirns in der Embryonalphase. Das Miller-Dieker-Syndrom geht häufig mit weiteren Entwicklungsfehlern einher. Die Erstbeschreibung erfolgte 1963 durch James Quinter Miller[1] sowie 1969 durch Hans Dieker.[2]
| Klassifikation nach ICD-10 | |
|---|---|
| Q93.5 | Chromosomenanomalie |
| ICD-10 online (WHO-Version 2019) | |
Epidemiologie
Das Miller-Dieker-Syndrom stellt eine seltene Erkrankung dar und kommt in weniger als 1,2:100.000 Lebendgeburten vor.[3] In 20 % der Fälle liegt eine balancierte Translokation des betroffenen Genabschnittes bei den Eltern vor.[4] 80 % der Fälle stellen eine Neumutation dar.[4] Liegt bei den Eltern eine balancierte Translokation vor, so liegt das Risiko für das Auftreten eines Miller-Dieker-Syndroms beim Kind bei bis zu 25 %.[5]
Entstehung und Pathophysiologie
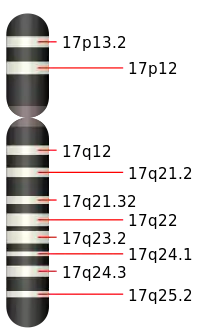
Ursache für die Entstehung eines Miller-Dieker-Syndroms ist eine Chromosomenaberration mit Mikrodeletionen im terminalen kurzen Arm von Chromosom 17 im Genlocus p13.3.[6] Hierdurch kommt es in der embryonalen Gehirnentwicklung zu einer Migrationsstörung der Nervenzellen der Großhirnrinde. Die ab der 22. Woche der Embryonalentwicklung stattfindenden Schritte in der Gehirnentwicklung, bei der sich die Hirnfurchen ausbilden, bleiben teilweise oder ganz aus.[7] Dadurch, dass es sich beim Miller-Dieker-Syndrom um ein Contiguous gene syndrome handelt, bei dem mehrere dicht beieinander liegende Gene betroffen sein können, kommt es je nach Ausprägung des Defektes zu weiteren genetisch bedingten Fehlbildungen.[8]
Diagnostik
Die Diagnose kann mittels zytogenetischer Testung von im Rahmen einer Amniozentese gewonnenem Fruchtwasser gestellt werden.[5] Ab der 26. Schwangerschaftswoche kann die Diagnose per Sonografie gestellt werden. Hierbei können neben einer Mikrocephalie und Agyrie auch Erweiterungen der Hirnventrikel, eine abnormale Schädelform, ein Hydramnion, Ohrmuschel- und Nasenveränderungen sowie eine generelle Wachstumsverzögerung sichtbar sein. Je nach Ausmaß der Chromosomenschädigung können mögliche Herzfehler, Nieren- oder Magendarmfehlbildungen sowie ein Kryptorchismus darstellbar sein.[5] Das Ausmaß der Hirnschädigung kann vorgeburtlich entweder durch eine Magnetresonanztomographie-Untersuchung oder durch vaginale Sonografie ermittelt werden.[5] Nach der Geburt kann die Diagnose mittels genetischer Untersuchung durch Fluoreszenz-in-situ-Hybridisierung oder DNA-Microarray gestellt werden.[8] Eine Magnetresonanztomographie kann das Ausmaß der Lissenzephalie zeigen.[4]
Klinik

Kinder, die mit dem Miller-Dieker-Syndrom geboren werden weisen eine schwere geistige Behinderung auf. Typisch ist eine ausgeprägte muskuläre Hypotonie sowie eine ausgeprägte Neigung zu epileptischen Anfällen.[5] Die Kinder haben oft massive Atemwegs- und Schluckprobleme.[4] Das Erscheinungsbild ist geprägt durch eine Mikrocephalie mit einer hohen Stirn und hervorstehendem Hinterhaupt. Im Bereich der Schläfen finden sich beidseits Eindellungen. Das Gesicht weist eine schmale Oberlippe mit einem auffällig langen Philtrum auf. Es finden sich Ohrmuscheldysplasien sowie eine breite Nasenwurzel.[5] Im Gehirn finden sich aufgehobene Furchen und Falten bis hin zum Vollbild einer Lissenzephalie. Die Hirnrinde ist verdickt und es finden sich erweiterte Hirnventrikel.[5] Es kann eine Balkenagenesie oder -hypoplasie vorliegen.[9] Begleitend können je nach Ausmaß der mitbeteiligten Gene eine Mikrogenie, Herzfehler wie z. B. eine Fallot-Tetralogie, Nierenfehlbildungen, Fehlbildungen des Magen-Darm-Traktes, ein Kryptorchismus, Korneatrübungen sowie Kampto- und Klinodaktylien auftreten.[5]
Therapie
Eine kausale Therapie des Miller-Dieker-Syndroms ist nicht möglich. Liegt bei den Eltern eine balancierte Dislokation auf dem Chromosom 17 vor sollte eine genetische Beratung erfolgen. Eine erneute Schwangerschaft kann durch künstliche Befruchtung mit Präimplantationsdiagnostik erfolgen. Bei einer Krankheitsentstehung durch eine Neumutation ist das Risiko für ein erneutes Auftreten eines Miller-Dieker-Syndroms nicht erhöht.[9][4] Die Therapie betroffener Kinder ist symptomatisch und beinhaltet die Behandlung der Epilepsie, Prophylaxe von Pneumonien und anderen Atemwegserkrankungen sowie Ernährung mittels Magensonde.[4]
Prognose
Die meisten Betroffenen sterben im Kleinkindalter an den Folgen der Ernährungsprobleme, an aspirationsbedingten Atemwegserkrankungen und allgemeinen Infekten oder den Folgen der ständigen epileptischen Anfälle.[4] Die meisten Kinder sterben bis zum Alter von zwei Jahren, wenige erreichen ein Alter von zehn Jahren.[4] Der bis 2015 älteste bekannte Fall erreichte ein Alter von 17 Jahren. Zurzeit gibt es einen jungen Mann, der 1992 geboren wurde.[4]
Weblinks
- Miller-Dieker-syndrome in der Genetics Home Reference der United States National Library of Medicine
- Miller-Dieker-Syndrom in der Online Mendelian Inheritance in Man
- Miller-Dieker-Syndrom in der Diseases Database
- Miller-Diekes-Syndrom in der MeSH-Datenbank der United States National Library of Medicine
Einzelnachweise
- J. Q. Miller: LISSENCEPHALY IN 2 SIBLINGS. In: Neurology. Band 13, Oktober 1963, S. 841–850, ISSN 0028-3878. PMID 14066999.
- H. Dieker, R. H. Edwards, G. ZuRhein u. a.: The lissencephaly syndrome. In: Birth defects Orig Art. Ser V, 1969 (2), S. 53–64.
- Miller-Dieker-Syndrom auf Orphanet
- William B. Dobyns, Soma Das: LIS1-Associated Lissencephaly/Subcortical Band Heterotopia. GeneReviews 3. März 2009
- Michael Entezami, Matthias Albig, Adam Gasiorek-Wiens, Rolf Becker: Sonographische Fehlbildungsdiagnostik: Lehratlas der fetalen Ultraschalluntersuchung. Georg Thieme Verlag, 2002, S. 248
- W. B. Dobyns: Developmental aspects of lissencephaly and the lissencephaly syndromes. In: Birth defects original article series. Band 23, Nummer 1, 1987, S. 225–241, ISSN 0547-6844. PMID 3472611.
- Birgit Ertl-Wagner: Pädiatrische Neuroradiologie. Springer 2007 S. 25
- Gerhard Jorch: Fetoneonatale Neurologie: Erkrankungen des Nervensystems von der 20. SSW bis zum 20. Lebensmonat. Georg Thieme Verlag, 2013, S. 206
- Jürgen Kunze: Wiedemanns Atlas klinischer Syndrome: Phänomenologie, Ätiologie, Differenzialdiagnose. Schattauer Verlag, 2010, S. 88