Log cell kill
Mit dem englischen Begriff Log cell kill, oft auch Fractional cell kill oder Fractional kill genannt, wird eine Hypothese in der Onkologie bezeichnet. Es gibt derzeit keine adäquate deutschsprachige Bezeichnung für die Hypothese, die besagt, dass bei jedem Zyklus einer Chemotherapie oder Strahlentherapie der gleiche Anteil, aber nicht die gleiche absolute Anzahl an Krebszellen abgetötet wird.
Erläuterung
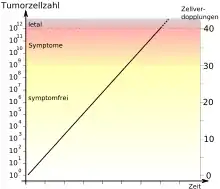
Die Log-cell-kill-Hypothese wurde anhand von Versuchen mit leukämischen Mäusen 1964 durch Howard E. Skipper und Kollegen aufgestellt.[1][2] Bei einer Leukämie vermehren sich die Krebszellen exponentiell, das heißt die Zeitspanne zur Verdopplung der Krebszellen ist konstant. Im halblogarithmischen Tumorzellzahl/Zeit-Diagramm entspricht dies einer Geraden (siehe Diagramm 1). Bei der Behandlung dieser Mäuse mit Chemotherapeutika wurde festgestellt, dass bei der gleichen Dosis die Anzahl der Krebszellen logarithmisch (log) abnimmt.[3] Werden bei der ersten Gabe des Chemotherapeutikums 99 % der Krebszellen abgetötet, so nimmt die Zahl an Krebszellen beispielsweise von 109 auf 107 ab, was zwei Größenordnungen (log-Schritten) entspricht. Bei der zweiten Gabe werden wiederum 99 % der Krebszellen abgetötet. Die Zahl der Krebszellen nimmt dabei von 107 auf 105 ab. Allerdings sind – im Vergleich zum ersten Zyklus – absolut betrachtet erheblich weniger Krebszellen abgetötet worden; eine Milliarde im ersten Zyklus gegenüber 10 Millionen im zweiten. In diesem idealisierten Modell bleibt der Anteil abgetöteter Krebszellen konstant (99 %), aber die absolute Anzahl abgetöteter Krebszellen wird immer geringer.[4]
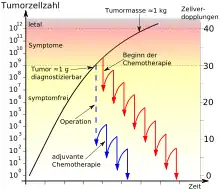
Die blaue Kurve stellt den Verlauf nach einer operativen Tumorentfernung mit adjuvanter Chemotherapie dar. Die rote Kurve den Verlauf bei einem nicht operablen Tumor und Chemotherapie.
Von der ersten entarteten Zelle bis zum nachweisbaren Tumor werden etwa 30 Zellteilungszyklen benötigt (= 109 Krebszellen mit 1 g Masse). Von diesem Punkt bis zur normalerweise tödlichen Tumormasse von ungefähr 1 kg (= 1012 Krebszellen) werden nur noch 10 weitere Teilungszyklen benötigt.[5]
Dieser Sachverhalt ist der Grund dafür, dass bei einer Chemotherapie im Verlauf der Behandlungszyklen die Dosis nicht herabgesetzt werden sollte, selbst wenn kein Tumor mehr diagnostizierbar ist. Die Diagnosegrenze liegt bei etwa 109 Zellen, was einer Tumormasse von ungefähr 1 Gramm entspricht. In Diagramm 2 ist diese Grenze durch die untere waagerechte gestrichelte Linie angedeutet. Eine zu geringe Dosis würde zudem die widerstandsfähigsten Tumorzellen selektieren, die sich dann weiter vermehren und auf einen nachfolgenden Therapiezyklus deutlich schlechter ansprechen würden. Die derzeit hauptsächlich angewandten Behandlungsprotokolle sehen daher einen möglichst frühzeitigen Einsatz der Chemotherapie, mit möglichst hohen Dosen und kurzen Regenerationsphasen zwischen den Behandlungszyklen vor.[1] Die Log-cell-kill-Hypothese ist die theoretische Grundlage dafür, dass auch nach einer vollständigen Remission ein Patient intensiv weiter behandelt wird.[2]
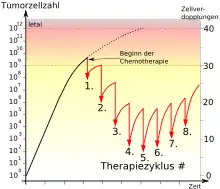
In der klinischen Realität ist bei den meisten humanen Tumoren die idealisierte Modellvorstellung allerdings nicht gegeben. Die Log-cell-kill-Hypothese kann zwar teilweise auch auf schnell wachsende solide Tumoren übertragen werden – auch wenn diese kein exponentielles Wachstum zeigen –, die Zellabtötungskinetik verläuft jedoch in den meisten Fällen wie in Diagramm 3 dargestellt.[2]
Das Tumorwachstum verläuft nach der sogenannten Gompertz-Kinetik (benannt nach Benjamin Gompertz). Das heißt, dass das Tumorwachstum mit zunehmender Größe langsamer wird. Im halblogarithmischen Diagramm ist dies durch die abflachende Kurve dargestellt. Viele Zellen verlassen mit zunehmendem Tumorwachstum den Zellzyklus und gehen in die sogenannte G0-Phase (Ruhephase) über. Das Tumorwachstum ist vom umgebenden Gefäßsystem, das ihn mit Sauerstoff und Nährstoffen versorgt, abhängig. Die Gefäßneubildung kann in vielen Fällen nicht mit dem Tumorwachstum Schritt halten. Deshalb gehen viele Zellen in die Ruhephase oder sterben ab (Tumornekrose). In dieser Phase ist die Empfindlichkeit gegenüber Chemotherapeutika erheblich reduziert. Aus diesem Grund wird zu Beginn einer Chemotherapie nur ein kleiner Teil der Tumorzellen abgetötet (siehe Diagramm 3). Als Folge des ersten Therapiezyklusses nimmt die Tumormasse ab und viele der ruhenden Krebszellen nehmen wieder am Zellzyklus teil. Diese Zellen können beim zweiten Zyklus dann abgetötet werden. Die Chemotherapie ist deshalb beim zweiten Zyklus wirksamer, als bei ersten Therapiezyklus, da ein höherer Prozentsatz (aber keine höhere Absolutzahl) an Krebszellen vernichtet wird. Bei weiteren Therapiezyklen steigt die Anzahl der resistenten Krebszellen an, was wiederum den Prozentsatz der abgetöteten Krebszellen herabsetzt.[6]
Literatur
Einzelnachweise
- H. E. Skipper: Perspectives in Cancer Chemotherapy: Therapeutic Design. In: Cancer Res 24, 1964, S. 1295–1302. PMID 14221786
- J. R. Siewert und V. Schumpelick: Praxis der Viszeralchirurgie. Verlag Springer, 2005, ISBN 3-540-21914-5
- M. Friedkin und A. Goldin: The use of dihydrofolate reductase in studies of mixed populations of sensitive and resistant leukemic cells. In: Cancer Res 22, 1962, S. 607–616. PMID 13895220
- Chemotherapie (Memento vom 5. Juni 2008 im Internet Archive) – Universität Jena
- O. A. Adam: Antineoplastische Chemotherapie. (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis. (PDF; 1,6 MB) LMU München
- H. D. Bruhn (Herausgeber) u. a.: Onkologische Therapie. Verlag Schattauer, 2003, ISBN 3-794-52165-X, S. 89–92. eingeschränkte Vorschau in der Google-Buchsuche