G-Protein Ras
Ras (Rat sarcoma) ist ein Proto-Onkogen, das für ein sogenanntes kleines G-Protein (monomer) codiert. Es wurde 1981 vom amerikanischen Molekularbiologen Robert Allan Weinberg beschrieben und ist damit das erste entdeckte Proto-Onkogen.
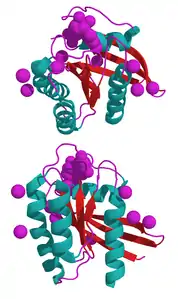
| GTPase NRas | ||
|---|---|---|
| ||
| mit GDP und Mg2+ nach PDB 3CON | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 189 Aminosäuren; 21,2 kDa | |
| Kofaktor | GDP/GTP | |
| Bezeichner | ||
| Gen-Namen | NRAS ; NRAS1 | |
| Externe IDs | ||
| Vorkommen | ||
| Homologie-Familie | HBG009351 | |
| Übergeordnetes Taxon | Chordatiere | |
| Orthologe | ||
| Mensch | Maus | |
| Entrez | 4893 | 18176 |
| Ensembl | ENSG00000009307 | ENSMUSG00000027852 |
| UniProt | P01111 | Q3TMF4 |
| Refseq (mRNA) | NM_002524 | NM_010937 |
| Refseq (Protein) | NP_002515 | NP_035067 |
| Genlocus | Chr 1: 115.05 – 115.06 Mb | Chr 3: 102.86 – 102.87 Mb |
| PubMed-Suche | 4893 | 18176 |
Funktion
Ras ist ein zentrales Glied verschiedener Signaltransduktionswege, die Wachstums- und Differenzierungsprozesse regulieren. Als monomeres GTP-bindendes Protein nimmt es die Funktion eines regulierten molekularen Schalters ein, mit dem zelluläre Prozesse an- oder abgeschaltet werden können. Ras wechselt dabei zwischen zwei Zuständen, in denen es entweder GTP gebunden hat (RasG) oder das GTP zu GDP hydrolysiert ist (Ras). Die Grundlage dieser molekularen Schalterfunktion basiert auf unterschiedlichen Proteinkonformationen bei der Bindung von GTP oder GDP. Ras kann nur im GTP-gebundenen Zustand mit weiteren Signal-Proteinen (sogenannten Effektoren) interagieren, die dann ihrerseits die Signalweiterleitung vermitteln. Da sowohl die intrinsische GTP-Hydrolyse (GTPase-Aktivität) als auch der intrinsische Nukleotidaustausch grundsätzlich sehr langsame Prozesse sind, wird die Lebensdauer des aktiven und inaktiven Zustands von Ras über Nukleotid-Austauschfaktoren (guanine-nucleotide exchange factor, GEF) und GTPase-aktivierende Proteine (GAP) gesteuert.
Signaltransduktionsweg
- am Beispiel des Rezeptor-Tyrosinkinase-Signaltransduktionsweges
Die Bindung eines Liganden an eine Rezeptor-Tyrosinkinase (RTK) bewirkt deren Dimerisierung, welche die Transphosphorylierung des Rezeptors zur Folge hat. Die phosphorylierten Tyrosine auf der RTK dienen nun als Andockstelle für das zytosolische Adapterprotein Grb2, welches wiederum konstitutiv mit dem Ras-GEF SOS (Son Of Sevenless) assoziiert ist. Die Autophosphorylierung des Rezeptors führt also zur Rekrutierung des Grb2/SOS-Protein-Komplexes zur Membran und damit in die unmittelbare Nähe von Ras. SOS aktiviert nun Ras, indem es die Freisetzung von GDP und den anschließenden Austausch mit GTP ermöglicht, welches im Zytosol in ca. zehnfach höherer Konzentration vorliegt. Aktiviertes Ras-GTP kann nun das Effektorprotein Raf-Kinase binden. Die Membranrekrutierung führt zur Aktivierung von Raf, unter anderem aufgrund einer Konformationsänderung. Aktive Raf-Kinase kann nun im Gegenzug die Kinase MEK durch Phosphorylierung aktivieren. Aktives MEK wiederum phosphoryliert und aktiviert die Erk-Kinase. Aktives Erk gelangt letztlich in den Zellkern, wo es durch Phosphorylierung eine Reihe von Transkriptionsfaktoren aktivieren kann.
Krebsforschung
Die Tatsache, dass in 20 bis 30 Prozent aller menschlichen Tumoren Punktmutationen im ras-Gen gefunden werden, unterstreicht die bedeutende Funktion von Ras bei der Kontrolle des Zellwachstums. Die onkogene Bedeutung von ras wird weiterhin durch die Beobachtung verstärkt, dass aktivierende NRAS-Mutationen typischerweise als Escape-Mechanismen nach einer Behandlung mit BRAF-Inhibitoren auftreten.[1] Die Punktmutationen der ras-Gene führen allesamt zum Verlust der GTPase-Bindungsaktivität von Ras, die auch in Gegenwart von GTPase aktivierenden Proteinen (GAP) nicht mehr angeregt werden kann. Da der Wechsel von der GTP-gebundenen Form zur GDP-Form blockiert ist, kommt es zu einer Akkumulation von aktivem Ras und damit zu einem permanenten wachsstumsstimulierenden Signal in der Zelle. Große Anstrengungen wurden unternommen, um die molekularen Grundlagen der Schalterfunktion von Ras-Proteinen zu verstehen und gegen onkogenes Ras gerichtete Antitumor-Medikamente zu entwickeln. Einige Formen von Ras wie z. B. KRAS spielen sogar eine entscheidende Rolle dabei, ob bestimmte onkologische Medikamente wirksam sind.
Siehe auch
- Ras-Raf-Signalweg
- Raf (Protein)
Literatur
- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Biochemie. 6 Auflage, Spektrum Akademischer Verlag, Heidelberg 2007, ISBN 978-3-8274-1800-5.
- Donald Voet, Judith G. Voet: Biochemistry. 3. Auflage, John Wiley & Sons, New York 2004, ISBN 0-471-19350-X.
- Bruce Alberts, Alexander Johnson, Peter Walter, Julian Lewis, Martin Raff, Keith Roberts: Molecular Biology of the Cell. 5. Auflage, Taylor & Francis, New York 2008, ISBN 978-0-8153-4106-2.
Einzelnachweise
- Carolina Hertzman Johansson, Suzanne Egyhazi Brage: BRAF inhibitors in cancer therapy. In: Pharmacology & Therapeutics. Band 142, Nr. 2, Mai 2014, S. 176–182, doi:10.1016/j.pharmthera.2013.11.011.